ПРИЛОГ 1
МЕТОДЕ УЗОРКОВАЊА И ИСПИТИВАЊА УЗОРАКА ХРАНЕ ЗА СЛУЖБЕНУ КОНТРОЛУ НИВОА ЕЛЕМЕНАТА У ТРАГОВИМА И ПРОЦЕСНИХ КОНТАМИНЕНАТА1
Овај прилог односи се на методе узорковања, припрему узорака, методе испитивања узорака и извештавање и тумачење резултата ради утврђивања присуства и нивоа у храни: олова, кадмијума, живе, неорганског калаја, неорганског арсена, 3-монохлорпропан-1,2-диола (3-MCPD), естара масних киселина 3-MCPD, глицидил естара масних киселина, полицикличних ароматичних угљоводоника (PAH), перхлората и акриламида.
А) ДЕФИНИЦИЈЕ2
Поједини изрази употребљени у овом прилогу имају следеће значење:
1) производна партија (серија или лот) јесте количина хране која се може идентификовати, испоручена у једном тренутку (одједном) и за коју је службено лице утврдило да има заједничке карактеристике (као што су порекло, сорта, врста, подручје, врста паковања, паковалац, пошиљалац или ознаке);
2) производна потпартија (подсерија или подлот) јесте физички одвојен и препознатљив дeо веће производне партије из кога се узимају узорци или на који се примењује метода узорковања;
3) појединачни узорак јесте количина хране узета са једног места из производне партије, односно потпартије;
4) збирни узорак јесте узорак састављен од свих појединачних узорака узетих из производне партије, односно потпартије;
5) лабораторијски узорак јесте репрезентативни део или количина збирног узорка намењена за лабораторијско испитивање;
6) упоредива величина или маса јесте разлика у величини или маси која није већа од 50%.
––––––––
1 Прилог 1 овог правилника усклађен је са Уредбом Комисије (ЕЗ) број 333/2007 од 28. марта 2007. године о утврђивању метода узорковања и испитивања за контролу нивоа елемената у траговима и процесних контаминената у прехрамбеним производима (Commission Regulation (EC) No 333/2007 of 28 March 2007 laying down the methods of sampling and analysis for the control of the levels of trace elements and processing contaminants in foodstuffs) и њеним изменама и допунама које су објављене у „Службеном листу Европске уније” до краја 2021. године.
2 Дефиниције дате у овом прилогу, које се односе на значење појединих израза, примењују се и на остале прилоге који су одштампани уз овај правилник.
Б) МЕТОДЕ УЗОРКОВАЊА
Б.1. Општa правила
Б.1.1. Лице које обавља узорковање
Узорковање обавља надлежни инспектор, у складу са поделом надлежности уређеном прописом који се односи на безбедност хране.
Б.1.2. Храна која се узоркује
Свака производна партија или потпартија хране предвиђена за испитивање узоркује се посебно.
Б.1.3. Мере предострожности
Током узорковања хране предузимају се мере предострожности како би се избегле било какве промене које би могле утицати на нивое контаминената у храни, негативно утицати на лабораторијско испитивање, или због којих би збирни узорци постали нерепрезентативни.
Б.1.4. Појединачни узорци
Када год је то могуће, појединачни узорци се узимају са различитих места у серији или подсерији.
Одступање од поступка узимања појединачних узорака наводи се у записнику о узорковању из одељка Б) пододељак Б.1. тачка Б.1.8. овог прилога.
Б.1.5. Припрема збирног узорка
Збирни узорак се добија обједињавањем појединачних узорака.
Б.1.6. Узорци за службене контроле, додатно стручно мишљење (жалба) и судски поступак
Узорци за сврхе службене контроле, додатна стручна мишљења (жалбе) и судске поступке узимају се из хомогенизованог збирног узорка.
Б.1.7. Паковање и достављање узорака
Сваки узорак ставља се у чисту, инертну посуду, кесу или контејнер који пружа одговарајућу заштиту од контаминације, губитка аналита адсорпцијом на унутрашњим зидовима посуде, кесе или контејнера и оштећења приликом транспорта. Потребно је предузети све мере предострожности како би се избегла промена састава узорака до које би могло доћи током транспорта или складиштења.
У случају узимања узорака за испитивање полицикличних ароматичних угљоводоника (у даљем тексту: PAH), ако је могуће, треба избегавати пластичне посуде јер могу да измене садржај PAH у узорку. Када год је то могуће, користе се инертне, стаклене посуде без PAH, које на одговарајући начин штите узорак од светлости. Ако је то практично немогуће, треба избегавати директан контакт узорка са пластиком, нпр. у случају чврстих узорака умотавањем узорка у алуминијску фолију пре него што се ставе у посуде за узорковање.
Б.1.8. Пломбирање и означавање узорака
Сваки узорак који се узима за службену контролу пломбира се и означава на месту узорковања.
О сваком узорковању сачињава се записник о узорковању који омогућава да свака производна партија или потпартија буде недвосмислено идентификована и у којем се наводи број производне партије/потпартије, датум и место узорковања, заједно са додатним подацима који би могли бити од користи при лабораторијском испитивању.
Б.2. Планови узорковања
Б.2.1. Подела производне партије на потпартије
Велике производне партије деле се на потпартије под условом да се потпартија може и физички одвојити. Када је реч о храни која се продаје у расутом стању (нпр. жита), за поделу прозводне партије на потпартије примењује се Табела 1. овог прилога. За остале производе примењује се Табела 2. овог прилога. Узимајући у обзир да маса производне партије није увек тачан збир маса потпартија, маса потпартије може прећи доленаведену масу за највише 20%.
Табела 1.
Подела производних партија на потпартије за храну која се продаје у расутом стању
|
Маса производне партије (у t) |
Маса (у t) или број потпартија |
|
≥ 1500 |
500 |
|
> 300 и < 1500 |
3 потпартије |
|
≥ 100 и ≤ 300 |
100 |
|
< 100 |
– |
Табела 2.
Подела производних партија на потпартије за осталу храну
|
Маса производне партије (у t) |
Маса (у t) или број потпартија |
|
≥ 15 |
15–30 |
|
< 15 |
– |
Б.2.2. Број појединачних узорака
За храну (осим сушених зачина или зачинског биља, сушених гљива, алги или лишајева и додатака исхрани), збирни узорак је најмање 1 kg или 1 l, осим ако то није могуће, нпр. ако се узорак састоји од једног паковања или јединице.
За сушене зачине или зачинско биље, сушене гљиве, алге или лишајеве и додатке исхрани, збирни узорак је најмање 100 gr или 100 ml.
За храну, осим додатака исхрани, минималан број појединачних узорака који се узима из производне партије или потпартије наведен је у Табели 3. овог прилога.
Табела 3.
Минималан број појединачних узорака који се узима из производне партије или потпартије
|
Маса или запремина производне партије/потпартије (у kg или l) |
Минималан број појединачних узорака које треба узети |
|
< 50 |
3 |
|
≥ 50 и ≤ 500 |
5 |
|
> 500 |
10 |
У случају да се ради о течним производима у великим паковањима, производне партије или потпартије треба темељно промешати непосредно пре узорковања, колико год је то могуће, ручно или помоћу механичких уређаја, у мери у којој то неће утицати на квалитет производа. У том случају се претпоставља да ће се контаминенти равномерно распоредити кроз целу производну партију или потпартију. Стога, да би се формирао збирни узорак, из производне партије или потпартије узимају се три појединачна узорка.
Ако се прозводна партија или потпартија састоји од појединачних паковања или јединица, за храну, осим додатака исхрани, број паковања или јединица (појединачни узорци) које се узимају за збирни узорак треба да буде у складу са Табелом 4а овог прилога.
Табела 4а
Број паковања или јединица (појединачних узорака) који се узимају за збирни узорак, кад се производна партија или потпартија састоји од појединачних паковања или јединица, осим у случају додатака исхрани
|
Број паковања или јединица у производној партији/потпартији |
Број паковања или јединица које треба узети |
|
≤ 25 |
најмање 1 паковање или јединица |
|
26–100 |
око 5%, а најмање 2 паковања или јединице |
|
> 100 |
око 5%, а највише 10 паковања или јединица |
Појединачни узорци треба да буду сличне масе/запремине. За храну, осим додатака исхрани, сушених зачина или зачинског биља, сушених гљива, алги или лишајева, маса/запремина појединачних узорака је најмање 100 g или 100 ml, тако да је збирни узорак најмање 1 kg или 1 l.
За сушене зачине или зачинско биље, суве гљиве, алге или лишајеве маса/запремина појединачног узорка није мања од 35 g или 35 ml, тако да је збирни узорак најмање 100 g или 100 ml.
Максималне концентрације за неоргански калај примењују се на садржај сваке лименке, али, из практичних разлога, узорци се узимају као збирни узорци. Ако је резултат теста за збирни узорак лименки мањи, али близу максималне концентрације за неоргански калај и ако се сумња да појединачне лименке могу прелазити максималне концентрације, треба спровести додатна испитивања.
За додатке исхрани, најмањи број и величина појединачних узорака треба да буду у складу са Табелом 4б овог прилога.
Табела 4б
Минимални број и величина појединачних узорака за додатке исхрани
|
Величина серије (број паковања) |
Број паковања (појединачних узорака) које треба узети за узорак |
Величина појединачног узорка |
|
1–50 |
1 |
Целокупан садржај паковања |
|
51–250 |
2 |
Целокупан садржај паковања |
|
251–1.000 |
4 |
Из сваког малопродајног паковања узетог за узорак половина садржаја паковања |
|
> 1.000 |
4 + 1 паковање на 1.000 малопродајних паковања са највише 25 малопродајних паковања |
≤ 10 паковања: из сваког малопродајног паковања, половина садржаја паковања > 10 паковања: из сваког паковања узима се једнака количина како би се добио узорак који одговара садржају 5 паковања |
|
Непознато (примењује се само за е-трговину) |
1 |
Целокупан садржај паковања |
Ако узорковање није могуће због неприхватљивих комерцијалних последица (на пример због облика паковања, оштећења у производној партији и сл.) или када није могуће применити горенаведену методу узорковања, узорковање се може спровести алтернативном методом, под условом да је та метода репрезентативна за узорковану производну партију или потпартију и да је у потпуности документована. То се уноси у записник из одељка Б) пододељак Б.1. тачка Б.1.8. овог прилога.
Б.2.3. Посебне одредбе за узорковање производних партија које садрже целе рибе упоредиве величине или масе
Број појединачних узорака који се узимају из производне партије прописан је у Табели 3. овог прилога. Збирни узорак, који обједињује све појединачне узорке, је најмање 1 kg, како је прописано у одељку Б) пододељак Б.2 тачка Б.2.2. овог прилога.
Када производна партија која се узоркује садржи ситну рибу (појединачне рибе масе < 1 kg), за формирање збирног узорка се као појединачни узорак узима цела риба. Када је маса добијеног збирног узорка већа од 3 kg, појединачни узорци се могу састојати од средњих делова рибе, од којих је сваки најмање 100 g, а који чине збирни узорак. За хомогенизацију узорка користи се цео део на који се примењује максимална дозвољена концентрација.
Средина рибе је тамо где је центар гравитације. У већини случајева центар гравитације се налази на леђном перају (ако риба има леђно пераје) или на пола пута између шкржног отвора и ануса.
Када производна партија која се узоркује садржи веће рибе (појединачне рибе масе ≥ 1 kg), појединачни узорак се састоји од средњег дела рибе. Маса сваког појединачног узорка је најмање 100 g.
За рибе средње величине (≥ 1 kg и < 6 kg), појединачни узорак се састоји од комада рибе узетог између кичме и трбуха у средњем делу рибе. За веома велике рибе (≥ 6 kg), појединачни узорак се узима са десне стране (гледано спреда) из меса дорзо-латералног мишића у средњем делу рибе. Када узимање таквог комада средњег дела рибе може довести до значајне економске штете, могу се, без обзира на величину производне партије, прихватити као довољни:
– три појединачна узорка од по најмање 350 g, или
– три појединачна узорка од по најмање 350 g, сваки из једнаког дела (175 g) меса мишића узетог близу репа и меса мишића узетог близу главе сваке рибе.
Б.2.4. Посебне одредбе за узорковање производних партија рибе које садрже целе рибе различите величине или масе
Када преовлађује риба одређене величине/категорије или масе (око 80% или више производне партије), узорак се узима од рибе преовлађујуће величине или масе. Сматра се да је узорак репрезентативан за целу производну партију.
Када одређена класа/категорија величине или масе не преовлађује, обезбеђује се да риба одабрана за узорак буде репрезентативна за производну партију. За такве случајеве посебна упутства су дата у Смерницама за узорковање целе рибе различите величине и/или масе3.
Б.2.5. Посебне одредбе за узорковање копнених животиња
За месо и изнутрице свиња, говеда, оваца, коза и копитара узима се узорак од 1 kg од најмање једне животиње. Ако није могуће узети узорак од 1 kg од најмање једне животиње, узимају се једнаке количине узорка од више животиња да би се добила количина узорка од 1 kg.
За месо живине, да би се добио збирни узорак од 1 kg, узоркују се једнаке количине од најмање три животиње. За изнутрице живине, да би се добио збирни узорак од 300 g, узоркују се једнаке количине од најмање три животиње.
За месо и изнутрице дивљачи из узгоја и дивљих копнених животиња узима се узорак од 300 g од најмање једне животиње. Ако није могуће узети узорак од 300 g од најмање једне животиње, узимају се једнаке количине узорка од више животиња, да би се добила количина узорка од 300 g.
Б.3. Узорковање у фази малопродаје
Узорковање хране у малопродаји спроводи се у складу са одељком Б) пододељак Б.2 тачка Б.2.2. овог прилога.
Ако узорковање није могуће због неприхватљивих комерцијалних последица (нпр. због облика паковања, оштећења у производној партији и сл.) или када није могуће применити горенаведену методу узорковања, може се применити алтернативна метода узорковања, под условом да је та метода репрезентативна за узорковану производну партију или потпартију и да је у потпуности документована.
В) ПРИПРЕМА И ИСПИТИВАЊЕ УЗОРАКА
В.1. Лабораторијски стандарди квалитета
Лабораторије које спроводе испитивања хране на присуство конатаминаната за службену контролу треба да учествују у одговарајућим лабораторијским програмима за испитивање оспособљености у складу са Међународним усклађеним протоколом за проверу оспособљености хемијских аналитичких лабораторија4 развијеним у складу са IUPAC/ISO/АОАC.
Лабораторије требa да имају успостављен интерни систем за контролу квалитета. Примери за то су Смернице IUPAC/ISO/АОАC за интерну контролу квалитета у аналитичким хемијским лабораторијима5.
Тачност испитивања процењује се коришћењем у испитивању одговарајућих сертификованих референтних материјала, кад год је то могуће.
––––––––
3 https://ec.europa.eu/food/safety/chemical-safety/contaminants/sampling-and-analysis
4 Међународни усклађени протокол за проверу квалитета рада (хемијских) аналитичких лабораторија (The international harmonized protocol for the proficiency testing of analytical chemistry laboratories), аутори М. Thompson, S.L.R. Ellison и R. Wood, Pure. Appl. Chem., 2006, 70, 145–196.
5 Приредили М. Thompson и R. Wood, Pure. Appl. Chem., 1995, 67, 649-666.
В.2. Припрема узорка
В.2.1. Мере предострожности и општа правила
Основни захтев је да се припреми репрезентативан и хомоген лабораторијски узорак, без секундарне контаминације.
Сав узорковани материјал који је достављен у лабораторију користи се за припрему лабораторијског узорка.
Усклађеност са прописаним максималним концентрацијама утврђује се на основу концентрације утврђене у лабораторијским узорцима.
В.2.2. Посебни поступци за припрему узорка
В.2.2.1. Посебни поступци за олово, кадмијум, живу, неоргански калај и неоргански арсен
Лабораторија треба да обезбеди да не дође до контаминације узорака током припреме. Кад год је могуће, апарати и опрема који долазе у контакт са узорком не треба да садрже метале који се утврђују, односно треба да буду израђени од инертних материјала, на пример пластике као што је полипропилен, политетрафлуоретилен (PTFE), итд. Сав прибор се чисти киселином како би се ризик од контаминације смањио на најмању могућу меру. Све оштрице треба да буду израђене од висококвалитетног нерђајућег челика. За сечење крајева може се користити висококвалитетни нерђајући челик.
Постоји много задовољавајућих специфичних поступака припреме узорака који се могу користити за производе који се разматрају. За оне аспекте који нису посебно обухваћени овим прилогом, може бити једнако задовољавајући стандард SRPS EN 13804 Прехрамбени производи – Одређивање елемената и њихових хемијских врста – Општа разматрања и специфични захтеви, али и друге методе припреме узорка су једнако валидне.
У случају неорганског калаја, посебна пажња се обраћа на то да сав узорак буде у потпуности растворен, јер је познато да може доћи до губитака услед хидролизе Sn(IV) оксида.
В.2.2.2. Посебни поступци за полицикличне ароматичне угљоводонике
Лабораторија треба да обезбеди да се узорци не контаминирају током припреме узорака. Посуде се испирају ацетоном или хексаном високе чистоће пре употребе како би се ризик од контаминације свео на најмању могућу меру. Кад год је могуће, апарати и опрема која долази у контакт са узорком треба да буде направљена од инертних материјала, нпр. алуминијума, стакла или полираног нерђајућег челика. Потребно је избегавати пластику као што је полипропилен, PTFE и сл., јер се аналити могу адсорбовати од стране ових материјала.
За лабораторијско испитивање полицикличких ароматичних угљоводоника у какаoу и производима од какаа, утврђивање садржаја масти спроводи се у складу са методом АОАС 963.15. За утврђивање садржаја масти у какао зрну (какаовцу) могу се применити и друге методе чији је поступак истоветан поступку утврђивања садржаја масти и за који се може доказати да се употребљеним поступком за утврђивање садржаја масти добија једнака вредност садржаја масти.
В.2.3. Обрада узорка који је примљен у лабораторији
Када је то неопходно, цео збирни узорак фино се самеље и детаљно измеша, користећи поступак којим се доказано постиже потпуна хомогенизација.
В.2.4. Узорци за службене контроле, додатно стручно мишљење (жалба) и судски поступак
Узорци за сврхе службене контроле, додатна стручна мишљења (жалбе) и судске поступке, узимају се из хомогенизованог збирног узорка.
В.3. Методе испитивања
В.3.1. Дефиниције
Поједини изрази употребљени у овом прилогу имају следеће значење:
1) поновљивост (r) јесте вредност испод које се може очекивати да се апсолутна разлика између појединачних резултата испитивања добијена под условима поновљивости (нпр. исти узорак, исти испитивач, исти инструмент, иста лабораторија и кратак временски период) налази у оквиру одговарајућег интервала поузданости (обично 95%), па је отуда r = 2,8 x sr;
2) sr јесте стандардна девијација израчуната из резултата добијених под условима поновљивости;
3) RSDr јесте релативна стандардна девијација израчуната из резултата добијених под условима поновљивости;
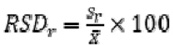
4) репродуктивност (R) јесте вредност испод које се може очекивати да се апсолутна разлика између појединачних резултата испитивања добијена под условима репродуктивности (нпр. на идентичном материјалу који су испитивачи добили у различитим лабораторијима, користећи стандардизовану методу за ипитивање) налази у оквиру одговарајућег интервала поузданости (обично 95 %), R = 2,8 x sr;
5) SR јесте стандардна девијација израчуната из резултата добијених под условима репродуктивности;
6) RSDR јесте релативна стандардна девијација израчуната из резултата добијених под условима репродуктивности;
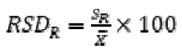
7) граница детекције (LOD) јесте најмањи измерени (аналит) садржај за који је могуће потврдити присуство аналита са разумном статистичком вероватноћом;
8) граница квантификације (LOQ) јесте најмања количина аналита која се може одредити уз разумну статистичку вероватноћу;
9) HORRAT6r јесте добијена RSDr подељена са вредношћу RSDr која је процењена уз помоћ Horwitz-ове једначине7 (модификоване), како је наведено у подтачки В.3.3.1. овог прилога – Напомене за критеријуме изводљивости, користећи претпоставку да је r = 0,66 R;
10) HORRAT5R јесте добијена RSDR подељена са вредношћу RSDR која је процењена уз помоћ Horwitz-ове једначине6 (модификоване), како је наведено у подтачки В.3.3.1. овог прилога – Напомене за критеријуме изводљивости;
11) u јесте комбинована стандардна мерна несигурност добијена коришћењем појединачних стандардних мерних несигурности које су у вези са улазним количинама у мерном моделу8;
12) U јесте проширена мерна несигурност, добијена коришћењем фактора покривености 2, који даје ниво поузданости од 95%;
13) Uf јесте највећа стандардна мерна несигурност.
В.3.2. Општи захтеви
За лабораторијска испитивања нивоа неорганског калаја примењују се лабораторијске методе које се примењују за укупни калај.
За лабораторијска испитивања олова у вину примењују се методе и правила које је утврдио ОIV9, у складу са посебним прописом.
––––––––
6 Horwitz W. e Albert, R., 2006, The Horwitz Ratio (HorRat): A useful Index of Method Performance with respect to Precision, Journal of AOAC International, Vol. 89, 1095– 1109.
7 Thompson, Analyst, 2000, стр. 125. и 385–386.
8 Међународни речник метрологије – Основни и општи појмови и придружени појмови (VIM), JCGM 200: 2008 (International vocabulary of metrology – Basic and general concepts and associated terms (VIM), JCGM 200:2008).
9 Међународна организација за винову лозу и вино (Organisation international de la vigne et du vin – International Organisation of Vine and Wine).
За лабораторијска испитивања нивоа неорганског арсена примењују се лабораторијске методе које се примењују за укупни арсен.
Ако је укупна концентрација арсена испод максимално дозвољене концентрације за неоргански арсен, не спроводи се додатно испитивање и сматра се да је узорак у складу са максимално дозвољеним концентрацијама за неоргански арсен.
Ако је укупна концентрација арсена на нивоу максимално дозвољене концентрације или изнад ње, спроводи се додатно испитивање како би се утврдило да ли је концентрација неорганског арсена изнад максимално дозвољене концентрације за неоргански арсен.
В.3.3. Посебни захтеви
В.3.3.1. Критеријуми изводљивости за методе испитивања олова, кадмијума, живе, неорганског калаја и неорганског арсена
Када нису прописане посебне методе за утврђивање контаминaната у храни, лабораторије могу да изаберу било коју валидирану методу испитивања за одређени контаминент, под условом да изабрана метода испуњава посебне критеријуме изводљивости наведене у табелама 5, 6. и 7. овог прилога.
Ако је могуће, валидација укључује сертификован референтни материјал.
(a) Критеријуми изводљивости за методе испитивања олова, кадмијума, живе, неорганског калаја и неорганског арсена
Табела 5.
|
Параметар |
Критеријум |
|||
|
Применљивост |
Храна наведена у посебном пропису о максималним концентрацијама одређених контаминената у храни |
|||
|
Специфичност |
Без спектралних интерференција или утицаја матрикса |
|||
|
Поновљивост (RSDr) |
HORRATr < 2 |
|||
|
Репродуктивност (RSDR) |
HORRATR < 2 |
|||
|
Аналитички принос |
Примењује се одељак Г) пододељак Г.1. тачка Г.1.2. овог прилога |
|||
|
Граница детекције (LOD) |
= три десетине LOQ |
|||
|
Граница квантификације (LOQ) |
Неоргански калај |
≤ 10 mg/kg |
||
|
Oлово |
ML ≤ 0,02 mg/kg |
0,02˂ ML˂ 0,1 mg/kg |
ML ≥ 0,1 mg/kg |
|
|
≤ ML |
≤ две трећине ML |
≤ једна петина ML |
||
|
Кадмијум, жива |
ML ≤ 0,02 mg/kg |
0,02 < ML < 0,1 mg/kg |
ML je ≥ 0,1 mg/kg |
|
|
≤ две петине ML-a |
≤ две петине ML |
≤ једна петина ML |
||
|
Неоргански арсен и укупни арсен |
ML ≤ 0,03 mg/kg |
0,03 < ML < 0,1 mg/kg |
ML je ≥ 0,1 mg/kg |
|
|
≤ ML |
≤ две трећине ML |
≤ две трећине ML |
||
ML = максимални ниво (maximum level)
(б) Критеријуми изводљивости за методе испитивања за 3-монохлорпропан-1,2-диол (3-MCPD), естре масних киселина 3-MCPD и глицидил естре масних киселина
Табела 6а
Критеријуми изводљивости за методе испитивања за 3-MCPD за храну који се односе на 3-MCPD у посебном пропису о максималним концентрацијама одређених контаминената у храни
|
Параметар |
Критеријум |
|
Применљивост |
Храна наведена у одељку који се односи на 3-MCPD у посебном пропису о максималним концентрацијама одређених контаминената у храни |
|
Специфичност |
Без спектралних интерференција или утицаја матрикса |
|
Теренска слепа проба |
Мање од LOD |
|
Поновљивост (RSDr) |
0,66 х RSDr како је добијена из Horwitz-ове једначине (модификоване) |
|
Репродуктивност (RSDR) |
Добијена из Horwitz-ове једначине (модификоване) |
|
Аналитички принос |
75–110% |
|
Граница детекције (LOD) |
≤ 5 μg/kg (изражено на суву материју) |
|
Граница квантификације (LOQ) |
≤ 10 μg/kg (изражено на суву материју) |
Табела 6б
Критеријуми изводљивости за методе испитивања за 3-MCPD за храну који се односе на суму 3-MCPD и 3-MCPD естара масних киселина, изражену као 3-MCPD у посебном пропису о максималним концентрацијама одређених контаминената у храни
|
Параметар |
Критеријум |
|
Применљивост |
Храна наведена у одељку који се односи на суму 3-MCPD и 3-MCPD естара масних киселина, изражену као 3-MCPD у посебном пропису о максималним концентрацијама одређених контаминената у храни. |
|
Специфичност |
Без спектралних интерференција или утицаја матрикса |
|
Теренска слепа проба |
Мање од LOD |
|
Поновљивост (RSDr) |
0,66 х RSDr како је добијена из Horwitz-ове једначине (модификоване) |
|
Репродуктивност (RSDR) |
Добијена из Horwitz-ове једначине (модификоване) |
|
Аналитички принос |
75–110% |
|
Граница детекције (LOD) |
≤ 7 μg/kg |
|
Граница квантификације (LOQ) |
≤ 14 μg/kg |
Табела 6в
Критеријуми изводљивости за методе испитивања 3-MCPD естара масних киселина изражене као 3-MCPD за храну која се односи на суму 3-MCPD и 3-MCPD естара масних киселина, изражену као 3-MCPD у посебном пропису о максималним концентрацијама одређених контаминената у храни
|
Параметар |
Критеријум |
|
|
Применљивост |
Храна наведена у одељку који се односи на суму 3-MCPD и 3-MCPD естара масних киселина, изражену као 3-MCPD у посебном пропису о максималним концентрацијама одређених контаминената у храни. |
|
|
Специфичност |
Без спектралних интерференција или утицаја матрикса |
|
|
Поновљивост (RSDr) |
0,66 х RSDr, како је добијена из Horwitz-ове једначине (модификоване) |
|
|
Репродуктивност (RSDR) |
Добијена из Horwitz-ове једначине (модификоване) |
|
|
Аналитички принос |
70–125% |
|
|
Граница детекције (LOD) |
Три десетине LOQ |
|
|
Граница квантификације (LOQ) за биљна уља и масти, рибља уља и уља из других морских организама који се стављају на тржиште за крајњег корисника или за употребу као састојак хране (осим девичанских маслинових уља) и биљна уља и масти, рибља уља и уља из других морских организама намењена за производњу дечје хране и прерађене хране на бази житарица за одојчад и малу децу |
≤ 100 μg/kg у уљима и мастима |
|
|
Граница квантификације (LOQ) за почетне формуле за одојчад, прелазне формуле за одојчад и храну за посебне медицинске потребе намењену за одојчад и малу децу и храна за малу децу (у праху) |
≤ две петине максимално дозвољене концентрације |
|
|
Граница квантификације (LOQ) за почетне формуле за одојчад, прелазне формуле за одојчад и храну за посебне медицинске потребе намењену за одојчад и малу децу и храну за малу децу (течна) |
≤ 15 μg/kg масти |
|
Табела 6г
Критеријуми изводљивости за методе испитивања глицидил естара масних киселина изражених као глицидол
|
Параметар |
Критеријум |
|
Применљивост |
Храна наведена у одељку који се односи на глицидил естре масних киселина изражене као глицидол у посебном пропису о максималним концентрацијама одређених контаминената у храни. |
|
Специфичност |
Без спектралних интерференција или утицаја матрикса |
|
Поновљивост (RSDr) |
0,66 х RSDr како је добијена из Horwitz-ове једначине (модификоване) |
|
Репродуктивност (RSDR) |
Добијена из Horwitz-ове једначине (модификоване) |
|
Аналитички принос |
70–125% |
|
Граница детекције (LOD) |
Три десетине LOQ |
|
Граница квантификације (LOQ) за биљна уља и масти, рибља уља и уља из других морских организама који се стављају на тржиште за крајњег корисника или за употребу као састојак хране и биљна уља и масти, рибља уља и уља из других морских организама намењена за производњу дечје хране и прерађене хране на бази житарица за одојчад и малу децу |
≤ 100 μg/kg у уљима и мастима |
|
Граница квантификације (LOQ) за: – почетне формуле за одојчад, прелазне формуле за одојчад и храну за посебне медицинске потребе намењену за одојчад и малу децу и храна за малу децу (у праху) са садржајем масти < 65%; – почетне формуле за одојчад, прелазне формуле за одојчад и храну за посебне медицинске потребе намењену за одојчад и малу децу и храну за малу децу (течна) са садржајем масти < 8%. |
≤ две петине максимално дозвољене концентрације |
|
Граница квантификације (LOQ) за: – почетне формуле за одојчад, прелазне формуле за одојчад и храну за посебне медицинске потребе намењену за одојчад и малу децу и храна за малу децу (у праху) са садржајем масти ≥ 65%; – почетне формуле за одојчад, прелазне формуле за одојчад и храну за посебне медицинске потребе намењену за одојчад и малу децу и храну за малу децу (течна) са садржајем масти ≥ 8%. |
≤ 31 μg/kg масти |
(в) Критеријуми изводљивости за методе испитивања полицикличних ароматичних угљоводоника
Четири полициклична ароматична угљоводоника, на које се примењују критеријуми, јесу: бензо(a)пирен, бензо(a)антрацен, бензо(b)флуорантен и кризен.
Табела 7.
|
Параметар |
Критеријум |
|
Применљивост |
Храна наведена у посебном пропису о максималним концентрацијама одређених контаминената у храни |
|
Специфичност |
Без спектралних интерференција или утицаја матрикса |
|
Поновљивост (RSDr) |
HORRATr вредности мање од 2 |
|
Репродуктивност (RSDR) |
HORRATR вредности мање од 2 |
|
Аналитички принос |
50–120% |
|
Граница детекције (LOD) |
≤ 0,30 μg/kg за сваку од четири супстанце |
|
Граница квантификације (LOQ) |
≤ 0,90 μg/kg за сваку од четири супстанце |
(в) Критеријуми изводљивости за методе испитивања за акриламид
Табела 8.
|
Параметар |
Критеријум |
|
Применљивост |
Све категорије хране |
|
Специфичност |
Без спектралних интерференција или утицаја матрикса |
|
Теренска слепа проба |
Мање од границе детекције (LOD) |
|
Поновљивост (RSDr) |
0,66 х RSDr како је добијена из Horwitz-ове једначине (модификоване) |
|
Репродуктивност (RSDR) |
Добијена из Horwitz-ове једначине (модификоване) |
|
Аналитички принос |
75–110% |
|
Граница детекције (LOD) |
Три десетине LOQ |
|
Граница квантификације (LOQ) |
За храну са референтним вредностима < 125 μg/kg: ≤ две петине нивоа референтне вредности, међутим не захтева се да буде нижа од 20 μg/kg. За храну са нивоом референтне вредности ≥ 125 μg/kg: ≤ 50 μg/kg |
(в) Критеријуми изводљивости за методе испитивања за перхлорат
Табела 9.
|
Параметар |
Критеријум |
|
Применљивост |
Све категорије хране |
|
Специфичност |
Без спектралних интерференција или утицаја матрикса |
|
Поновљивост (RSDr) |
0,66 х RSDr како је добијена из Horwitz-ове једначине (модификоване) |
|
Репродуктивност (RSDR) |
Добијена из Horwitz-ове једначине (модификоване) |
|
Аналитички принос |
70–110% |
|
Граница детекције (LOD) |
Три десетине LOQ |
|
Граница квантификације (LOQ) |
≤ две петине максимално дозвољене концентрације |
Напомене за критеријуме изводљивости:
Horwitz-ова једначина10 (за концентрације 1,2 × 10-7 ≤ С ≤ 0,138) и модификована Horwitz-ова једначина11 (за концентрације С < 1,2 × 10-7) су генерализоване једначине за прецизност, независне од аналита и матрикса и зависе искључиво од концентрације за све рутинске методе испитивања.
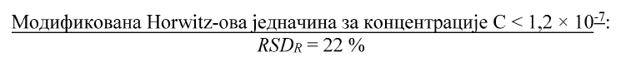
где је:
RSDR релативна стандардна девијација израчуната из резултата добијених у условима репродуктивности
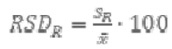
С однос концентрације (тј. 1 = 100 g/100g, 0,001 = 1.000 mg/kg). Модификована Horwitz-ова једначина примењује се за концентрације C < 1,2 × 10-7.
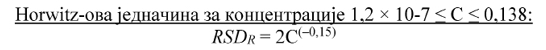
где је:
RSDR релативна стандардна девијација израчуната из резултата добијених у условима репродуктивности
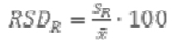
С однос концентрације (тј. 1 = 100 g/100g, 0,001 = 1.000 mg/kg). Horwitz-ова једначина примењује се за концентрације 1,2 × 10-7 ≤ C ≤ 0,138.
В.3.3.2. Приступ „примереност за примену”
За интерно валидиране методе може се користити приступ „примереност за примену”12, као алтернатива за процену њихове примерености за службену контролу. Методе које су примерене за службену контролу треба да дају резултате са комбинованом стандардном мерном несигурношћу (u), којa је мања од највеће стандардне мерне несигурности израчунате уз помоћ следеће формуле:
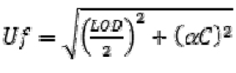
где је:
Uf највећа стандардна мерна несигурност (μg/kg);
граница детекције (LOD) граница детекције методе (μg/kg) која испуњава критеријуме изводљивости из подтачке В.3.3.1. овог прилога за концентрацију која се разматра;
C концентрација која се разматра (μg/kg);
α нумерички фактор који се користи у зависности од вредности C, а вредности које се користе дате су у табели 10. овог прилога.
Табела 10.
Нумеричке вредности које се користе за константу α, у зависности од концентрације која се разматра
|
C (μg/kg) |
Α |
|
≤ 50 |
0,2 |
|
51 до 500 |
0,18 |
|
501 до 1.000 |
0,15 |
|
1.001 до 10.000 |
0,12 |
|
> 10.000 |
0,1 |
––––––––
10 W. Horwitz, L.R. Kamps, K.W. Boyer, J.Assoc.Off.Analy.Chem.,1980, 63, 1344.
11 Thompson, Analyst, 2000, стр. 125 и 385-386.
12 M. Thompson and R. Wood, Accred. Qual. Assur., 2006, стр. 10. и 471.-478.
Аналитичар треба да користи и Извештај о односу између аналитичких резултата, мерне несигурности, фактора аналитичког приноса и одредаба законодавства ЕУ о храни и храни за животиње13.
Г) ИЗВЕШТАВАЊЕ И ТУМАЧЕЊЕ РЕЗУЛТАТА
Г.1. Извештавање
Г.1.1. Изражавање резултата
Резултати се изражавају у истим јединицама и заокружују се на исти број децимала као и максималне концентрације уређене посебним прописом који се односи на максималне концентрације одређених контаминената у храни.
Г.1.2. Израчунавање аналитичког приноса
Ако је у аналитичкој методи коришћен поступак екстракције, аналитички резултат се коригује за аналитички принос. У том случају, у извештају се наводи ниво аналитичког приноса.
Ако се у аналитичкој методи не примењује екстракција (нпр. код метала), резултат се не коригује за аналитички принос ако је правилним коришћењем одговарајућег сертификованог референтног материјала доказано да је добијена сертификована концентрација унутар граница мерне несигурности (тј. велика тачност мерења). У случају да је резултат изражен без корекције за аналитички принос, то треба и да се наведе у извештају.
Г.1.3. Мерна несигурност
Резултат испитивања изражава се као x +/– U, где је x аналитички резултат, а U је проширена мерна несигурност, добијена коришћењем фактора покривености 2, који даје ниво поузданости од 95% (U = 2u).
Аналитичар узима у обзир и Извештај о односу између аналитичких резултата, мерне несигурности, фактора аналитичког приноса и одредаба законодавства ЕУ о храни и храни за животиње14.
Г.2. Тумачење резултата
Г.2.1. Прихватање производне партије/потпартије
Производна партија или потпартија се прихвата ако аналитички резултат за лабораторијски узорак не прелази одговарајућу максималну концентрацију уређену посебним прописом који се односи на максималне концентрације одређених контаминената у храни, узимајући у обзир проширену мерну несигурност и корекцију резултата за аналитички принос, ако је у коришћеној аналитичкој методи примењен поступак екстракције.
Г.2.2. Одбијање производне партије/потпартије
Производна партија или потпартија се одбија ако аналитички резултат за лабораторијски узорак прелази одговарајућу максималну концентрацију уређену посебним прописом који се односи на максималне концентрације одређених контаминената у храни, узимајући у обзир проширену мерну несигурност и корекцију резултата за аналитички принос, ако је у коришћеној аналитичкој методи примењен поступак екстракције.
––––––––
13 Извештај о односу између аналитичких резултата, мерне несигурности, фактора аналитичког приноса и одредaбa законодавства ЕУ о храни и храни за животиње (Report on the relationship between analytical results, measurement uncertainty, recovery factors and the provisions of EU food and feed legislation) http://ec.europa.eu/food/food/chemicalsafety/ contaminants/report-sampling_analysis_ 2004_en.pdf.
14 Извештај о односу између аналитичких резултата, мерне несигурности, фактора аналитичког приноса и одредaбa законодавства ЕУ о храни и храни за животиње (Report on the relationship between analytical results, measurement uncertainty, recovery factors and the provisions of EU food and feed legislation) http://ec.europa.eu/food/food/chemicalsafety/ contaminants/report-sampling_analysis_ 2004_en.pdf.
ПРИЛОГ 2
МЕТОДЕ15 УЗОРКОВАЊА И ИСПИТИВАЊА УЗОРАКА ХРАНЕ ЗА СЛУЖБЕНУ КОНТРОЛУ НИВОА МИКОТОКСИНА16
1. ОПШТЕ ОДРЕДБЕ
Дефиниције
Примењују се дефиниције из Прилога 1 одељак А) овог правилника, као и следеће дефиниције:
1) подузорак јесте количина материјала узетог из збирног узорка за контролу склероција главице ражи визуалним прегледом;
2) аналитички принос (Rec, %) јесте % добијен применом формуле x/xref × 100%, при чему је:
x – измерена концентрација (код обогаћених узорака коригована за позадинску концентрацију, ако није реч о слепом узорку), и
xref – референтна концентрација (концентрација сертификованог референтног материјала (CRM), материјала из тестова оспособљености или обогаћеног узорка);
3) мерно одступање јесте разлика између измерене вредности и референтне концентрације;
4) релативна стандардна девијација поновљивости (RSDr) јесте релативна стандардна девијација (%) израчуната из резултата добиjених под условима поновљивости (прецизност поновљивости): исти испитивач примењује исту методу на истом узоркованом материјалу у једној лабораторији помоћу истог инструмента у кратком временском интервалу (један дан или један низ-секвенца);
5) релативна стандардна девијација репродуктивности унутар лабораторије (RSDwR) јесте релативна стандардна девијација (%) израчуната из резултата добијених под условима унутар лабораторијске репродуктивности (средња прецизност): иста метода примењује се на истом узоркованом материјалу у једној лабораторији, али у различитим данима (по могућности у дужем временском интервалу), а може укључивати и друге услове, као што су различити испитивачи и/или различити (еквивалентни) инструменти;
6) релативна стандардна девијација репродуктивности (RSDR) јесте релативна стандардна девијација (%) израчуната из резултата добијених под условима репродуктивности (међулабораторијска прецизност), што значи да исти материјал анализирају различите лабораторије. RSDR се посебно може утврдити на основу међулабораторијских студија и тестова оспособљености;
7) граница квантификације (LОQ) јесте најмањи садржај аналита који се може измерити са оправданом статистичком сигурношћу. То значи најнижи успешно валидирани ниво, тј. најнижа испитана концентрација аналита у узоркованом материјалу за коју су доказано испуњени критеријуми за искоришћење, прецизност и идентификацију17;
8) циљна концентрација скрининга (screening target concentration – STC) јесте релевантна концентрација за детекцију микотоксина у узорку. Када је сврха испитивање уклађености са прописаним максималним концентрацијама, STC је једнака применљивој максималној концентрацији. За остале потребе или када није прописана максимална концентрација, STC је унапред одређена од стране лабораторије;
––––––––
15 Прилог 2 овог правилника усклађен је са Спроведбеном уредбом Комисије (ЕУ) број 2023/2782 од 14. децембра 2023. године о утврђивању метода за узорковање и испитивање за контролу нивоа микотоксина у храни и о стављању ван снаге Уредбе (ЕЗ) број 401/2006 (Commission Implementing Regulation (EU) No 2023/2782 of 14 December 2023 laying down the methods of sampling and analysis for the control of the levels of mycotoxins in food and repealing Regulation (EC) No 401/2006).
16 Смернице за надлежне органе за контролу усклађености са законодавством ЕУ о афлатокси-нима доступне су на: http://europa.eu.int/comm/food/food/chemicalsafety/сontaminants /aflatoxin_guidance_en.pdf. Смерницама се дају додатне практичне информације, али информације садржане у смерницима су подређене одредбама прописаним у овом правилнику.
17 Границе квантификације које одговарају сврси су генерално ниже за процену ризика него за службену контролу ради провере усаглашености са прописаним максималним концентрацијама јер је циљ да се прикупе нумерички подаци за већину анализираних узорака (тј. да се избeгну лево цензурисани подаци) како би се могле спровести тачне процене изложености. За потребе мониторинга, може се прихватити пријављивање нивоа испод границе квантификације, како је и прописано у овом прилогу.
9) метода скрининга јесте метода која се користи за избор оних узорака чије концентрације микотоксина са одређеном сигурношћу премашују STC. За потребе скрининга микотоксина, постојање 95% сигурности сматра се погодним за сврху, а резултат скрининга изражава се као „негативан” или „сумњив”. Методе скрининга омогућавају економично испитивање великог броја узорака чиме се повећава могућност откривања нових случајева високе изложености и ризика за здравље потрошача. Ове методе се заснивају на биоаналитичким методама, LC-MS или HPLC методама (течна хроматографија високих перформанси или течна хроматографија – масена спектрометрија). Резултати узорака који премашују граничну вредност се проверавају и, у ту сврху, оригинални узорак се подвргава потпуно новом испитивању које се спроводи потврдном методом;
10) негативан узорак јесте узорак чији је садржај микотоксина у узорку < STC са сигурношћу од 95% (тј. постоји 5% могућности да су узорци нетачно приказани као негативни);
11) лажно негативан узорак јесте узорак чији је садржај микотоксина > STC, али је идентификован као негативан;
12) сумњив узорак (оријентационо позитиван) јесте узорак који премашује граничну вредност и може да садржи количине микотоксина веће од STC;
13) лажно сумњив узорак јесте негативни узорак који је идентификован као сумњив;
14) потврдне методе јесу методе које пружају потпуне или додатне информације које омогућавају да се микотоксин недвосмислено идентификује и квантификује на нивоу значајности;
15) граничнa вредност јесте одговор, сигнал или концентрација добијена методом скрининга, изнад које је узорак класификован као „сумњив”. Гранична вредност се одређује током валидације и узима у обзир варијабилност мерења;
16) негативан контролни узорак (слепа проба матрикса) јесте узорак за који се зна да у њему нема микотоксина који се проверава претходним одређивањем користећи потврдну методу довољне осетљивости или другом методом, или ако се такав узорак не може добити, материјал сa најнижим могућим нивоом, ако се на основу тог нивоа може закључити да је метода скрининга погодна за ту сврху;
17) узорак за који је познато да је слободан јесте узорак који садржи количину аналита која није већа од једне петине STC. Ако се ниво може квантификовати потврдном методом, ниво треба узети у обзир за процену валидације;
18) позитиван контролни узорак јесте узорак који садржи микотоксин у циљној концентрацији скрининга, нпр. сертификовани референтни материјал, материјал познатог садржаја (нпр. материјал за испитивање из тестова оспособљености) или материјал који је на другачији начин довољно окарактерисан уз помоћ потврдне методе. Ако не постоји ниједна од претходно наведених могућности, може се користити мешавина узорака са различитим нивоима контаминације или обогаћени узорак припремљен у лабораторији и који је довољно окарактерисан, под условом да се докаже да је ниво контаминације проверен.
А.1. Општа правила
А.1.1. Лице које обавља узорковање
Узорковање обавља надлежни инспектор, у складу са поделом надлежности уређеном прописима који се односе на безбедност хране.
А.1.2. Храна која се узоркује
Свака производна партија коју треба испитивати узоркује се посебно. У складу са посебним правилима за узорковање за различите микотоксине, велике производне партије деле се у потпартије које се узоркују посебно.
А.1.3. Мере предострожности
Током узорковања хране и припреме узорака предузимају се мере предострожности како би се избегле било какве промене које би могле:
– утицати на садржај микотоксина;
– негативно утицати на аналитичко одређивање;
– учинити збирне узорке нерепрезентативним;
– утицати на безбедност хране производних партија које се узоркују.
Такође, треба предузети све потребне мере за заштиту лица која узимају узорке.
А.1.4. Појединачни узорци
Када год је то могуће, појединачни узорци се узимају са различитих места у производној партији или потпартији.
Одступање од поступка узимања појединачних узорака наводи се у записнику о узорковању из дела 1. одељак А) пододељак А.1. тачка А.1.8. овог прилога.
А.1.5. Припрема збирног узорка
Збирни узорак се добија обједињавањем појединачних узорака.
А.1.6. Дупли узорци
Дупли узорци за сврхе службене контроле, додатна стручна мишљења (жалбе) и судске поступке узимају се из хомогенизованог збирног узорка.
А.1.7. Паковање и достављање узорака
Сваки узорак се ставља у чисту, инертну посуду која пружа одговарајућу заштиту од контаминације и оштећења у транспорту. Потребно је предузети све мере предострожности како би се избегла промена састава узорака до које би могло доћи током транспорта или складиштења.
А.1.8. Пломбирање и означавање узорака
Сваки узорак који се узима за службену контролу се пломбира и означава на месту узорковања.
О сваком узорковању сачињава се записник о узорковању који омогућава да свака производна партија буде недвосмислено идентификована и у којем се наводи датум и место узорковања, заједно са додатним подацима који би могли бити од користи при лабораторијском испитивању.
А.2. Различити типови производних партија (учесталост узорковања)
Храна се може стављати на тржиште у расутом стању, посудама или појединачним паковањима, попут врећа, врећица и малопродајних/појединачних паковања. Метода узорковања може се применити на све наведене различите облике у којима се производи стављају на тржиште.
Следећа формула може се користити за учесталост узорковања прозводних партија које су стављене на тржиште у појединачним паковањима, као што су вреће, врећице и малопродајна/појединачна паковања:

где је:
маса: у kg;
учесталост узорковања (SF): свака n-та врећа или врећица из које треба да се узме појединачни узорак (децималне бројеве треба заокружити на најближи цео број).
А.3. Узорковање производа са високим односом запремина/маса
У случају узорковања производа који имају велику запремину у односу на масу (тј. запремина (dm3)/маса (kg) > 5), захтеви у погледу масе могу се заменити еквивалентним захтевом у погледу запремине (тј. 1 kg замењује се 1 dm3).
То се не односи на производе из дела 2. одељци К) и Л) овог прилога.
2. МЕТОДЕ УЗОРКОВАЊА
А) МЕТОДА УЗОРКОВАЊА ЗА ЖИТА, СЕМЕНКЕ УЉАРИЦА, ОСИМ КИКИРИКИЈА, ПРОИЗВОДЕ ОД ЖИТА И ПРОИЗВОДЕ ОД СЕМЕНКИ УЉАРИЦА, ОСИМ ПРОИЗВОДА ОД КИКИРИКИЈА
А.1. Маса појединачног узорка
Маса појединачног узорка је око 100 g, осим ако није другачије прописано у овом одељку и осим у случају семенки уљарица и жита, за које је маса 1.000 семенки < 10 g (мале честице семенки уљарица и жита).
За мале честице семенки уљарица и жита маса појединачног узорка је око 25 g.
У случају производних партија у малопродајним/појединачним паковањима, маса појединачног узорка зависи од масе малопродајног/појединачног паковања.
У случају малопродајних/појединачних паковања > 100 g (или > од 25 g у случају малих честица семенки уљарица и жита), маса збирног узорка биће већа од потребне масе наведене у табелама 1. и 2. пододељак А.2. део 2. овог прилога. Ако је маса малопродајног/појединачног паковања много већа (тј. више него двоструко) од 100 g (или много већа од 25 g у случају малих честица семенки уљарица и жита), тада се, као појединачни узорак, узима 100 g (или 25 g у случају малих честица семенки уљарица и жита) из сваког малопродајног/појединачног паковања. То се може урадити или приликом узорковања или у лабораторији.
Међутим, у случајевима када би таква метода узорковања проузроковала неприхватљиве комерцијалне последице због оштећења производне партије (због облика паковања, транспортних средстава итд.), тада се може применити алтернативна метода узорковања.
На пример, у случајевима када се вредан производ ставља на тржиште у малопродајним/појединачним паковањима од 500 g или 1 kg, збирни узорак се може добити обједињавањем одређеног броја појединачних узорака који је мањи од броја наведеног у табелама 1. и 2. одељак А) део 2. овог прилога, под условом да маса збирног узорка буде једнака маси збирног узорка из наведених табела.
Ако је маса малопродајног/појединачног паковања < 100 g (или < 25 g у случају малих честица семенки уљарица и жита) и ако разлика није много велика (односно није мања од половине од 100 g или 25 g), једно малопродајно/појединачно паковање се сматра једним појединачним узорком, што даје збирни узорак мањи од потребне масе наведене у табелама 1. и 2. одељак А) део 2. овог прилога. Ако је маса малопродајног/појединачног паковања много мања од 100 g (или много мања од 25 g у случају малих честица семенки уљарица и жита), тада се један појединачни узорак састоји од два или више малопродајних/појединачних паковања, чија укупна маса треба да буде што ближе 100 g (или што ближе 25 g у случају малих честица семенки уљарица и жита).
А.2. Општи преглед методе узорковања за жита, семенке уљарица осим кикирикија, производе од жита и производе од семенки уљарица, осим производа од кикирикија
Табела 1.
Дељење производних партија на потпартије у зависности од производа и масе производне партије
|
Производ |
Маса производне партије (у t) |
Маса или број потпартија |
Број појединачних узорака |
Збирни узорак (у kg) |
|
Жита, семенке уљарица осим кикирикија, производи од жита и производи од семенки уљарица, осим производа од кикирикија |
> 300 и < 1500 |
3 потпартије |
100 |
10 2,5 за мале честице семенки уљарица и жита |
|
≥ 100 и ≤ 300 |
100 t |
100 |
10 2,5 за мале честице семенки уљарица и жита |
|
|
< 100 |
– |
3–100(*) |
1–10 0,25 – 2,5 за мале честице семенки уљарица и жита |
|
|
(*) У зависности од масе производне партије, како је наведено у Табели 2. овог прилога |
||||
А.3. Метода узорковања за жита, семенке уљарица осим кикирикија, производе од жита и производе од семенки уљарица, осим производа од кикирикија за производне партије ≥ 50 t
Сваку производну партију треба поделити на потпартије у складу са Табелом 1. овог прилога, под условом да потпартија може да буде физички одвојена.
Имајући у виду да маса производне партије није увек једнака збиру маса потпартија, маса потпартије може прећи наведену масу за највише 20%. У случају да се производна партија не може физички раздвојити на потпартије, из производне партије је потребно узети најмање 100 појединачних узорака.
За производне партије > 500 t, број појединачних узорака наведен је у пододељку Љ.2. одељак Љ) овог прилога.
Сваку потпартију је потребно посебно узорковати.
Број појединачних узорака је 100, а маса збирног узорка је 10 kg (или 25 kg у случају малих честица семенки уљарица и жита).
Уколико није могуће спровести методу узорковања из ове тачке због неприхватљивих комерцијалних последица услед оштећења производне партије (због облика паковања, транспортних средстава и сл.), може се применити алтернативна метода узорковања, под условом да је, колико је год то могуће, репрезентативна и да је у потпуности описана и документована.
Алтернативна метода узорковања може се такође применити и у случајевима кад је практично немогуће применити претходнонаведену методу узорковања. То је на пример случај када се велике производне партије жита складиште у складиштима (магацинима) или када се жита складиште у силосима18. Узорковање таквих производних партија се спроводи у складу са методама прописаним у одељку Љ) овог прилога.
А.4. Метода узорковања за жита, семенке уљарица осим кикирикија, производе од жита и производе од семенки уљарица, осим производа од кикирикија за производне партије < 50 t
За производне партије жита, семенки уљарица осим кикирикија, производа од жита и производа од семенки уљарица, осим производа од кикирикија < 50 t, користи се план узорковања од 10 до 100 појединачних узорака, у зависности од масе производне партије, што даје збирни узорак од 1 до 10 kg (или 0,25–2,5 kg у случају малих честица семенки уљарица и жита). За веома мале производне партије (≤ 0,5 t), узима се мањи број појединачних узорака, али тако да маса збирног узорка, који обухвата све појединачне узорке, такође буде најмање 1 kg (или 0,25 kg у случају малих честица семенки уљарица и жита). За одређивање склероција главнице ражи маса збирног узорка је најмање 1 kg.
Табела 2. примењује се за одређивање броја појединачних узорака које треба узети.
––––––––
18 Узорковање тих производних партија спроводи се у складу са правилима прописаним у одељку Љ) овог прилога. Смернице за узорковање великих серија наводе се у смерницама које су доступне на следећој веб страници: https://food.ec.europa.eu/system/files/2016-10/cs_contaminants_sampling_guidance-sampling-final_en.pdf.
Табела 2.
Број појединачних узорака које треба узети у зависности од масе производне партије жита, семенки уљарица осим кикирикија, производа од жита и производа од семенки уљарица, осим производа од кикирикија
|
Маса производне партије (у t) |
Број појединачних узорака |
Маса збирног узорка (у kg)(*) |
Маса збирног узорка (у kg)(*) за мале честице семенки уљарица и жита |
|
£ 0,05 |
3 |
1 |
0,25 |
|
> 0,05 – ≤ 0,5 |
5 |
1 |
0,25 |
|
> 0,5 – ≤ 1 |
10 |
1 |
0,25 |
|
> 1 – ≤ 3 |
20 |
2 |
0,5 |
|
> 3 – ≤ 10 |
40 |
4 |
1,0 |
|
> 10 – ≤ 20 |
60 |
6 |
1,5 |
|
> 20 – ≤ 100 |
100 |
10 |
2,5 |
|
(*) У случају контроле присуства склероција главнице ражи, маса збирног узорка је најмање 1 kg. |
|||
А.5. Узорковање у фази малопродаје
Узорковање хране у фази малопродаје спроводи се, ако је могуће, у складу сa правилима прописаним у овом одељку.
Ако то није могуће, може се применити алтернативна метода узорковања у фази малопродаје, под условом да обезбеђује да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована. У сваком случају, збирни узорак је најмање 1 kg19.
А.6. Прихватање производне партије или потпартије
Контрола склероција главице ражи
Из збирног узорка за испитивање узимају се два подузорка од најмање 0,5 kg. Испитује се један подузорак. Ако је резултат подузорка једнак или мањи од 50% (аналитички праг) прописане максималне концентрације, узорак је у складу са прописаном максималном концентрацијом. Ако је резултат већи од 50% прописане максималне концентрације, испитује се други подузорак и, за проверу усаглашености са прописаном максималном концентрацијом, користи се просек резултата двају подузорака. Примењују се следећи исходи:
производна партија или потпартија се прихвата, ако аналитички резултат испитивања за први подузорак садржи мање од 50% прописане максималне концентрације за склероције главице ражи или ако је просек двају подузорака у складу са прописаном максималном концентрацијом;
производна партија или потпартија се не прихвата, ако просек аналитичких резултата испитивања двају подузорака прелази прописану максималну концентрацију.
Контрола микотоксина
Примењују се следећи исходи:
производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу са прописаном максималном концентрацијом, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност;
производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност. То је случај када аналитички резултат (исправљен за аналитички принос, ако је применљиво) умањен за проширену мерну несигурност која произлази из анализе прелази прописану максималну концентрацију.
Б) МЕТОДА УЗОРКОВАЊА ЗА СУШЕНО ВОЋЕ И ПРОИЗВОДЕ ДОБИЈЕНЕ/ПРЕРАЂЕНЕ ОД СУШЕНОГ ВОЋА, ОСИМ СУШЕНИХ СМОКАВА
Ова метода узорковања примењује се за службену контролу нивоа микотоксина у сушеном воћу и производима добијеним/
––––––––
19 У случају да је део који треба узорковати тако мали да није могуће добити збирни узорак од 1 kg, маса збирног узорка може бити мања од 1 kg.
прерађеним од сушеног воћа, осим сушених смокава и производа добијених/прерађених од сушених смокава, за које је метода узорковања прописана у одељку В) овог прилога.
Б.1. Маса појединачног узорка
Маса појединачног узорка је око 100 g, осим ако није другачије прописано у овом одељку. У случају производних партија у малопродајним/појединачним паковањима, маса појединачног узорка зависи од масе малопродајног/појединачног паковања.
У случају малопродајних/појединачних паковања > 100 g, маса збирних узорака биће већа од потребне масе наведене у табелама 3. и 4. овог одељка. Ако је маса појединачног малопродајног паковања много већа (тј. више него двоструко) од 100 g тада се, као појединачни узорак, узима 100 g из сваког малопродајног/појединачног паковања. То се може урадити или приликом узорковања или у лабораторији.
Међутим, у случајевима када би таква метода узорковања проузроковала неприхватљиве комерцијалне последице због оштећења производне партије (због облика паковања, транспортних средстава итд.), тада се може применити алтернативна метода узорковања.
На пример, у случајевима када се вредан производ ставља на тржиште у малопродајним паковањима од 500 g или 1 kg, збирни узорак се може добити обједињавањем одређеног броја малопродајних/појединачних узорака који је мањи од броја наведеног у табелама 3. и 4. овог прилога, под условом да маса збирног узорка буде једнака маси збирног узорка наведеног у табелама 3. и 4. овог прилога.
Ако је маса малопродајног/појединачног паковања < 100 g и ако разлика није много велика (односно није мања од половине од 100 g), једно малопродајно/појединачно паковање се сматра једним појединачним узорком, што даје збирни узорак чија је маса мања од потребне масе наведене у табелама 3. и 4. овог прилога. Ако је маса малопродајног/појединачног паковања много мања од 100 g, тада се један појединачни узорак састоји од два или више малопродајних/појединачних паковања, чија је укупна маса око 100 g.
Б.2. Општи преглед методе узорковања за сушено воће и производе добијене/прерађене од сушеног воћа, осим сушених смокава
Табела 3.
Дељење производних партија на потпартије у зависности од производа и масе производне партије
|
Производ |
Маса производне партије (у t) |
Маса или број потпартија |
Број појединачних узорака |
Збирни узорак (у kg) |
|
Сушено воће, осим сушених смокава |
≥ 15 |
15–30 t |
100 |
10 |
|
< 15 |
– |
10–100 (*) |
1–10 |
|
|
(*) У зависности од масе производне партије, како је наведено у Табели 4. овог прилога. |
||||
Б.3. Метода узорковања за сушено воће и производе добијене/прерађене од сушеног воћа (производне партије ≥ 15 t), осим сушених смокава
Сваку производну партију треба поделити на потпартије у складу са Табелом 3. овог прилога, под условом да потпартија може да буде физички одвојена.
Имајући у виду да маса производне партије није увек једнака збиру маса потпартија, маса потпартије може прећи наведену масу за највише 20%.
Сваку потпартију је потребно посебно узорковати.
Број појединачних узорака је 100, а маса збирног узорка је 10 kg.
Уколико није могуће спровести методу узорковања прописану у овој тачки због комерцијалних последица услед оштећења производне партије (због облика паковања, транспортних средстава и сл), може се применити алтернативна метода узорковања, под условом да је, колико је то год могуће, репрезентативна и да је у потпуности описана и документована.
Б.4. Метода узорковања за сушено воће и производе добијене/прерађене од сушеног воћа (производне партије < 15 t), осим сушених смокава
За производне партије сушеног воћа (осим сушених смокава) < 15 t, користи се план узорковања од 10 до 100 појединачних узорака, у зависности од масе производне партије, што даје збирни узорак од 1 до 10 kg.
За одређивање броја појединачних узорака које треба узети примењује се Табела 4. овог прилога.
Табела 4.
Број појединачних узорака које треба узети у зависности од масе производне партије сушеног воћа и производе добијене/прерађене од сушеног воћа, осим сушених смокава
|
Маса производне партије (у t) |
Број појединачних узорака |
Маса збирног узорка (у kg) |
|
≤ 0,1 |
10 |
1 |
|
> 0,1 – ≤ 0,2 |
15 |
1,5 |
|
> 0,2 – ≤ 0,5 |
20 |
2 |
|
> 0,5 – ≤ 1,0 |
30 |
3 |
|
> 1,0 – ≤ 2,0 |
40 |
4 |
|
> 2,0 – ≤ 5,0 |
60 |
6 |
|
> 5,0 – ≤ 10,0 |
80 |
8 |
|
> 10,0 – ≤ 15,0 |
100 |
10 |
Б.5. Узорковање у фази малопродаје
Узорковање хране у фази малопродаје спроводи се у складу сa правилима прописаним у овом одељку.
Ако то није могуће, може се применити алтернативна метода узорковања у фази малопродаје под условом да обезбеђује да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована.
У сваком случају, збирни узорак је најмање 1 kg20.
Б.6. Посебни поступци за узорковање сушеног воћа и производа добијених/прерађених од сушеног воћа, осим сушених смокава, које се продају у вакуумским паковањима
За производне партије чија је маса ≥ 15 t узима се најмање 25 појединачних узорака који чине збирни узорак од 10 kg.
За производне партије < 15 t узима се 25% од броја појединачних узорака наведених у Табели 4. овог прилога, што чини збирни узорак чија маса одговара маси узорковане серије, како је наведено у Табели 4. овог прилога.
Б.7. Прихватање производне партије или потпартије
Примењују се следећи исходи:
производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу са прописаном максималном концентрацијом, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност;
производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност. То је случај када аналитички резултат (исправљен за аналитички принос, ако је применљиво) умањен за проширену мерну несигурност која произлази из анализе прелази прописану максималну концентрацију.
В) МЕТОДА УЗОРКОВАЊА ЗА СУШЕНЕ СМОКВЕ И ПРОИЗВОДЕ ДОБИЈЕНЕ/ПРЕРАЂЕНЕ ОД СУШЕНИХ СМОКАВА
В.1. Маса појединачног узорка
Маса појединачног узорка је око 300 g, осим ако није другачије прописано у овом одељку. У случају производних партија
––––––––
20 У случају да је део који треба узорковати тако мали да није могуће добити збирни узорак од 1 kg, маса збирног узорка може бити мања од 1 kg.
у малопродајним/појединачним паковањима, маса појединачног узорка зависи од масе малопродајног/појединачног паковања.
У случају малопродајних/појединачних паковања > 300 g, маса збирних узорака биће већа од потребне масе наведене у табелама 5, 6. и 7. овог прилога. Ако је маса малопродајног/појединачног паковања много већа (тј. више него двоструко) од 300 g, тада се, као појединачни узорак, узима 300 g из сваког малопродајног/појединачног паковања. То се може урадити или приликом узорковања или у лабораторији.
Међутим, у случајевима када би таква метода узорковања проузроковала неприхватљиве комерцијалне последице због оштећења производне партије (због облика паковања, транспортних средстава итд.), тада се може применити алтернативна метода узорковања.
На пример, у случајевима када се вредан производ ставља на тржиште у малопродајним/појединачним паковањима од 500 g или 1 kg, збирни узорак се може добити обједињавањем одређеног броја појединачних узорака који је мањи од броја наведеног у табелама 5, 6. и 7. овог прилога, под условом да маса збирног узорка буде једнака маси збирног узорка наведеног у табелама 5, 6. и 7. овог прилога.
Ако је маса малопродајног паковања < 300 g и ако разлика није много велика (тј. није мања од пововине од 300 g), једно малопродајно/појединачно паковање се сматра једним појединачним узорком, што даје збирни узорак мањи од потребне масе наведене у табелама 5, 6. и 7. овог прилога. Ако је маса малопродајног/појединачног паковања много мања од 300 g, тада се један појединачни узорак састоји од два или више малопродајних/појединачних паковања, чија је укупна маса око 300 g.
В.2. Општи преглед методе узорковања за сушене смокве
Табела 5.
Дељење производних партија на потпартије у зависности од производа и масе производне партије
|
Производ |
Маса производне партије (у t) |
Маса или број потпартија |
Број појединачних узорака |
Збирни узорак (у kg) |
|
Сушене смокве |
≥ 15 |
15–30 t |
100 |
30 |
|
< 15 |
– |
10–100(*) |
≤ 30 |
|
|
(*) У зависности од масе производне партије, како је наведено у Табели 6. овог прилога |
||||
В.3. Метода узорковања за сушене смокве
(производне партије ≥ 15 t)
Сваку производну партију треба поделити на потпартије у складу са Табелом 5. овог прилога, под условом да потпартија може да буде физички одвојена. Имајући у виду да маса производне партије није увек једнака збиру маса потпартија, маса потпартије може прећи наведену масу за највише 20%.
Сваку потпартију је потребно посебно узорковати.
Број појединачних узорака је 100.
Маса збирног узорка је 30 kg и он се пре млевења меша и дели у три једнака лабораторијска узорка од по 10 kg (ова подела на три лабораторијска узорка није потребна у случају сушених смокава намењених за даље сортирање или другу физичку обраду и ако је на располагању опрема помоћу које се може хомогенизовати узорак масе 30 kg).
Сваки лабораторијски узорак масе 10 kg посебно се ситно самеље и темељно промеша, како би се постигла потпуна хомогенизација, у складу са правилима из дела 3. овог прилога.
Уколико није могуће спровести методу узорковања прописану у овој тачки због комерцијалних последица услед оштећења производне партије (због облика паковања, транспортних средстава и сл.), може се применити алтернативна метода узорковања, под условом да је, колико је то год могуће, репрезентативна и да је у потпуности описана и документована.
В.4. Метода узорковања за сушене смокве
(производне партије < 15 t)
Број појединачних узорака које треба узети зависи од масе производне партије. Најмањи број појединачних узорака је 10, а највећи 100.
Табела 6. овог прилога примењује се за одређивање броја појединачних узорака које треба узети, као и за каснију поделу збирног узорка.
Табела 6.
Број појединачних узорака које треба узети у зависности од масе производне партије и броју подела збирног узорка
|
Маса производне партије (у t) |
Број појединачних узорака |
Маса збирног узорка (у kg) (у случају малопродајних паковања, маса збирног узорка може се разликовати – видети тачку Г.1.1.) |
Број лабораторијских узорака из збирног узорка |
|
≤ 0,1 |
10 |
3 |
1 (без поделе) |
|
> 0,1 – ≤ 0,2 |
15 |
4,5 |
1 (без поделе) |
|
> 0,2 – ≤ 0,5 |
20 |
6 |
1 (без поделе) |
|
> 0,5 – ≤ 1,0 |
30 |
9 (– < 12 kg) |
1 (без поделе) |
|
> 1,0 – ≤ 2,0 |
40 |
12 |
2 |
|
> 2,0 – ≤ 5,0 |
60 |
18 (– < 24 kg) |
2 |
|
> 5,0 – ≤ 10,0 |
80 |
24 |
3 |
|
> 10,0 – ≤ 15,0 |
100 |
30 |
3 |
Маса збирног узорка је ≤ 30 kg и он се пре млевења меша и дели на два или три једнака лабораторијска узорка по ≤ 10 kg (ова подела на два или три лабораторијска узорка није потребна у случају сушених смокава намењених за даље сортирање или другу физичку обраду и ако је на располагању опрема помоћу које се може хомогенизовати узорак масе 30 kg).
У случајевима када је маса збирног узорка мања од 30 kg, збирни узорак се дели у лабораторијске узорке у складу са следећим смерницама:
< 12 kg: без поделе на лабораторијске узорке;
≥ 12 – < 24 kg: подела на два лабораторијска узорка;
≥ 24 kg: подела на три лабораторијска узорка.
Сваки лабораторијски узорак посебно се ситно самеље и темељно промеша, како би се постигла потпуна хомогенизација, у складу са одредбама прописаним у делу 3. овог прилога.
Уколико није могуће применити методу узорковања прописану у овој тачки због комерцијалних последица услед оштећења производне партије (због облика паковања, транспортних средстава и сл.), може се применити алтернативна метода узорковања, под условом да је, колико је то год могуће, репрезентативна и да је у потпуности описана и документована.
В.5. Метода узорковања за добијене/прерађене производе и сложену храну
В.5.1. Добијени/прерађени производи са врло малом масом честица (хомогена дистрибуција контаминације микотоксином)
Производне партије пасте од смокава, у већини случајева, немају хомогену дистрибуцију контаминације микотоксинима и због тога се примењује метода узорковања и прихватање производне партије како је прописано за сушене смокве у пододељцима В.3. и В.4 овог прилога.
Број појединачних узорака је 100; а за производне партије < 50 t број појединачних узорака је од 10 до 100, у зависности од масе производне партије, како је наведено у Табели 7. овог прилога.
Табела 7.
Број појединачних узорака које треба узети у зависности од масе производне партије
|
Маса производне партије (у t) |
Број појединачних узорака |
Маса збирног узорка (у kg) |
|
≤ 1 |
10 |
1 |
|
> 1 – ≤ 3 |
20 |
2 |
|
> 3 – ≤ 10 |
40 |
4 |
|
> 10 – ≤ 20 |
60 |
6 |
|
> 20 – ≤ 50 |
100 |
10 |
Маса појединачног узорка је око 100 g. У случају производних партија у малопродајним/појединачним паковањима, маса појединачног узорка зависи од масе малопродајног/појединачног паковања.
Маса збирног узорка је 1–10 kg. Збирни узорак треба темељно промешати.
В.5.2. Остали добијени/прерађени производи са релативно великом величином честица (хетерогена дистрибуција контаминације микотоксином)
У овом случају се примењује метода узорковања и прихватљивости производне партије за сушене смокве, како је прописано у пододељцима В.3. и В.4. овог прилога.
В.6. Узорковање у фази малопродаје
Узорковање хране у фази малопродаје спроводи се, ако је могуће, у складу сa правилима прописаним у овом одељку.
Ако то није могуће, могу се применити друге ефективне методе узорковања у фази малопродаје, под условом да обезбеђују да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована.
У сваком случају, збирни узорак је најмање 1 kg21.
––––––––
21 У случају да је део који треба узорковати тако мали да није могуће добити збирни узорак од 1 kg, маса збирног узорка може бити мања од 1 kg.
В.7. Посебна метода узорковања за вакуумски упаковане сушене смокве и добијене/прерађене производе
В.7.1. Сушене смокве
За производне партије масе 15 t или више, узима се најмање 50 појединачних узорака од којих се добија збирни узорак масе 30 kg. За производне партије чија је маса < 15 t, узима се 50% од броја појединачних узорака наведених у Табели 6. овог прилога, што даје збирни узорак чија маса одговара маси узорковане производне партије, како је наведено у Табели 6. овог прилога.
В.7.2. Производи добијени/прерађени од сушених смокава са малом величином честица
За производне партије масе 50 t или више, узима се најмање 25 појединачних узорака од којих се добија збирни узорак масе 10 kg.
За производне партије чија је маса < 50 t, узима се 25% од броја појединачних узорака наведених у Табели 7. овог прилога, што даје збирни узорак чија маса одговара маси узорковане производне партије, како је наведено у Табели 7. овог прилога.
В.8. Прихватање производне партије или потпартије
Примењују се следећи исходи:
За сушене смокве:
– производна партија или потпартија се прихвата ако ниједан аналитички резултат испитивања лабораторијског узорка не прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност;
– производна партија или потпартија се не прихвата ако један или више аналитичких резултата испитивања лабораторијских узорака без сумње прелазе прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност. То је случај када аналитички резултат (исправљен за аналитички принос, ако је применљиво) умањен за проширену мерну несигурност која произлази из анализе прелази прописану максималну концентрацију.
У случајевима када је маса збирног узорка 12 kg или мањa:
– производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу сa прописаном максималнoм концентрацијoм, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност;
– производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност. То је случај када аналитички резултат (исправљен за аналитички принос, ако је применљиво) умањен за проширену мерну несигурност која произлази из анализе прелази прописану максималну концентрацију.
Г) МЕТОДА УЗОРКОВАЊА ЗА КИКИРИКИ, КОШТИЦЕ КАЈСИЈЕ, ЈЕЗГРАСТО ВОЋЕ И ОРАШАСТЕ ПЛОДОВЕ И СУШЕНЕ ЗАЧИНЕ ЧИЈЕ СУ ЧЕСТИЦЕ РЕЛАТИВНО ВЕЛИКЕ И ОД ЊИХ ДОБИЈЕНИХ/ПРЕРАЂЕНИХ ПРОИЗВОДА
Ова метода узорковања користи се за службену контролу нивоа микотоксина у кикирикију, коштицама кајсије, језграстом воћу и орашастим плодовима и сушеним зачинима чије су честице релативно велике и од њих добијених/прерађених производа.
Ова метода узорковања се примењује и на службену контролу нивоа микотоксина у зачинима чије су честице релативно велике, тј. честице чија је величина упоредива са кикирикијем или већа, нпр. као мускатни орашчић.
Г. 1. Маса појединачног узорка
Маса појединачног узорка је око 200 g, осим ако није другачије прописано у овом одељку.
У случају производних партија у малопродајним/појединачним паковањима, маса појединачног узорка зависи од масе малопродајног/појединачног паковања.
У случају малопродајних/појединачних паковања > 200 g, маса збирних узорака биће већа од потребне масе наведене у табелама 8, 9. и 10. овог прилога.
Ако је маса малопродајног/појединачног паковања много већа од 200 g, тада се, као појединачни узорак, узима 200 g из сваког малопродајног/појединачног паковања. То се може урадити или приликом узорковања или у лабораторији.
Међутим, у случајевима када би таква метода узорковања проузроковала неприхватљиве комерцијалне последице због оштећења производне партије (због облика паковања, транспортних средстава итд.), тада се може применити алтернативна метода узорковања.
На пример, у случајевима када се вредан производ ставља на тржиште у малопродајним паковањима од 500 g или 1 kg, збирни узорак се може добити обједињавањем одређеног броја појединачних узорака који је мањи од броја наведеног у табелама 8, 9. и 10. овог прилога, под условом да маса збирног узорка буде једнака маси збирног узорка наведеног у табелама 8, 9. и 10. овог прилога.
Ако је маса малопродајног/појединачног паковања мања од 200 g и ако разлика није много велика (тј. није мања од пововине од 200 g), једно малопродајно/појединачно паковање се сматра једним појединачним узорком, што даје збирни узорак мањи од потребне масе наведене табелама 8, 9. и 10. овог прилога.
Ако је маса малопродајног/појединачног паковања много < 200 g, тада се један појединачни узорак састоји од два или више малопродајних/појединачних паковања, чија je укупна маса око 200 g.
Г.2. Општи преглед методе узорковања за кикирики, коштице кајсије, језграсто воће и орашасте плодове и сушене зачине чије су честице релативно велике
Табела 8.
Дељење производних партија на потпартије у зависности од производа и масе производне партије
|
Производ |
Маса производне партије (у t) |
Маса или број потпартија |
Број појединачних узорака |
Збирни узорак (у kg) |
|
Кикирики, коштице кајсије, језграсто воће и орашасти плодови и сушени зачини чије су честице релативно велике |
≥ 500 |
100 t |
100 |
20 |
|
> 125 и < 500 |
5 подсерија |
100 |
20 |
|
|
≥ 15 и ≤ 125 |
25 t |
100 |
20 |
|
|
< 15 |
– |
10–100(*) |
≤ 20 |
|
|
(*) У зависности од масе производне партије, како је наведено у Табели 9. овог прилога |
||||
Г.3. Метода узорковања за кикирики, коштице кајсије, језграсто воће и орашасте плодове и сушене зачине чије су честице релативно велике (производне партије ≥ 15 t)
Сваку производну партију треба поделити на потпартије у складу са Табелом 8. овог прилога, под условом да потпартија може да буде физички одвојена. Имајући у виду да маса производне партије није увек једнака збиру маса потпартија, маса потпартије може прећи наведену масу за највише 20%.
Сваку потпартију је потребно посебно узорковати.
Број појединачних узорака је 100.
Маса збирног узорка је 20 kg и он се пре млевења меша и дели на два једнака лабораторијска узорка од по 10 kg (ова подела на два лабораторијска узорка није потребна у случају кикирикија, коштица кајсије, језграстог воћа и орашастих плодова и сушених зачина чије су честице релативно велике који су намењени за даље сортирање или другу физичку обраду и ако је на располагању опрема помоћу које се може хомогенизовати узорак масе 20 kg).
Сваки лабораторијски узорак масе 10 kg посебно се ситно самеље и темељно промеша, како би се постигла потпуна хомогенизација, у складу са одредбама прописаним у делу 3. овог прилога.
Уколико није могуће применити методу узорковања прописану у овој тачки због комерцијалних последица услед оштећења производне партије (због облика паковања, транспортних средстава и сл.), може се применити алтернативна метода узорковања, под условом да је, колико је то год могуће, репрезентативна и да је у потпуности описана и документована.
Г.4. Метода узорковања за кикирики, коштице кајсије, језграсто воће и орашасте плодове и сушене зачине чије су честице релативно велике (производне партије < 15t)
Број појединачних узорака које треба узети зависи од масе производне партије. Најмањи број појединачних узорака је 10 а највиши 100.
Табела 9. овог прилога се примењује за одређивање броја појединачних узорака које треба узети, као и за каснију поделу збирног узорка.
Табела 9.
Број појединачних узорака које треба узети у зависности од масе производне партије и броју подела збирног узорка
|
Маса производне партије (у t) |
Број појединачних узорака |
Маса збирног узорка (у kg) (у случају малопродајних паковања, маса збирног узорка може се разликовати – видети тачку Г.2.1.) |
Број лабораторијских узорака из збирног узорка |
|
≤ 0,1 |
10 |
2 |
1 (без поделе) |
|
> 0,1 – ≤ 0,2 |
15 |
3 |
1 (без поделе) |
|
> 0,2 – ≤ 0,5 |
20 |
4 |
1 (без поделе) |
|
> 0,5 – ≤ 1,0 |
30 |
6 |
1 (без поделе) |
|
> 1,0 – ≤ 2,0 |
40 |
8 (– < 12 kg) |
1 (без поделе) |
|
> 2,0 – ≤ 5,0 |
60 |
12 |
2 |
|
> 5,0 – ≤ 10,0 |
80 |
16 |
2 |
|
> 10,0 – ≤ 15,0 |
100 |
20 |
2 |
Маса збирног узорка је ≤ 20 kg и он се пре млевења меша и дели на два једнака лабораторијска узорка ≤ 10 kg (ова подела на два лабораторијска узорка није потребна у случају кикирикија, коштица кајсије, језграстог воћа и орашастих плодова и сушених зачина чије су честице релативно велике који су намењени за даље сортирање или другу физичку обраду и ако је на располагању опрема помоћу које се може хомогенизовати узорак масе 20 kg).
У случајевима када је маса збирног узорка < 20 kg, збирни узорак се дели у лабораторијске узорке у складу са следећим смерницама:
< 12 kg: без поделе на лабораторијске узорке;
≥ 12 kg: подела на два лабораторијска узорка.
Сваки лабораторијски узорак посебно се ситно самеље и темељно промеша, како би се постигла потпуна хомогенизација, у складу са одредбама прописаним у делу 3. овог прилога.
Уколико није могуће спровести методу узорковања прописану у овој тачки због комерцијалних последица услед оштећења производне партије (због облика паковања, транспортних средстава и сл.), може се применити алтернативна метода узорковања, под условом да је, колико је то год могуће, репрезентативна и да је у потпуности описана и документована.
Г.5. Метода узорковања за прерађене производе (осим биљних уља) и сложену храну
Г.5.1. Прерађени производи (осим биљних уља) чије су честице релативно мале, тј. брашно, кикирики путер (хомогена дистрибуција контаминације микотоксином) и сложена храна
Број појединачних узорака је 100, а за производне партије < 50 t број појединачних узорака је oд 10 до 100, у зависности од масе производне партије, као што је наведено у Табели 10. овог прилога.
Табела 10.
Број појединачних узорака које треба узети у зависности од масе производне партије
|
Маса производне партије (у t) |
Број појединачних узорака |
Маса збирног узорка (у kg) |
|
≤ 1 |
10 |
1 |
|
> 1 – ≤ 3 |
20 |
2 |
|
> 3 – ≤ 10 |
40 |
4 |
|
> 10 – ≤ 20 |
60 |
6 |
|
> 20 – ≤ 50 |
100 |
10 |
Маса појединачног узорка је око 100 g. У случају производних партија у малопродајним/појединачним паковањима, маса појединачног узорка зависи од масе малопродајног/појединачног паковања.
Маса збирног узорка је од 1 до 10 kg. Збирни узорак треба темељно промешати.
Г.5.2. Прерађени производи чије су честице релативно велике (хетерогена дистрибуција контаминације микотоксином) и сложена храна
Примењују се методе узорковања и прихватљивост производних партија или потпартија за кикирики, коштице кајсије, језграсто воће и орашасте плодове и сушене зачине чије су честице релативно велике прописане у пододељку Г. 3. и Г. 4. овог прилога.
Г.6. Узорковање у фази малопродаје
Узорковање хране у фази малопродаје спроводи се, ако је могуће, у складу сa одредбама прописаним у овом одељку.
Ако то није могуће, могу се применити друге ефективне методе узорковања у фази малопродаје, под условом да обезбеђују да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована. У сваком случају, збирни узорак је најмање 1 kg22.
Г.7. Посебна метода узорковања за кикирики, коштице кајсије, језграсто воће и орашасте плодове, сушене зачине чије су честице релативно велике и добијене/прерађене производе који се продају у вакуумским паковањима
Г.7.1. Пистаћи, кикирики, бразилски орах
За производне партије масе ≥ 15 t, узима се најмање 50 појединачних узорака од којих се добија збирни узорак масе 20 kg, а за производне партије чија је маса < 15 t, узима се 50% од броја појединачних узорака наведених у Табели 9. овог прилога, што даје збирни узорак чија маса одговара маси узорковане производне партије, као што је наведено у Табели 9. овог прилога.
Г.7.2. Коштице кајсије, језграсто воће и орашасти плодови (осим пистаћа и бразилског ораха) и сушени зачини чије су честице релативно велике
За производне партије масе ≥ 15 t узима се најмање 25 појединачних узорака од којих се добија збирни узорак масе 20 kg, а за производне партије чија је маса < 15 t, узима се 25% од броја појединачних узорака наведених у Табели 9. овог прилога, што даје збирни узорак чија маса одговара маси узорковане производне партије, као што је наведено у Табели 9. овог прилога.
––––––––
22 У случају да је део који треба узорковати тако мали да није могуће добити збирни узорак од 1 kg, маса збирног узорка може бити мања од 1 kg.
Г.7.3. Производи добијени/прерађени од кикирикија, језграстог воћа и орашастих плодова, коштица кајсије и сушених зачина чије су честице релативно велике
За производне партије масе ≥ 50 t узима се најмање 25 појединачних узорака од којих се добија збирни узорак масе 10 kg, а за производне партије чија је маса < 50 t, узима се 25% од броја појединачних узорака наведених у Табели 10. овог прилога, што даје збирни узорак чија маса одговара маси узорковане производне партије као што је наведено у Табели 10. овог прилога.
Г.8. Прихватање производне партије или потпартије
За кикирики, коштице кајсије, језграсто воће и орашасте плодове који су намењени за даље сортирање или другу физичку обраду:
– производна партија или потпартија се прихвата ако је аналитички резултат испитивања збирног узорка или просечан аналитички резултат испитивања лабораторијских узорака у складу са прописаним максималним концентрацијама, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност;
– производна партија или потпартија се не прихвата ако аналитички резултат испитивања збирног узорка или просечан аналитички резултат испитивања лабораторијских узорака без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност.
За кикирики, коштице кајсије, језграсто воће и орашасте плодове и сушене зачине чије су честице релативно велике, стављене на тржиште за крајњег потрошача или за употребу као састојка хранe:
– производна партија или потпартија се прихвата ако ниједан аналитички резултат испитивања лабораторијских узорака не прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност;
– производна партија или потпартија се не прихвата ако један или оба аналитичка резултата испитивања лабораторијских узорака без сумње прелазе прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност.
У случајевима када је маса збирног узорка 12 kg или мање:
– производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу са прописаним максималним концентрацијама, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност;
– производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност.
Д) МЕТОДА УЗОРКОВАЊА ЗА СУШЕНЕ ЗАЧИНЕ, ОСИМ СУШЕНИХ ЗАЧИНА ЧИЈЕ СУ ЧЕСТИЦЕ РЕЛАТИВНО ВЕЛИКЕ И ЗАЧИНА У ПРАХУ
Ова метода узорковања примењује се за службену контролу нивоа микотоксина у зачинима. Међутим, код сушених зачина чије су честице релативно велике тј. честице чија је величина упоредива са кикирикијем или већа, нпр. мускатни орашчић са хетерогеном дистрибуцијом контаминације микотоксином, примењује се метода узорковања прописана у одељку Г) овог прилога. За зачине у праху примењује се метода узорковања прописана у одељку Г) овог прилога.
Д.1. Маса појединачног узорка
Маса појединачног узорка је око 100 g, осим ако није другачије прописано у овом одељку. У случају производних партија у малопродајним/појединачним паковањима, маса појединачног узорка зависи од масе малопродајног/појединачног паковања.
У случају малопродајних/појединачних паковања > 100 g, маса збирних узорака биће већа од потребне масе наведене у табелама 11. и 12. овог прилога. Ако је маса малопродајног/појединачног паковања много већа од 100 g тада се, као појединачни узорак, узима 100 g из сваког малопродајног/појединачног паковања. То се може урадити или приликом узорковања или у лабораторији.
Међутим, у случајевима када би таква метода узорковања проузроковала неприхватљиве комерцијалне последице због оштећења производне партије (због облика паковања, транспортних средстава итд.), тада се може применити алтернативна метода узорковања. На пример, у случајевима када се вредан производ ставља на тржиште у малопродајним/појединачним паковањима од 500 g или 1 kg, збирни узорак се може добити обједињавањем одређеног броја појединачних узорака који је мањи од броја наведеног у табелама 11. и 12. овог прилога, под условом да маса збирног узорка буде једнака маси збирног узорка наведеног у табелама 11. и 12. овог прилога
Ако је маса малопродајног/појединачног паковања < 100 g и ако разлика није много велика (тј. није мања од половине од 100 g), једно малопродајно/појединачно паковање се сматра једним појединачним узорком, што даје збирни узорак мањи од потребне масе наведене у табелама 11. и 12. овог прилога
Ако је маса малопродајног/појединачног паковања много мања од 100 g, тада се један појединачни узорак састоји од два или више малопродајних/појединачних паковања, чија је укупна маса око 100 g.
Д.2. Општи преглед методе узорковања за сушене зачине, осим сушених зачина чије су честице релативно велике и зачина у праху
Табела 11.
Дељење производних партија на потпартије у зависности од производа и масе производне партије
|
Производ |
Маса производне партије (у t) |
Маса или број потпартија |
Број појединачних узорака |
Збирни узорак (у kg) |
|
Сушени зачини |
≥ 15 |
25 t |
100 |
10 |
|
< 15 |
– |
5–100(*) |
0,5–10 |
|
|
(*) У зависности од масе производне партије, како је наведено у Табели 12. овог прилога |
||||
Д.3. Метода узорковања за сушене зачине, осим сушених зачина чије су честице релативно велике и зачина у праху (производне партије ≥ 15 t)
Сваку производну партију треба поделити на потпартије у складу са Табелом 11. овог прилога, под условом да потпартија може да буде физички одвојена. Имајући у виду да маса производне партије није увек једнака збиру маса потпартија, маса потпартије може прећи наведену масу за највише 20%.
Сваку потпартију је потребно посебно узорковати.
Број појединачних узорака је 100, а маса збирног узорка је 10 kg.
Уколико није могуће применити методу узорковања прописану у овој тачки због комерцијалних последица услед оштећења производне партије (због облика паковања, транспортних средстава и сл.), може се применити алтернативна метода узорковања, под условом да је, колико је то год могуће, репрезентативна и да је у потпуности описана и документована.
Д.4. Метода узорковања за сушене зачине, осим сушених зачина чије су честице релативно велике и зачина у праху (производне партије < 15 t)
За производне партије зачина < 15 t, користи се план узорковања од 5 до 100 појединачних узорака, у зависности од масе производне партије, што даје збирни узорак од 0,5 до 10 kg.
Табела 12. овог прилога примењује се за одређивање броја појединачних узорака које треба узети.
Табела 12.
Број појединачних узорака које треба узети у зависности од масе производне партије зачина
|
Маса производне партије (у t) |
Број појединачних узорака |
Маса збирног узорка (у kg) |
|
≤ 0,01 |
5 |
0,5 |
|
> 0,01 – ≤ 0,1 |
10 |
1 |
|
> 0,1 – ≤ 0,2 |
15 |
1,5 |
|
> 0,2 – ≤ 0,5 |
20 |
2 |
|
> 0,5 – ≤ 1,0 |
30 |
3 |
|
> 1,0 – ≤ 2,0 |
40 |
4 |
|
> 2,0 – ≤ 5,0 |
60 |
6 |
|
> 5,0 – ≤ 10,0 |
80 |
8 |
|
> 10,0 – ≤ 15,0 |
100 |
10 |
Д.5. Узорковање у фази малопродаје
Узорковање хране у фази малопродаје спроводи се, ако је могуће, у складу сa одредбама прописаним у овом одељку.
Ако то није могуће, може се применити алтернативна метода узорковања у фази малопродаје под условом да обезбеђује да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована. У сваком случају, збирни узорак је најмање 0,5 kg23.
Д.6. Посебна метода узорковања за сушене зачине, осим сушених зачина чије су честице релативно велике и зачина у праху, који се продају у вакуумским паковањима
За производне партије чија је маса ≥ 15 t узима се најмање 25 појединачних узорака који чине 10 kg збирног узорка. За производне партије чија је маса < 15 t, узима се 25% од броја појединачних узорака наведених у Табели 12. овог прилога, што чини збирни узорак чија маса одговара маси узорковане серије у складу са Табелом 12. овог прилога.
Д.7. Прихватање производне партије или потпартије
Производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу са прописаном максималном концентрацијом, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност.
Производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за ианалитички принос и мерну несигурност. То је случај када аналитички резултат (исправљен за аналитички принос, ако је применљиво) умањен за проширену мерну несигурност која произлази из анализе прелази прописану максималну концентрацију.
Ђ) МЕТОДА УЗОРКОВАЊА ЗА МЛЕКО И МЛЕЧНЕ ПРОИЗВОДЕ, ПОЧЕТНЕ И ПРЕЛАЗНЕ ФОРМУЛЕ ЗА ОДОЈЧАД, ХРАНУ ЗА ПОСЕБЕНЕ МЕДИЦИНСКЕ НАМЕНЕ ЗА ОДОЈЧАД И МАЛУ ДЕЦУ И МЛЕКО НАМЕЊЕНО ИСХРАНИ МАЛЕ ДЕЦЕ
Ђ.1. Метода узорковања за млеко, млечне производе, почетне и прелазне формуле за одојчад, храну за посебене медицинске намене за одојчад и малу децу и млеко намењено исхрани мале деце
Маса збирног узорка је најмање 1 kg или 1 l, осим ако то није могуће, тј. када се узорак састоји од једне боце.
Најмањи број појединачних узорака које треба узети из производне партије наведен је у Табели 13. овог прилога. Конкретан број појединачних узорака зависи од уобичајеног облика у ком се одговарајући производи стављају на тржиште. У случају течних производа у расутом стању, непосредно пре узорковања производна партија се темељно меша ручно или механички, у мери у којој то не нарушава квалитет производа. У том случају, претпоставља се да је дистрибуција микотоксина унутар дате производне партије хомогена. Стога је довољно узети три појединачна узорка из производне партије како би се формирао збирни узорак.
Појединачни узорци, који често могу бити боца или паковање, треба да буду сличне масе. Маса појединачног узорка је најмање 100 g, што даје збирни узорак од најмање 1 kg или 1 l.
Одступање од поступка узимања појединачних узорака наводи се у записнику о узорковању из дела 1. одељак А) пододељак А.1 тачка А.1.8. овог прилога.
––––––––
23 У случају да је део који треба узорковати тако мали да није могуће добити збирни узорак од 0,5 kg, маса збирног узорка може бити мања од 0,5 kg.
Табела 13.
Најмањи број појединачних узорака које треба узети из производне партије
|
Облик паковања |
Запремина или маса производне партије (у l или kg) |
Најмањи број појединачних узорака које треба узети |
Најмања запремина или маса збирног узорка (у l или kg) |
|
Расуто стање |
– |
3–5 |
1 |
|
Боце/паковања |
≤ 50 |
3 |
1 |
|
Боце/паковања |
50 до 500 |
5 |
1 |
|
Боце/паковања |
> 500 |
10 |
1 |
Ђ.2. Узорковање у фази малопродаје
Узорковање хране у фази малопродаје спроводи се, ако је могуће, у складу сa одредбама прописаним у овом одељку.
Ако то није могуће, може се применити алтернативна метода узорковања у фази малопродаје под условом да обезбеђује да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована24.
Ђ.3. Прихватање производне партије или потпартије
Производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу са прописаном максималном концентрацијом, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност.
Производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност. То је случај када аналитички резултат (исправљен за аналитички принос, ако је применљиво) умањен за проширену мерну несигурност која произлази из анализе прелази прописану максималну концентрацију.
Е) МЕТОДА УЗОРКОВАЊА ЗА КАФУ, ПРОИЗВОДЕ ОД КАФЕ, КАКАО, КАКАКО ПРОИЗВОДЕ, СЛАДИЋ/СЛАТКИ КОРЕН И ПРОИЗВОДЕ ОД СЛАДИЋА/СЛАТКОГ КОРЕНА
Ова метода узорковања примењује се за службену контролу нивоа микотоксина у кафи, производима од кафе, какау, какао проиводима, сладићу/слатком корену и производа од сладића/слатког корена. Што се тиче кафе, производа од кафе, какаа и какао производа, метода узорковања предвиђена у овом одељку примењује се на чврсте (осушене) производе. За пића (течности), примењује се метода узорковања прописана у одељку Ж) овог прилога.
Е.1. Маса појединачног узорка
Маса појединачног узорка је око 100 g, осим ако није другачије прописано у овом одељку.
У случају производних партија у малопродајним/појединачним паковањима, маса појединачног узорка зависи од масе малопродајног/појединачног паковања.
У случају малопродајних/појединачних паковања > 100 g, маса збирних узорака биће већа од потребне масе наведене у табелама 14. и 15. овог прилога. Ако је маса малопродајног/појединачног паковања много већа од 100 g тада се, као појединачни узорак узима 100 g из сваког малопродајног/ појединачног паковања. То се може урадити или приликом узорковања или у лабораторији.
Међутим, у случајевима када би таква метода узорковања проузроковала неприхватљиве комерцијалне последице због оштећења производне партије (због облика паковања, транспортних средстава итд.), тада се може применити алтернативна метода узорковања. На пример, у случајевима када се вредан производ ставља на тржиште у малопродајним/појединачним паковањима од 500 g или 1 kg, збирни узорак се може добити обједињавањем одређеног броја појединачних узорака који је мањи од броја наведеног у табелама 14. и 15. овог прилога, под условом да маса збирног узорка буде једнака маси збирног узорка наведеној у табелама 14. и 15. овог прилога.
––––––––
24 У случају да је део који треба узорковати тако мали да није могуће добити збирни узорак од 1 kg, маса збирног узорка може бити мања од 1 kg.
Ако је маса малопродајног појединачног паковања < 100 g и ако разлика није много велика (тј. није мања од пововине од 100 g), једно малопродајно/појединачно паковање се сматра једним појединачним узорком, што даје збирни узорак мањи од потребне масе наведене у табелама 14. и 15. овог прилога. Ако је маса малопродајног/појединачног паковања много мања од 100 g, тада се један појединачни узорак састоји од два или више малопродајних/појединачних паковања, чија је укупна маса око 100 g.
Е.2. Општи преглед методе узорковања за кафу, производе од кафе, какао, какао производе, сладић/слатки корен и производе од сладића/слатког корена
Табела 14.
Дељење производних партија на потпартије у зависности од производа и масе производне партије
|
Производ |
Маса производне партије (у t) |
Маса или број потпартија |
Број појединачних узорака |
Збирни узорак (у kg) |
|
Кафа, производи од кафе, какао, какао производи, сладић/ слатки корен и производи од сладића/слатког корена |
≥ 15 |
15–30 t |
100 |
10 |
|
< 15 |
– |
10–100(*) |
1–10 |
|
|
(*) У зависности од масе производне партије, како је наведено у Табели 15. овог прилога |
||||
Е.3. Метода узорковања за кафу, производе од кафе, какао, какао производе, сладић/слатки корен и производе од сладића/слатког корена (производне партије ≥ 15 t)
Сваку производну партију треба поделити на потпартије у складу са Табелом 14. овог прилога, под условом да потпартија може да буде физички одвојена. Имајући у виду да маса производне партије није увек једнака збиру маса потпартија, маса потпартије може прећи наведену масу за највише 20%.
Сваку потпартију је потребно посебно узорковати.
Број појединачних узорака је 100, а маса збирног узорка је 10 kg.
Уколико није могуће спровести методу узорковања прописану у овој тачки због комерцијалних последица услед оштећења производне партије (због облика паковања, транспортних средстава и сл.), може се применити алтернативна метода узорковања, под условом да је, колико је то год могуће, репрезентативна и да је у потпуности описана и документована.
Е.4. Метода узорковања за кафу, производе од кафе, какао, какао производе, сладић/слатки корен и производе од сладића/слатког корена (производне партије < 15 t)
За производне партије кафе, производа од кафе, какао, какао производа, сладића/слатког корена и производа од сладића/слатког корена < 15 t, користи се план узорковања од 10 до 100 појединачних узорака, у зависности од масе производне партије, што даје збирни узорак од 1 до 10 kg.
Табела 15. овог прилога се примењује за одређивање броја појединачних узорака које треба узети.
Табела 15.
Број појединачних узорака које треба узети у зависности од масе производне партије кафе, производа од кафе, какакаа, какао производа, сладића/слатког корена и производа од сладића/слатког корена
|
Маса производне партије (у t) |
Број појединачних Узорака |
Маса збирног узорка (у kg) |
|
≤ 0,01 |
10 |
1 |
|
> 0,1 – ≤ 0,2 |
15 |
1,5 |
|
> 0,2 – ≤ 0,5 |
20 |
2 |
|
> 0,5 – ≤ 1,0 |
30 |
3 |
|
> 1,0 – ≤ 2,0 |
40 |
4 |
|
> 2,0 – ≤ 5,0 |
60 |
6 |
|
> 5,0 – ≤ 10,0 |
80 |
8 |
|
> 10,0 – ≤ 15,0 |
100 |
10 |
Е.5. Метода узорковања за кафу, прозводе од кафе, какао, какао производе, сладић/слатки корен и производе од сладића/слатког корена, који се продају у вакуумским паковањима
За производне партије масе ≥ 15 t узима се најмање 25 појединачних узорака који чине 10 kg збирног узорка. За производне партије масе < 15 t, узима се 25% од броја појединачних узорака наведених у Табели 15. овог прилога, што чини збирни узорак чија маса одговара маси узорковане серије као што је наведено у Табели 15. овог прилога.
Е.6. Узорковање у фази малопродаје
Узорковање хране у фази малопродаје спроводи се, ако је могуће, у складу сa одредбама прописаним у овом одељку.
Ако то није могуће, може се применити алтернативна метода узорковања у фази малопродаје, под условом да обезбеђује да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована. У сваком случају, збирни узорак је најмање 1 kg25.
Е.7. Прихватање производне партије или потпартије
Производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу са прописаном максималном концентрацијом, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност.
Производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност. То је случај када аналитички резултат (исправљен за аналитички принос, ако је применљиво) умањен за проширену мерну несигурност која произлази из анализе прелази прописану максималну концентрацију.
Ж) МЕТОДА УЗОРКОВАЊА ПИЋА
Ова метода примењује се за службену контролу нивоа микотоксина у пићима, осим у млеку.
Ж.1. Метода узорковања
Маса збирног узорка је најмање 1 l, осим ако то није могуће, тј. када се узорак састоји од једне боце или једног паковања.
Најмањи број појединачних узорака које треба узети из производне партије наведен је у Табели 16. овог прилога.
Утврђени број појединачних узорака је функција уобичајеног облика у којем се дотични производи стављају на тржиште. У случају течних производа у расутом стању, производна партија се, непосредно пре узорковања, темељно промеша, колико год је то могуће, ручно или помоћу механичких уређаја, у мери у којој то не утиче на квалитет производа. У том случају, претпоставља се да је дистрибуција микотоксина унутар дате производне партије хомогена. Стога је довољно узети три појединачна узорка из производне партије да би се формирао збирни узорак.
Појединачни узорци, који често могу бити боца или паковање, су сличне запремине. Запремина појединачног узорка је најмање 100 ml, што даје збирни узорак од најмање 1 l. Одступање од поступка узимања појединачних узорака наводи се у записнику о узорковању из дела 1. одељак А) пододељак А.1. тачка А.1.8. овог прилога.
––––––––
25 У случају да је део који треба узорковати тако мали да није могуће добити збирни узорак од 1 kg, маса збирног узорка може бити мања од 1 kg.
Табела 16.
Најмањи број појединачних узорака које треба узети из производне партије
|
Облик паковања |
Запремина производне партије (у l) |
Најмањи број појединачних узорака које треба узети |
Најмања запремина збирног узорка (у l) |
|
Пића у расутом стању |
– |
3 |
1 |
|
Боце/паковања (пића, осим вина) |
≤ 50 |
3 |
1 |
|
Боце/паковања (пића, осим вина) |
50 до 500 |
5 |
1 |
|
Боце/паковања (пића, осим вина) |
> 500 |
10 |
1 |
|
Боце/паковања вино |
≤ 50 |
1 |
1 |
|
Боце/паковања вино |
50 до 500 |
2 |
1 |
|
Боце/паковања вино |
> 500 |
3 |
1 |
Ж.2. Узорковање у фази малопродаје
Узорковање хране у фази малопродаје спроводи се, ако је могуће, у складу сa одредбама прописаним у овом одељку26.
Ако то није могуће, може се применити алтернативна метода узорковања у фази малопродаје под условом да обезбеђује да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована.
Ж.3. Прихватање производне партије или потпартије
Производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу са прописаном максималном концентрацијом, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност.
Производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност. То је случај када аналитички резултат (исправљен за аналитички принос, ако је применљиво) умањен за проширену мерну несигурност која произлази из анализе прелази прописану максималну концентрацију.
З) МЕТОДА УЗОРКОВАЊА ЗА ЧВРСТЕ ПРОИЗВОДЕ ОД ВОЋА И ПОВРЋА
Ова метода узорковања се примењује за службену контролу нивоа микотоксина у чврстим производима од воћа (осим производа од сушеног воћа за које су прописане методе у одељку Б) и В) овог прилога) и производе од поврћа, укључујући чврсте производе од воћа и поврћа за одојчад и малу децу.
З.1. Метода узорковања
Маса збирног узорка је најмање 1 kg, осим ако то није могуће, тј. када се узорак састоји од једног паковања. Најмањи број појединачних узорака које треба узети из производне партије наведен је у Табели 17. овог прилога.
Појединачни узорци су сличне масе. Маса појединачног узорка је најмање 100 g, што даје збирни узорак од најмање 1 kg.
Одступање од поступка узимања појединачних узорака наводи се у записнику о узорковању из дела 1. одељак А) пододељак А.1 тачка А.1.8. овог прилога.
––––––––
26 У случају да је део који треба узорковати тако мали да није могуће добити збирни узорак од 1 l, маса збирног узорка може бити мања од 1 l.
Табела 17.
Најмањи број појединачних узорака које треба узети из производне партије
|
Маса производне партије (у kg) |
Најмањи број појединачних узорака које треба узети |
Маса збирног узорка (у kg) |
|
< 50 |
3 |
1 |
|
50–500 |
5 |
1 |
|
> 500 |
10 |
1 |
Ако се производна партија састоји од појединачних паковања, тада је број паковања које треба узети да би се формирао збирни узорак дат у Табели 18. овог прилога.
Табела 18.
Број паковања (појединачних узорака) које треба узети да би се формирао збирни узорак, ако се производна партија састоји од појединачних паковања
|
Број паковања или јединица у производној партији |
Број паковања или јединица које треба узети |
Маса збирног узорка (у kg) |
|
1–25 |
1 паковање или јединица |
1 |
|
26–100 |
Око 5 %, најмање два паковања или јединице |
1 |
|
> 100 |
Око 10 %, највише 10 паковања или јединица |
1 |
З.2. Узорковање у фази малопродаје
Узорковање хране у фази малопродаје спроводи се, ако је могуће, у складу сa одредбама прописаним у овом одељку.
Ако то није могуће, може се применити алтернативна метода узорковања у фази малопродаје под условом да обезбеђује да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована27.
З.3. Прихватање производне партије или потпартије
Производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу са прописаном максималном концентрацијом, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност.
Производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност. То је случај када аналитички резултат (исправљен за аналитички принос, ако је применљиво) умањен за проширену мерну несигурност која произлази из анализе прелази прописану максималну концентрацију.
И) МЕТОДА УЗОРКОВАЊА ЗА ДЕЧЈУ ХРАНУ И ПРЕРАЂЕНУ ХРАНУ НА БАЗИ ЖИТА ЗА ОДОЈЧАД И МАЛУ ДЕЦУ
Ова метода узорковања примењује се за службену контролу нивоа микотоксина у дечјој храни и прерађеној храни на бази жита за одојчад и малу децу, осим у пићима на које се примењује метода узорковања прописана у одељку Ж) и осим у чврстим производима од воћа и поврћа на које се примењује метода узорковања прописана у одељку З) овог прилога.
И.1. Метода узорковања
Метода узорковања за жита и производе од жита, прописана у делу 1. одељак А) тачка А.4. овог прилога, примењује се на храну намењену за одојчад и малу децу. Стога, број појединачних узорака које треба узети зависи од масе производне партије и треба да
––––––––
27 У случају да је део који треба узорковати тако мали да није могуће добити збирни узорак од 1 kg, маса збирног узорка може бити мања од 1 kg.
буде најмање 10, а највише 100, у складу са делом 1. одељак А) пододељак А.4. Табела 2. овог прилога. Код врло малих производних партија (≤ 0,5 t), може се узети мањи број појединачних узорака, али збирни узорак који обједињује све појединачне узорке је у том случају најмање 1 kg.
Маса појединачног узорка је око 100 g. У случају производних партија у малопродајним/појединачним паковањима, маса појединачног узорка зависи од масе малопродајног/појединачног паковања, а у случају врло малих производних партија (≤ 0,5 t), појединачни узорци су такве масе да се обједињавањем појединачних узорака добије збирни узорак од најмање 1 kg. Одступање од поступка узимања појединачних узорака наводи се у записнику о узорковању из дела 1. одељак А) пододељак А.1. тачка А.3.8. овог прилога.
Збирни узорак треба да буде довољно промешан, а његова маса је од 1 до 10 kg.
И.2. Узорковање у фази малопродаје
Узорковање хране у фази малопродаје спроводи се, ако је могуће, у складу сa одредбама прописаним у овом одељку.
Ако то није могуће, може се применити алтернативна метода узорковања у фази малопродаје, под условом да обезбеђује да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована28.
И.3. Прихватање производне партије или потпартије
Производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу са прописаном максималном концентрацијом, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност.
Производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност. То је случај када аналитички резултат (исправљен за аналитички принос, ако је применљиво) умањен за проширену мерну несигурност која произлази из анализе прелази прописану максималну концентрацију.
Ј) МЕТОДА УЗОРКОВАЊА ЗА БИЉНА УЉА
Ј.1. Метода узорковања за биљна уља
Маса појединачног узорка је најмање 100 g (ml) (у зависности од природе пошиљке, нпр. ако се ради о биљном уљу у расутом стању, треба узети најмање три појединачна узорка од око 350 ml), што даје збирни узорак од најмање 1 kg (l).
Сваку производну партију треба поделити на потпартије у складу са Табелом 19. овог прилога, под условом да потпартија може да буде физички одвојена. Имајући у виду да маса производне партије није увек једнака збиру маса потпартија, маса потпартије може прећи наведену масу за највише 20%. У случају да производна партија није или не може да се физички подели на потпартије, из производне партије се узимају најмање три појединачна узорка.
Најмањи број појединачних узорака које треба узети из производне партије треба да буде у складу са Табелом 20. овог прилога.
Непосредно пре узорковања, производну партију треба што темељније промешати, ручно или помоћу механичких уређаја. У том случају, претпоставља се да је дистрибуција микотоксина унутар дотичне производне партије хомогена, па је стога за формирање збирног узорка довољно из производне партије узети три појединачна узорка.
––––––––
28 У случају да је део који треба узорковати тако мали да није могуће добити збирни узорак од 1 kg, маса збирног узорка може бити мања од 1 kg.
Табела 19.
Дељење производних партија на потпартије у зависности од производа и масе производне партије
|
Производ |
Маса производне партије (у t) |
Маса или број потпартија |
Најмањи број појединачних узорака |
Најмања маса збирног узорк (у kg) |
|
Биљна уља |
≥ 1.500 |
500 t |
3 |
1 |
|
> 300 и < 1.500 |
3 подсерије |
3 |
1 |
|
|
≥ 50 и ≤ 300 |
100 t |
3 |
1 |
|
|
< 50 |
– |
3 |
1 |
Табела 20.
Најмањи број појединачних узорака које треба узети из производне партије
|
Облик паковања |
Маса производне партије (у kg) Запремина производне партије (у l) |
Најмањи број појединачних узорака које треба узети |
|
У расутом стању(*) |
– |
3 |
|
Паковања |
≤ 50 |
3 |
|
Паковања |
> 50 до 500 |
5 |
|
Паковања |
> 500 |
10 |
|
(*) Под условом да се производна партија може физички одвојити, велике пошиљке/производне партије биљног уља у расутом стању деле се на потпартије, како је наведено у Табели 19. овог прилога. |
||
Ј.2. Метода узорковања за биљна уља у фази малопродаје
Узорковање хране у фази малопродаје спроводи се, ако је могуће, у складу сa одредбама прописаним у овом одељку.
Ако то није могуће, може се применити алтернативна метода узорковања у фази малопродаје, под условом да обезбеђује да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована. У сваком случају, збирни узорак је најмање 1 kg.
Ј.3. Прихватање производне партије или потпартије
Производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу са прописаном максималном концентрацијом, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност.
Производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност. То је случај када аналитички резултат (исправљен за аналитички принос, ако је применљиво) умањен за проширену мерну несигурност која произлази из анализе прелази прописану максималну концентрацију.
К) МЕТОДА УЗОРКОВАЊА ЗА ДОДАТАКЕ ИСХРАНИ, ПОЛЕН И ПРОИЗВОДЕ ОД ПОЛЕНА
К.1. Маса појединачног узорка и метода узорковања
Метода узорковања прописана за додатке исхрани, полен и производе од полена у облику капсула/таблета заснива се на малопродајним/појединачним паковањима која обично садрже од 30 до 120 капсула/таблета по малопродајном/појединачном паковању.
Табела 21.
|
Величина производне партије (број малопродајних/појединачних паковања) |
Број малопродајних/ појединачних паковања које треба узети за узорак |
Величина узорка (најмања количина збирног узорка) |
|
1–50 |
1 |
Додаци исхрани у облику капсула/таблета: Укупан садржај малопродајног/појединачног паковања |
|
Остали облици додатака исхрани – појединачни узорци од око 20 g или 20 ml – 100 g за додатке исхрани који садрже биљне састојке укључујући екстракте (најмање пет појединачних узорака) – 50 g или 50 ml за остале додатке исхрани (најмање три појединачна узорка) |
||
|
51–250 |
2 |
Додаци исхрани у облику капсула/таблета: Укупан садржај два малопродајна/појединачна паковања |
|
Остали облици додатака исхрани – појединачни узорци од око 20 g или 20 ml – 200 g за додатке исхрани који садрже биљне састојке укључујући екстракте (најмање 10 појединачних узорака) – 100 g или 100 ml за остале додатке исхрани (најмање пет појединачних узорака) |
||
|
251–1.000 |
4 |
Додаци исхрани у облику капсула/таблета: Половина капсула/таблета из сваког малопродајног/појединачног паковања који је узет за узорак |
|
Остали облици додатака исхрани – појединачни узорци од око 20 g или 20 ml – 200 g за додатке исхрани који садрже биљне састојке укључујући екстракте (најмање 10 појединачних узорака) – 100 g или 100 ml за остале додатке исхрани (најмање пет појединачних узорака) |
||
|
> 1.000 |
4 + 1 малопродајних/ појединачних паковања на 1.000 малопродајних/ појединачних паковања са највише 25 малопродајних/ појединачних паковања |
Додаци исхрани у облику капсула/таблета: ≤ 10 малопродајних/појединачних паковања: половина капсула из сваког малопродајног/појединачног паковања > 10 малопродајних/појединачних паковања: из сваког малопродај-ног/појединачног паковања узима се једнак број капсула/таблета да би се добио узорак са истим садржајем пет малопродајних/појединачних паковања |
|
Остали облици додатака исхрани – појединачни узорци од око 20 g или 20 ml ≤ 10 малопродајних/појединачних паковања: – 200 g за додатке исхрани који садрже биљне састојке укључујући екстракте (најмање 10 појединачних узорака) – 100 g или 100 ml за остале додатке исхрани (најмање пет појединачних узорака) > 10 малопродајних/појединачних паковања – на пет малопродајних/појединачних паковања: – 100 g за додатке исхрани који садрже биљне састојке укључујући екстракте (најмање пет појединачних узорака) – 50 g или 50 ml за остале додатке исхрани (најмање три појединачна узорка) |
||
|
Непознато (примењиво само за е-трговину) |
1 |
Додаци исхрани у облику капсула/таблета: Укупан садржај паковања |
К.2. Метода узорковања у фази малопродаје
Узорковање додатака исхрани, полена и производа од полена у фази малопродаје спроводи се, ако је могуће, у складу сa одредбама прописаним у овом одељку.
Ако то није могуће, може се применити алтернативна метода узорковања у фази малопродаје, под условом да обезбеђује да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована. У сваком случају, збирни узорак је најмање 0,05 kg.
К.3. Прихватање производне партије или потпартије
Производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу са прописаном максималном концентрацијом, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност.
Производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност. То је случај када аналитички резултат (исправљен за аналитички принос, ако је применљиво) умањен за проширену мерну несигурност која произлази из анализе прелази прописану максималну концентрацију.
Л) МЕТОДА УЗОРКОВАЊА ЗА СУШЕНО АРОМАТИЧНО БИЉЕ, БИЉНЕ ЧАЈЕВЕ (ОСУШЕНИ ПРОИЗВОД), ЧАЈЕВЕ (ОСУШЕНИ ПРОИЗВОД) И ЗАЧИНЕ У ПРАХУ
Л.1. Маса појединачног узорка
Маса појединачног узорка је око 80 g, осим ако није другачије прописано у овом одељку.
У случају производних партија у малопродајним/појединачним паковањима, маса појединачног узорка зависи од масе малопродајног/појединачног паковања.
У случају малопродајних/појединачних паковања > 80 g, маса збирних узорака биће већа од потребне масе наведене у табелама 22. и 23. овог прилога. Ако је маса малопродајног/појединачног паковања много већа од 80 g, тада се, као појединачни узорак, узима 80 g из сваког појединачног малопродајног/појединачног паковања. То се може урадити или приликом узорковања или у лабораторији.
Међутим, у случајевима када би такав начин узорковања довео до неприхватљивих комерцијалних последица услед оштећења партије (због облика паковања, транспортних средстава и сл.), онда се може применити алтернативни метод узорковања. На пример, у случају када се вредан производ продаје у малопродајним/појединачним паковањима од 500 g или 1 kg, збирни узорак се може добити агрегацијом већег броја појединачних узорака који је мањи од броја назначеног у табелама 22. и 23. овог прилога, под условом да тежина збирног узорка одговара потребној тежини збирног узорка из табела 22. и 23. овог прилога.
Када су малопродајна/појединачна паковања < 80 g и ако разлика није много велика (тј. није мања од половине од 80 g), једно малопродајно/појединачно паковање се сматра једним појединачним узорком, што даје збирни узорак мањи од потребне масе наведене у табелама 22. и 23. овог прилога. Ако је маса малопродајног/појединачног паковања много мања од 80 g, тада се један појединачни узорак састоји од два или више малопродајних/појединачних паковања, чија је укупна маса око 80 g.
Л.2. Подела производних партија на потпартије ради узорковања сушеног ароматичног биља, биљних чајева (осушени производ), чајева (осушени производ) и зачина у праху
Табела 22.
Дељење производних партија на потпартије у зависности од масе производне партије
|
Производ |
Маса производне партије (у t) |
Маса или број потпартија |
Број појединачних узорака |
Збирни узорак (у kg) |
|
Сушено ароматично биље, биљне чајеве (осушени производ), чајеве (осушени производ) и зачине у праху |
≥ 15 |
25 t |
50 |
4 |
|
< 15 |
– |
3–50(*) |
0,2–4,0 |
|
|
(*) У зависности од масе производне партије, како је наведено у Табели 23. овог прилога |
||||
Л.3. Метода узорковања за сушено ароматично биље, биљне чајеве (осушени производ), чајеве (осушени производ) и зачине у праху (производне партије ≥ 15 t)
Сваку производну партију треба поделити на потпартије у складу са Табелом 22. овог прилога, под условом да потпартија може да буде физички одвојена. Имајући у виду да маса производне партије није увек једнака збиру маса потпартија, маса потпартије може прећи наведену масу за највише 20%.
Сваку потпартију је потребно посебно узорковати.
Број појединачних узорака је 50, а маса збирног узорка је 4 kg.
Уколико није могуће применити методу узорковања прописану у овој тачки због комерцијалних последица услед оштећења производне партије (због облика паковања, транспортних средстава и сл.), може се применити алтернативна метода узорковања, под условом да је, колико је то год могуће, репрезентативна и да је у потпуности описана и документована.
Л.4. Метода узорковања за сушено ароматично биље, биљне чајеве (осушени производ), чајеве (осушени производ и зачине у праху (производне партије < 15 t)
За производне партије сушеног ароматичног биља, биљних чајева (осушени производ), чајева (осушени производ) и зачина у праху < 15 t, користи се план узорковања од 3 до 50 појединачних узорака, у зависности од масе производне партије, што даје збирни узорак од 0,2–4 kg.
Табела 23. овог прилога примењује се за одређивање броја појединачних узорака које треба узети.
Табела 23.
Најмањи број појединачних узорака које треба узети у зависности од масе производне партије сушеног ароматичног биља, биљних чајева (осушени производ), чајева (осушени производ) и зачина у праху
|
Маса производне партије (у t) |
Најмањи број појединачних узорака |
Најмања маса збирног узорка (у kg) |
|
≤ 0,1 |
3 |
0,2 |
|
> 0,1 – ≤ 0,5 |
10 |
0,8 |
|
> 0,5 – ≤ 5,0 |
25 |
2,0 |
|
> 5,0 – ≤ 10,0 |
35 |
2,8 |
|
> 10,0 – ≤ 15,0 |
50 |
4,0 |
Л.5. Метода узорковања у фази малопродаје
Узорковање хране у фази малопродаје спроводи се, ако је могуће, у складу сa одредбама прописаним у овом одељку.
Ако то није могуће, може се применити алтернативна метода узорковања у фази малопродаје, под условом да обезбеђује да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована. У сваком случају, збирни узорак је најмање 0,2 kg.
Л.6. Метода узорковања додатака исхрани који садрже сушено ароматично биље у ринфузи пре њиховог паковања у малопродајна/појединачна паковања намењена за крајњег потрошача
За узорковање додатака исхрани који садрже ароматично сушено биље у ринфузи пре њиховог паковања у малопродајна/појединачна паковања примењују се одредбе о узорковању предвиђене у овом одељку, и то на основу масе садржаја сушеног ароматичног биља у додацима исхрани у ринфузи.
Л.7. Прихватање производне партије или потпартије
Производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу са прописаном максималном концентрацијом, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност.
Производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка без сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност. То је случај када аналитички резултат (исправљен за аналитички принос, ако је применљиво) умањен за проширену мерну несигурност која произлази из анализе прелази прописану максималну концентрацију.
Љ) МЕТОДА УЗОРКОВАЊА ЗА ВРЛО ВЕЛИКЕ ПРОИЗВОДНЕ ПАРТИЈЕ ИЛИ ПАРТИЈЕ КОЈЕ СЕ СКЛАДИШТЕ ИЛИ ТРАНСПОРТУЈУ ТАКО ДА УЗОРКОВАЊЕ ЦЕЛЕ ПРОИЗВОДНЕ ПАРТИЈЕ НИЈЕ МОГУЋЕ
Љ.1. Општа правила
Ако начин транспорта или складиштења производне партије онемогућава узимање појединачних узорака у целој производној партији, пожељно је узорковање тих производних партија спроводити када је производна партија у покрету (динамичко узорковање).
У случају великих складишта намењених складиштењу хране, субјекте у пословању храном треба подстицати да у складиште уграде опрему која омогућава (аутоматско) узорковање целе ускладиштене производне партије.
Када се примењују поступци узорковања на начин прописан у овом одељку, субјекат у пословању храном или његов представник треба да буде обавештен о методи узорковања. Ако субјекат у пословању храном или његов представник доведе у питање ту методу узорковања, субјекат у пословању храном или његов представник омогућава надлежном органу спровођење узроковања у целој производној партији о свом трошку.
Узорковање дела производне партије је дозвољено под условом да узорковани део представља најмање 10% целе производне партије коју треба узорковати. Када се узоркује део производне партије хране исте категорије или истог описа и утврди се да није у складу са прописаним захтевима, сматраће се да цела производна партија није усаглашена, осим ако даља детаљна процена пружи доказ да је остатак производне партије усаглашен.
Одговарајуће одредбе о узорковању прописане у овом прилогу, као што је маса појединачног узорка, примењују се на узорковање врло великих производних партија или производних партија које се складиште или транспортују тако да узорковање целе производне партије није могуће.
Љ.2. Број појединачних узорака које треба узети у случају врло великих производних партија
Кад се узоркују велики делови (узорковани делови > 500 t), број појединачних узорака које треба узети израчунавасе на следећи начин:
Број појединачних узорака које треба узети = 100 појединачних узорака + √t.
Међутим, у случају када је маса производне партије < 1.500 t и када се она може поделити на потпартије у складу са делом 1. одељак А) пододељак А.2. Табела 1. овог прилога, уз услов да је потпартије могуће физички одвојити, број појединачних узорка који се узима прописан је у делу 1. одељак А) овог прилога.
Љ.3. Велике серије које се транспортују бродом
Љ.3.1. Динамичко узорковање великих производних партија које се транспортују бродом
Узорковање великих производних партија у бродовима по могућности се спроводи док је производ у покрету (динамичко узорковање).
Узорковање се спроводи у бродском складишту (за јединице које се могу физички одвојити). Међутим, бродска складишта се делимично празне једно за другим тако да након пребацивања у складишта више не постоји првобитно физичко одвајање. Узорковање се стога може спровести на основу почетног физичког одвајања или на основу одвајања након пребацивања у складишне објекте.
Истовар брода може трајати неколико дана. Обично се узорковање спроводи у редовним интервалима у току читавог трајања истовара. Међутим, није увек могуће или прикладно да надлежни инспектор буде присутан на узорковању у току читавог трајања истовара. Стога је дозвољено спровести узорковање дела производне партије (узорковани део). Број појединачних узорака одређује се узимајући у обзир величину узоркованог дела.
Присутво инспектора је потребно чак и када се службени узорак узима аутоматски. Међутим, ако се аутоматско узорковање спроводи на основу унапред задатих параметара које није могуће мењати у току узорковања, а појединачни узорци се сакупљају у посуду која се затвара пломбом, чиме се спречава свака могућа превара, тада је присуство инспектора потребно само на почетку узорковања, сваки пут када треба променити посуду за узорке и на крају узорковања.
Љ.3.2. Статичко узорковање производних партија које се трнспортују бродом
Ако се узорковање спроводи статичким узорковањем, примењује се иста метода која је прописана за складишне објекте (силосе) којима се приступа одозго, како је наведено у пододељку Љ.5. тачки Љ.5.1. овог одељка.
Узорковање се спроводи на приступачном делу производне партије/бродског складишта (одозго). Број појединачних узорака одређује се узимајући у обзир величину узоркованог дела.
Љ.4. Узорковање великих производних партија у складиштима
Узорковање се спроводи на приступачном делу производне партије. Број појединачних узорака одређује се узимајући у обзир величину узоркованог дела.
Љ.5. Узорковање у складишним објекатима (силоси)
Љ.5.1. Узорковање у силосима којима се (једноставно) приступа одозго
Узорковање се спроводи на приступачном делу производне партије. Број појединачних узорака одређује се узимајући у обзир величину узоркованог дела.
Љ.5.2. Узорковање у силосима којима се не приступа одозго (затворени силоси)
Љ.5.2.1. Силоси којима се не приступа одозго (затворени силоси) појединачне величине > 100 t
Храна ускладиштена у тим силосима не може се узорковати на статички начин. Стога, ако се храна у силосу мора узорковати и не постоји могућност премештања производне партије, потребно је склопити договор са субјектом у пословању храном у складу са којим је он дужан да обавести инспектора о томе када ће се силос истоварати, делимично или потпуно, да би се омогућило узорковање у тренутку када је храна у покрету.
Љ.5.2.2. Силоси којима се не приступа одозго (затворени силоси) појединачне величине < 100 t
Супротно одредбама пододељка Љ.1. овог одељка, које прописују да узорковани део представља најмање 10% целе производне партије, ова метода узорковања укључује испуштање у пријемну посуду за узорковање количине од 50 kg до 100 kg и узимање узорка из пријемне посуде за узорковање.
Величина збирног узорка одговара целој производној партији, а број појединачних узорака односи се на количину хране испуштену из силоса у пријемну посуду за узорковање.
Љ.6. Узорковање хране у расутом стању у великим затвореним контејнерима
Ове производне партије се често могу узорковати само након истовара. У одређеним случајевима, истовар није могуће обавити на месту увоза или контроле, па узорковање треба обавити при истовару контејнера. Да би инспектор могао спровести узорковање, субјекат у пословању храном обавештава инспектора о месту и времену истовара контејнера.
3. КРИТЕРИЈУМИ ЗА ПРИПРЕМУ УЗОРКА И ЗА МЕТОДЕ ИСПИТИВАЊА КОЈЕ СЕ КОРИСТЕ ЗА СЛУЖБЕНУ КОНТРОЛУ НИВОА МИКОТОКСИНА У ХРАНИ
А) УВОД
А.1. Превентивне мере
Будући да је расподела микотоксина уопштено нехомогена, узорке треба припремати изузетно пажљиво, а нарочито хомогенизовати.
Ако хомогенизацију спроводи лабораторија, хомогенизује се цео узорак који је лабораторија примила.
Код испитивања афлатоксина треба, колико год је то могуће, избегавати дневно светло у току поступка, јер се афлатоксини поступно разграђују под утицајем ултраљубичастог светла.
А.2. Израчунaвање односа љуска/језгро целих плодова језграстог воћа и орашастих плодова (кикирики и остали)
Прописане максималне концентрације примењују се на јестиви део.
Нивои микотоксина у јестивом делу утврђују се:
– уклањањем љуске са целих узоркованих плодова језграстог воћа и орашастих плодова и утврђивањем нивоа микотоксина у јестивом делу;
– узимањем целих плодова језграстог воћа и орашастих плодова (са љуском) применом поступка припреме узорка. Методом узорковања и испитивања процењује се маса јестивог дела плода у збирном узорку. Маса јестивог дела плода у збирном узорку процењује се након одређивања одговарајућег фактора који узима у обзир однос љуске и јестивог дела у целом плоду језграстог воћа и орашастих плодова. Овај однос се користи за утврђивање количине јестивог дела у збирном узорку који је узет у припреми узорка и методи испитивања узорка.
Око 100 целих плодова језграстог воћа и орашастих плодова/уљарица узима се насумичним одабиром из производне партије или се издваја из сваког збирног узорка. За сваки лабораторијски узорак однос се може добити мерењем масе целих плодова, уклањањем љуске и поновним мерењем масе љуски и јестивог дела.
Однос између љуске и јестивог дела, који лабораторија утврди на основу одређеног броја узорака, може се узети у обзир у даљем аналитичком раду. Међутим, ако се утврди да одређени лабораторијски узорак прелази прописане максималне концентрације, однос за тај узорак одређује се коришћењем око 100 плодова језграстог воћа и орашастих плодова/уљарица који су издвојени.
Б) ОБРАДА УЗОРКА ПРИМЉЕНОГ У ЛАБОРАТОРИЈИ
Сваки лабораторијски узорак се темељно промеша користећи поступак који укључује, ако је потребно, фино млевење и за који је доказано да се њиме постиже потпуна хомогенизација, осим узорака за контролу присуства ергот склероција.У случају да се лабораторијски узорак мора анализирати ради контроле присуства ергот склероција и микотоксина, део узорка који се користи за одређивање ергот склероција се узима из лабораторијског узорка пре млевења лабораторијског узорка.
У случају да се прописана максимална концентрација односи на суву материју, садржај суве материје у производу утврђује се на делу хомогенизованог узорка, користећи методу за коју је доказано да се њоме прецизно утврђује садржај суве материје.
В) ПОНОВЉЕНИ УЗОРЦИ
Поновљени узорци за сврхе службене контроле, додатна стручна мишљења (жалбе) и судске поступке узимају се из хомогенизованог збирног узорка.
Г) МЕТОДА ИСПИТИВАЊА КОЈУ ЛАБОРАТОРИЈА КОРИСТИ И ЗАХТЕВИ У ПОГЛЕДУ ЛАБОРАТОРИЈСКЕ КОНТРОЛЕ
Г.1. Општи захтеви
Потврдне методе испитивања које се користе у сврхе контроле хране треба да буду у складу са посебним прописом којим се уређује службена контрола хране.
Г.2. Посебни захтеви који се примењују до 1. јануара 2029. године на методе које су валидиране пре ступања на снагу овог правилника
Г.2.1. Посебни захтеви за потврдние методе
Г.2.1.1. Критеријум изводљивости
Препоручује се примена потпуно валидираних потврдних метода, према потреби и доступности (тј. метода које су валидиране међулабораторијским испитивањем релевантних матрикса). Уколико не постоје специфичне методе за одређивање микотоксина, лабораторије могу користити и друге одговарајуће валидиране потврдне методе (нпр. методе које су валидиране у лабораторији на релевантним матриксима из групе производа који се разматрају), под условом да те методе испуњавају критеријуме изводљивости прописане у табелама 24–31. овог прилога.
Ако је могуће, потврђивање документованих метода укључује сертификовани референтни материјал.
Табела 24.
Критеријум изводљивости за афлатоксине
|
Критеријум |
Распон концентрације |
Препоручена вредност |
Максимално дозвољена вредност |
|
Слепа проба |
Све |
Занемарљиво |
- |
|
Аналитички принос – афлатоксин М1 |
0,01 – 0,05 μg/kg |
60–120% |
|
|
> 0,05 μg/kg |
70–110% |
||
|
Аналитички принос– афлатоксини В1, В2, G1, G2 |
< 1,0 μg/kg |
50–120% |
|
|
1 – 10 μg/kg |
70–110% |
||
|
> 10 μg/kg |
80–110% |
||
|
Репродуктивност RSDR |
Све |
Вредност добијена уз помоћ Horwitz – ове једначине (*)(**) |
2 × вредност добијена уз помоћ Horwitz – ове једначине (*)(**) |
|
Поновљивост RSDr може се израчунати као 0,66 пута репродуктивност RSDR при концентрацији која се разматра |
|||
|
Напомена: Вредности које се примењују на афлатоксин В1 и на збир афлатоксина В1 + В2 + G1 + G2. Ако треба да се изрази збир појединачних афлатоксина В1 + В2 + G1 + G2, тада одговор сваког од афлатоксина на аналитички систем треба да буде или познат или еквивалентан. |
|||
Табела 25.
Критеријум изводљивости за охратоксин А
|
Ниво у μg/kg |
Охратоксин А |
||
|
RSDr у % |
RSDR у % |
Аналитички принос у % |
|
|
< 1 |
≤ 40 |
≤ 60 |
50–120 |
|
≥ 1 |
≤ 20 |
≤ 30 |
70–110 |
Табела 26.
Критеријум изводљивости за патулин
|
Ниво у μg/kg |
Патулин |
||
|
RSDr у % |
RSDR у % |
Аналитички принос у % |
|
|
< 20 |
≤ 30 |
≤ 40 |
50–120 |
|
20 – 50 |
≤ 20 |
≤ 30 |
70–105 |
|
> 50 |
≤ 15 |
≤ 25 |
75–105 |
Табела 27.
Критеријум изводљивости за деоксиниваленол
|
Ниво у μg/kg |
Деоксиниваленол |
||
|
RSDr у % |
RSDR у % |
Аналитички принос у % |
|
|
> 100 – ≤ 500 |
≤ 20 |
≤ 40 |
60–110 |
|
> 500 |
≤ 20 |
≤ 40 |
70–120 |
Табела 28.
Критеријум изводљивости за зеараленон
|
Ниво у μg/kg |
Зеараленон |
||
|
RSDr у % |
RSDR у % |
Аналитички принос у % |
|
|
≤ 50 |
≤ 40 |
≤ 50 |
60–120 |
|
> 50 |
≤ 25 |
≤ 40 |
70–120 |
Табела 29.
Критеријум изводљивости за фумонизин В1 и В2 појединачно
|
Ниво у μg/kg |
Фумонизин В1 и В2 појединачно |
||
|
RSDr у % |
RSDR у % |
Аналитички принос у % |
|
|
≤ 500 |
≤ 30 |
≤ 60 |
60–120 |
|
> 500 |
≤ 20 |
≤ 30 |
70–110 |
Табела 30.
Критеријум изводљивости за Т-2 и НТ-2 токсин појединачно
|
Ниво у μg/kg |
Т-2 и НТ-2 токсин појединачно |
||
|
RSDr у % |
RSDR у % |
Аналитички принос у % |
|
|
15 – 250 |
≤ 30 |
≤ 50 |
60–130 |
|
> 250 |
≤ 25 |
≤ 40 |
60–130 |
Табела 31.
Критеријум изводљивости за цитринин
|
Ниво у μg/kg |
Цитринин |
|||
|
RSDr у % |
RSDr у % |
RSDR у % |
Аналитички принос у % |
|
|
Све |
0,66 × RSDR |
Добијена уз помоћ Horwitz – ове једначине (*)(**) |
2 × вредност добијена уз помоћ Horwitz – ове једначине (*)(**) |
70–120 |
Напомене уз критеријум изводљивости за микотоксине:
Границе детекције коришћених метода нису наведене јер су вредности прецизности дате код концентрације која се разматра.
Вредности прецизности рачунају се из Horwitz-ове једначине, а посебно из оригиналне Horwitz-ове једначине (за концентрације 1,2 × 10–7 ≤ С ≤ 0,138)(*) и из модификоване Horwitz-ове једначине (за концентрације С < 1,2 × 10–7)(**):
(*) Horwitz-ова једначина за концентрације 1,2 × 10–7 ≤ С ≤ 0,138:
RSDR = 2>(1-0,5 logС)29
(**) Модификована Horwitz-ова једначина (*) за концентрације
С < 1,2 × 10–7: RSDR = 22%30,
при чему је:
RSDR релативна стандардна девијација израчуната из резултата добијених уз услове обновљивости [(sR / х¯) × 100];
С однос концентрације (тј. 1 = 100 g/100g, 0,001 = 1 000 mg/kg).
Ово је генерализована једначина прецизности која се показала независном од аналита и матрикса и, за већину рутинских метода испитивања, искључиво зависи од концентрације.
Г.2.1.2. Приступ „погодност за сврху”
За методе које су потврђене у лабораторији може се, као алтернатива, употребљавати приступ „погодност за сврху”31, како би се оценила њихова погодност за употребу у току службене контроле. Методе погодне за службену контролу дају резултате са стандардном мерном несигурношћу (u) која је мања од максималне стандардне мерне несигурности израчунате применом следеће формуле:
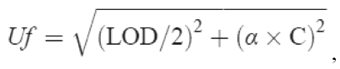
при чему је:
Uf – максимална стандардна мерна несигурност (μg/kg);
LOD – граница детекције методе (μg/kg);
––––––––
29 Извор: W. Horwitz, L.R. Kamps, K.W. Boyer, J.Assoc.Off.Analy.Chem.,1980., 63., 1344.
30 Извор: M. Thompson, Analyst, 2000, 125, р. 385–386.
31 Извор: M. Thompson and R. Wood, Accred. Qual. Assur., 2006, 10, p. 471–478.
α – константа, бројчани фактор који се користи у зависности од вредности С. Вредности које треба користити наведене су у табели 32. овог прилога;
С – концентрација која се разматра (μg/kg).
Ако метода испитивања даје резултате са мерном несигурношћу мањом од максималне стандардне несигурности, метода се сматра једнако погодном као и она која задовољава критеријуме изводљивости из подтачке Г.2.1.1. овог прилога.
Табела 32.
Вредности α у зависности од концентрације која се разматра
|
С ( у μg/kg) |
α |
|
≤ 50 |
0,2 |
|
51–500 |
0,18 |
|
501–1.000 |
0,15 |
|
1.000–10.000 |
0,12 |
|
> 10.000 |
0,1 |
Г.2.2. Посебни захтеви за семи-квантитативне методе скрининга
Г.2.2.1. Област примене
Област примене обухвата биоаналитичке методе које се заснивају на имунолошком препознавању или везивању на рецепторе (као што су ЕLISА, биохемијске траке за тестирање – dip-sticks, имунохроматографски тестови – lateral flow и имуносензори) и физичко-хемијске методе које се заснивају на хроматографији или на директној детекцији уз помоћ масене спектрометрије (нпр. масена спектрометрија у амбијенталном окружењу).
Друге методе, као што је танкослојна хроматографија, се не искључују, уз услов да су добијени сигнали директно повезани са микотоксинима који се разматрају и омогућавају примену принципа описаног у наставку.
Посебни захтеви се примењују нa методе за које је резултат мерења нумеричка вредност, на пример (релативни) одговор добијен уз помоћ читача биохемијске траке за тестирање, сигнал из везаног система течне хроматографије – масене спектрометрије (LC-MS) итд., као и да се примењују уобичајени статистички подаци.
Захтеви се не примењују нa методе којима се не добија нумеричка вредност, као нпр. када је реч само о линији која је присутна или није присутна. За те методе захтеви су прописани у подтачки Г.2.3. овог одељка.
Овај део прилога описује поступке за валидацију метода скрининга путем међулабораторијске валидације, верификацију изводљивости методе која је валидирана у оквиру међулабораторијског теста, као и валидацију методе скрининга у једној лабораторији.
Г.2.2.2. Дефиниције
Поједини изрази употребљени у овом прилогу имају следеће значење:
1) Циљна концентрација скрининга (screening target concentration – STC) јесте релевантна концентрација за детекцију микотоксина у узорку. Када је сврха испитивање уклађености са прописаним максималним концентрацијама, STC је једнака применљивој максималној концентрацији. За остале потребе или када није прописана максимална концентрација, STC је унапред одређена од стране лабораторије.
2) Метода скрининга јесте метода која се користи за избор оних узорака чије концентрације микотоксина са одређеном сигурношћу премашују STC. За потребе скрининга микотоксина, постојање 95% сигурности сматра се погодним за сврху, а резултат скрининга изражава се као „негативан” или „сумњив”. Методе скрининга омогућавају економично испитивање великог броја узорака чиме се повећава могућност откривања нових случајева високе изложености и ризика за здравље потрошача. Ове методе се заснивају на биоаналитичким методама, LC-MS или HPLC методама (течна хроматографија високих перформанси или течна хроматографија – масена спектрометрија). Резултати узорака који премашују граничну вредност се проверавају и, у ту сврху, оригинални узорак се подвргава потпуно новом испитивању које се спроводи потврдном методом.
3) Негативан узорак јесте узорак чији је садржај микотоксина у узорку < STC са сигурношћу од 95% (тј. постоји 5% могућности да су узорци нетачно приказани као негативни).
4) Лажно негативан узорак јесте узорак чији је садржај микотоксина > STC, али је идентификован као негативан.
5) Сумњив узорак (оријентационо позитиван) јесте узорак који премашује граничну вредност и може да садржи количине микотоксина веће од STC.
6) Лажно сумњив узорак јесте негативни узорак који је идентификован као сумњи
7) Потврдне методе јесу методе које пружају потпуне или додатне информације које омогућавају да се микотоксин недвосмислено идентификује и квантификује на нивоу значајности.
8) Граничнa вредност јесте одговор, сигнал или концентрација добијена методом скрининга, изнад које је узорак класификован као „сумњив”. Гранична вредност се одређује током валидације и узима у обзир варијабилност мерења.
9) Негативан контролни узорак (слепа проба матрикса) јесте узорак за који се зна да у њему нема микотоксина који се проверава, претходним одређивањем користећи потврдну методу довољне осетљивости или другом методом, или ако се такав узорак не може добити, материјал сa најнижим могућим нивоом, ако се на основу тог нивоа може закључити да је метода скрининга погодна за ту сврху.
10) Узорак за који је познато да је слободан јесте узорак који садржи количину аналита која није већа од једне петине STC. Ако се ниво може квантификовати потврдном методом, ниво треба узети у обзир за процену валидације.
11) Позитиван контролни узорак јесте узорак који садржи микотоксин у циљној концентрацији скрининга, нпр. сертификовани референтни материјал, материјал познатог садржаја (нпр. материјал за испитивање из тестова оспособљености) или материјал које је на другачији начин довољно окарактерисан уз помоћ потврдне методе. Ако не постоји ниједна од претходно наведених могућности, може се користити мешавина узорака са различитим нивоима контаминације или обогаћени узорак припремљен у лабораторији и који је довољно окарактерисан, под условом да се докаже да је ниво контаминације проверен.
Г.2.2.3. Поступак валидације
Циљ валидације је доказивање погодности примене методе скрининга. То се постиже одређивањем граничне вредности и одређивањем односа лажно негативних и лажно сумњивих резултата. У ова два параметра уграђене су карактеристике изводљивости као што су осетљивост, селективност и прецизност.
Методе скрининга могу бити валидиране међулабораторијском валидацијом или валидацијом у једној лабораторији. Ако су подаци из међулабораторијске валидације методе већ доступни за одређену комбинацију микотоксин/матрикс/STC, довољна је верификација изводљивости методе у лабораторији која примењује методу.
Г.2.2.3.1. Почетна валидација уз помоћ валидације у једној лабораторији
Микотоксини:
Валидација се спроводи за сваки појединачни микотоксин из обима примене. У случају биоаналитичких метода којима се добија комбинвани одговор за одређену групу микотоксина (нпр. афлатоксини B1, B2, G1 и G2, фумонизини B1 и B2 ), доказује се применљивост, па се у обиму примене методе наводе ограничења у погледу испитивања.
Не сматра се да се нежељеном унакрсном реактивношћу (нпр. DON-3-глукозид, 3– или 15-ацетил-DON у имунолошким методама испитивања DON-а) повећава проценат лажно негативних резултата циљних микотоксина, али може доћи до повећања процента лажно сумњивих резултата. Нежељено повећање опада спровођењем потврдног испитивања ради недвосмисленe идентификације и квантификације микотоксина.
Матрикси:
Почетну валидацију треба спровести за сваки производ, односно, ако је познато да се метода може применити на више производа, за сваку групу производа. У другом случају, из одговарајуће групе се бира један репрезентативан и релевантан производ како је наведено у Табели 33. овог прилога.
Скуп узорака:
Минималан број различитих узорака потребних за валидацију је 20 хомогених негативних контролних узорака и 20 хомогених позитивних контролних узорака који садрже микотоксин у циљној концентрацији скрининга (STC), испитивани под условима средње прецизности (RSDRi), распоређени током пет различитих дана. По избору, додатни сетови од 20 узорака који садрже микотоксин на другим нивоима могу да се додају скупу за валидацију како би се стекао увид у то у којој мери метода може да разликује различите концентрације микотоксина.
Концентрација:
За сваку циљну концентрацију скрининга (STC), која се користи у рутинској примени, спроводи се валидација.
Г.2.2.3.2. Почетна валидација путем међулабораторијског испитивања
Валидација међулабораторијским испитивањем спроводи се у складу са међународно признатим протоколом о међулабораторијским испитивањима (нпр. SRPS ISO 5725: 2007 или IUPAC – Међународни усклађени протокол) на основу кога се захтева укључивање валидних података из најмање осам различитих лабораторија. Осим тога, једина разлика у односу на валидацију у једној лабораторији је та што 20 или више узорака по производу/нивоу може бити равномерно подељено међу лабораторијима које учествују, са најмање два узорка по лабораторији.
Г.2.2.4. Одређивање граничног нивоа и процента лажно сумњивих резултата слепих узорака
Као основа за израчунавање тражених параметара узимају се (релативни) одговори у случају негативних и позитивних контролних узорака.
Методе скрининга код којих је одговор пропорционалан концентрацији микотоксина
На методе скрининга код којих је одговор пропорционалан концентрацији микотоксина, примењује се следеће:
Гранична вредност = RSTC – t-вредност0,05 x SDSTC,
где је:
RSTC средњи одговор позитивних контролних узорака (при циљној концентрацији скрининга (STC));
t-вредност једносмерна t-вредност за проценат лажно негативних резултата од 5%, како је наведено у Табели 34. овог прилога;
SDSTC стандардна девијација.
Методе скрининга код којих је одговор обрнуто пропорционалан концентрацији микотоксина
Слично томе, на методе скрининга код којих је одговор обрнуто пропорционалан концентрацији микотоксина гранична вредност се одређује као:
Гранична вредност = RSTC + t-вредност0,05 x SDSTC.
Користећи ову специфичну t-вредност за утврђивање граничне вредности, задата вредност процента лажно негативних резултата је подразумевано постављена на 5 %.
Оцена погодности за сврху32
Резултати добијени на основу негативних контролних узорака користе се за процену одговарајућег процента лажно сумњивих резултата, а t-вредност се израчунава у случају када је резултат
––––––––
32 Овај концепт је детаљно описан уз навођење примера у часопису Аналитичка и биоаналитичка хемија (Analytical and Bioanalytical Chemistry DOI 10.1007/s00216 -013– 6922-1).
негативног контролног узорка већи од граничне вредности, па је погрешно класификован као сумњив.
За методе скрининга код којих је одговор пропорционалан концентрацији микотоксина t-вредност је:

За методе скрининга код којих је одговор обрнуто пропорционалан концентрацији микотоксина t-вредност је:

Из добијене t-вредности на основу степена слободе који су израчунати из бројних експеримената, може се израчунати могућност појаве лажно сумњивих узорака за једнострану дистрибуцију (нпр. функција прошириве табеле „TDIST”) или узети из табеле за t-дистрибуцију.
Одговарајућом вредношћу једностране t-дистрибуције одређује се проценат лажно сумњивих резултата.
Овај концепт је детаљно описан на примеру у Аналитичкој и биоаналитичкој хемији DOI 10.1007/s00216 -013-6922-1.
Г.2.2.5. Проширење области примене методе
Г.2.2.5.1. Проширење области примене на друге микотоксине
Када се области примене постојеће методе скрининга додају нови микотоксини, нужно је спровести потпуну валидацију ради доказивања погодности методе.
Г.2.2.5.2. Проширење области примене на друге производе
Ако је познато или се очекује да ће метода скрининга бити применљива на друге производе, проверава се поузданост њене примене на те друге производе. Све док нови производ припада групи производа, као што је наведено у Табели 33. овог прилога, за коју је већ спроведена почетна валидација, довољно је спровести додатну ограничену валидацију. Да би се то учинило, анализира се најмање 10 хомогених негативних и 10 хомогених позитивних контролних узорака (при циљној концентрацији скрининга – STC), уз услове средње прецизности. Позитивни су контролни узорци изнад граничне вредности. У случају да овај критеријум није испуњен, потребна је потпуна валидација.
Г.2.2.6. Провера метода које су већ валидиране међулабораторијским испитивањима
За методе скрининга које су већ успешно валидиране међулабораторијским испитивањима проверава се њихова изводљивост. Да би се то учинило, анализира се најмање шест негативних контролних и шест позитивних контролних узорака (при циљној концентрацији скрининга – STC).
Позитивни су контролни узорци изнад граничне вредности. У случају да овај критеријум није испуњен, лабораторија спроводи анализу основног узрока како би утврдила зашто не може да понови резултат добијен у међулабораторијском испитивању. Тек након предузимања потребних корективних мера, лабораторија интерно поновно проверава изводљивост методе. У случају да лабораторија није у могућности да верификује резултате међулабораторијског испитивања, она одређује сопствену граничну вредност спроводећи потпуну валидацију у једној лабораторији.
Г.2.2.7. Стална провера методе / непрекидна валидација методе
Након почетне валидације, додатни подаци за валидацију се добијају укључивањем најмање два позитивна контролна узорка у сваку групу прегледаних узорака. Један позитивни контролни узорак је познат узорак (нпр. један који је коришћен током почетне валидације), други је од различитог производа из исте групе производа (у случају кад се испитује само један производ, употребљава се други узорак тог производа). Укључивање негативног контролног узорка није обавезно. Резултати добијени за два позитивна контролна узорка додају се постојећем скупу за валидацију.
Најмање једном годишње поново се утврђује гранична вредност и поново оцењује поузданост методе. Стална провера методе има неколико сврха, укључујући:
– контролу квалитета серије узорака која се проверава;
– пружање информација о робусности методе под условима у лабораторији која примењује методу;
– оправданост применљивости методе на различите производе;
– омогућавање прилагођавања граничних вредности у случају поступних одступања током времена.
Г.2.2.8. Извештај о валидацији
Извештај о валидацији садржи:
– изјаву о циљној концентрацији скрининга (STC);
– изјаву о добијеној граничној вредности,
Напомена: Гранична вредност има једнак број значајних цифара као и STC.
Нумеричке вредности које се користе за израчунавање граничне вредности имају најмање једну значајну цифру више од STC;
– изјаву о израчунатом проценту лажно сумњивих резултата;
– изјаву о начину добијања процента лажно сумњивих резултата,
Напомена: Изјава о израчунатом проценту лажно сумњивих резултата показује да ли је метода погодна за сврху, с обзиром на то да указује на број слепих узорака (или контаминацију ниског нивоа) који подлежу провери.
Табела 33.
Групе производа за валидацију метода скрининга
|
Групе производа |
Категорије производа |
Типични репрезентативни производи обухваћени категоријом |
||
|
Високи садржај воде |
Воћни сокови |
Сок од јабуке, сок од грожђа |
||
|
Алкохолна пића |
Вино, пиво, сајдер |
|||
|
Коренасто и кртоласто поврће |
Свежи ђумбир |
|||
|
Пире на бази жита или воћа |
Пире за одојчад и малу децу |
|||
|
Високи садржај масти |
Језграсто воћа и орашасти плодови |
Орах, лешник, кестен |
||
|
Семенке уљарица и њихови производи |
Уљана репица, сунцокрет, семе памука, соја, кикирики, сусам итд. |
|||
|
Плодови уљарица и њихови производи |
Уља и пасте (нпр. маслац од кикирикија, тахини) |
|||
|
Висок садржај скроба и/или протеина и низак садржај воде и масти |
Зрна житарица и њихови производи |
Пшеница, раж, јечам, кукуруз, пиринача, овас Интегрални хлеб, хлеб од белог брашна, крекери, жита за доручак, тестенина |
||
|
Дијететски производи |
Суви прашкови за припрему хране за одојчад и малу децу |
|||
|
Висок садржај киселине и висок садржај воде(*) |
Производи од цитруса / цитрусног воћа / агрума |
|||
|
„Компликовани или јединствени производи”(**) |
Какао и његови производи, копра и њени производи, кафа, чај Зачини, сладић / госпино биље / слатки корен |
|||
|
Висок садржај шећера, низак садржај воде |
Сушено воће |
Смокве, грожђице (од белог грожђа, од белог грожђа без семенки, од црног грожђа без семенки) |
||
|
Млеко и млечни производи |
Млеко |
Кравље, козије и бивоље млеко |
||
|
Сир |
Крављи и козији сир |
|||
|
Млечни производи (нпр. млеко у праху) |
Јогурт, павлака |
|||
|
(*) Ако се у току екстракције за стабилизацију рН промена употребљава пуферски раствор, тада се та група производа може спојити у једну групу производа „Висок садржај воде”. (**) „Компликоване или јединствене производи” треба потпуно валидирати само ако се често испитују. Ако се испитују само повремено, валидација се може свести на проверу нивоа извештивања коришћењем обогаћених екстраката слепе пробе. |
||||
Табела 34.
Једнострана t-вредност за лажно негативну стопу од 5%
|
Степен слободе |
Број понављања |
t-вредност (5%) |
|
10 |
11 |
1,812 |
|
11 |
12 |
1,796 |
|
12 |
13 |
1,782 |
|
13 |
14 |
1,771 |
|
14 |
15 |
1,761 |
|
15 |
16 |
1,753 |
|
16 |
17 |
1,746 |
|
17 |
18 |
1,74 |
|
18 |
19 |
1,734 |
|
19 |
20 |
1,729 |
|
20 |
21 |
1,725 |
|
21 |
22 |
1,721 |
|
22 |
23 |
1,717 |
|
23 |
24 |
1,714 |
|
24 |
25 |
1,711 |
|
25 |
26 |
1,708 |
|
26 |
27 |
1,706 |
|
27 |
28 |
1,703 |
|
28 |
29 |
1,701 |
|
29 |
30 |
1,699 |
|
30 |
31 |
1,697 |
|
40 |
41 |
1,684 |
|
60 |
61 |
1,671 |
|
120 |
121 |
1,658 |
|
∞ |
∞ |
1,645 |
Г.2.А. Посебни захтеви који се примењују од 1. јануара 2029. године на методе које су валидиране после ступања на снагу овог правилника
Г.2.А.1. Посебни захтеви за потврдне методе
Г.2.А.1.1. Критеријуми изводљивости
За потврдне методе важе следећи критеријуми изводљивости:
Аналитички принос: просечан аналитички принос је између 70 и 120%.
Просечан аналитички принос је просечна вредност из поновљених узорака добијен током валидације приликом одређивања параметара прецизности RSDr и RSDwR. Критеријум се односи на све концентрације и све појединачне токсине, са изузетком ергот алкалоида.
За ергот алкалоиде критеријум се односи на збир сваког пара епимера.
У изузетним случајевима, просечни аналитички приноси ван горњег опсега могу бити прихватљиви, али ће бити у границама од 50–130%, и то само када су испуњени критеријуми прецизности за RSDr и RSDwR.
Прецизност:
RSDr је ≤ 20%
RSDwR је ≤ 20%
RSDR је ≤ 25%
Ови критеријуми важе за све концентрације.
У случају да лабораторија пружи доказ да је критеријум RSDwR испоштован, нема потребе да се обезбеди тај доказ за RSDr критеријум, јер усклађеност са RSDwR гарантује усклађеност са RSDr критеријумом.
У случају да се прописана максимална концентрација примењује на збир токсина, онда се критеријуми прецизности примењују и на збир и на појединачне токсине. За ергот алкалоиде, критеријуми за појединачне токсине се примењују на збир сваког пара епимера.
Граница квантификације
Када је у Табели 35. овог прилога утврђен посебан захтев у погледу LOQ за микотоксин, за методу се примењује LOQ једднак или нижи од те вредности.
Табела 35.
LOQ захтеви за одређене микотоксине
|
Микотоксин |
Храна |
LOQ захтев (μg/kg) |
|
Афлатоксини |
||
|
Афлатоксин В1 |
Дечија храна и прерађена храна на бази жита за одојчад и малу децу и храна за посебне медицинске потребе намењена за одојчад и малу децу |
≤ 0,1 |
|
Афлатоксин В1, В2, G1, G2, сваки од афлатоксина |
Сва остала храна |
≤ 1 |
|
Охратоксин А |
≤ 10,0 |
|
|
Какао прах |
≤ 3,0 |
|
|
Ергот алкалоиди (сваки од 12 епимера укључених у дефиницију суме прописане максималне концентрације) |
Жита и храна на бази жита |
≤ 4 |
|
Прерађена храна на бази жита за одојчад и малу децу |
≤ 2 |
У осталим случајевима примењује се следеће: LOQ је ≤ 0,5*прописане максималне концентрације а по могућности и нижа (≤ 0,2*прописане максималне концентрације).
Ако се LOQ примењује на суму токсина, тада је LOQ за појединачне токсине ≤ 0,5*прописане максималне концентрације/n, при чему је n број токсина који је укључен у дефиницију суме прописане максималне концентрације.
Идентификација
За идентификацију се примењују критеријуми утврђени у Смерницама за идентификацију микотоксина и биљних токсина у храни и храни за животиње.33
Г.2.А.1.2. Проширење обима методе
Г.2.А.1.2.1. Проширење обима на друге микотоксине
Када се додају додатни аналити у обим постојеће потврдне методе, потребна је потпуна валидација да би се доказала погодност методе.
Г.2.А.1.2.2. Проширење на друге производе
Ако се зна или се очекује да ће потврдна метода бити применљива на друге производе, валидност за ове друге производе се верификује. Све док нови производ припада истој групи производа, наведеној у Табели 36. овог прилога, за коју је већ извршена почетна валидација, довољна је ограничена додатна валидација.
Г.2.А.2. Специфични захтеви за семи-квантитативне методе скрининга
Г.2.А.2.1. Обим
Овај одељак се односи на биоаналитичке методе засноване на имунолошком препознавању или везивању на рецепторе (као што су ЕLISА, биохемијске траке за тестирање – dip-sticks, уређаји за тестирање латералног тока – lateral flow и имуносензори) и физичко-хемијске методе које се заснивају на хроматографији или
––––––––
33 Доступно на: https://food.ec.europa.eu/document/download/f16cac78-9318-4f1f-b2fa-efb25d2f1880_en
директној детекцији уз помоћ масене спектрометрије (нпр. масена спектрометрија у амбијенталном окружењу).
Друге методе (нпр. танкослојна хроматографија) нису искључене, под условом да се добијени сигнали директно односе на микотоксине који се разматрају и омогућавају примену принципа описаног у наставку.
Специфични захтеви се примењују на методе чији је резултат мерења нумеричка вредност, као нпр. (релативни) одговор читача биохемијске траке за тестирање, сигнал из везаног система течне хроматографије – масене спектрометрије (LC-MS) итд., као и да се примењују уобичајени статистички подаци.
Захтеви се не примењују на методе којима се не добијају нумеричке вредности, као нпр. када је реч само о линији која је присутна или одсутна, а које захтевају различите приступе валидацији. Специфични захтеви за ове методе су дати у тачки Г.2.3. овог прилога.
Овај део прилога описује поступке за валидацију метода скрининга путем међулабораторијске валидације, верификацију изводљивости методе која је валидирана у оквиру међулабораторијског теста, као и валидацију методе скрининга у једној лабораторији.
Г.2.А.2.2. Поступак валидације
Циљ валидације је доказивање погодности примене методе скрининга. То се постиже одређивањем граничне вредности и одређивањем односа лажно негативних и лажно сумњивих резултата. У ова два параметра уграђене су карактеристике изводљивости, као што су осетљивост, селективност и прецизност.
Методе скрининга могу бити валидиране међулабораторијском валидацијом или валидацијом у једној лабораторији. Ако су подаци из међулабораторијске валидације методе већ доступни за одређену комбинацију микотоксин/матрикс/STC, довољна је верификација изводљивости методе у лабораторији која примењује методу.
Г.2.А.2.2.1. Почетна валидација уз помоћ валидације у једној лабораторији
Микотоксини:
Валидација се спроводи за сваки појединачни микотоксин из обима примене. У случају биоаналитичких метода којима се добија комбиновани одговор за одређену групу микотоксина (нпр. афлатоксини B1, B2, G1 и G2, фумонизини B1 и B2 ), доказује се применљивост, па се у обиму примене методе наводе ограничења у погледу испитивања.
Сматра се да се нежељеном унакрсном реактивношћу (нпр. DON-3-глукозид, 3– или 15-ацетил-DON у имунолошким методама испитивања DON-а) не повећава проценат лажно негативних резултата циљних микотоксина, али може доћи до повећања процента лажно сумњивих резултата. Нежељено повећање опада спровођењем потврдног испитивања ради недвосмисленe идентификације и квантификације микотоксина.
Матрикси:
Почетну валидацију треба спровести за сваки производ, односно, ако је познато да се метода може применити на више производа, за сваку групу производа. У другом случају, из одговарајуће групе се бира један репрезентативан и релевантан производ, како је наведено у Табели 36. овог прилога.
Скуп узорака:
Минималан број различитих узорака потребних за валидацију је 20 хомогених негативних контролних узорака и 20 хомогених позитивних контролних узорака који садрже микотоксин у циљној концентрацији скрининга (STC), испитивани под условима средње прецизности (RSDRi), распоређени током пет различитих дана. Додатни сетови од 20 узорака који садрже микотоксин на другим нивоима могу да се додају скупу за валидацију како би се стекао увид у то у којој мери метода може да разликује различите концентрације микотоксина.
Концентрација:
За сваку циљну концентрацију скрининга (STC), која се користи у рутинској примени, спроводи се валидација.
Г.2.А.2.2.2. Почетна валидација међулабораторијским испитивањем
Валидација међулабораторијским испитивањем спроводи се у складу са SRPS ISO 5725: 2007 или IUPAC међународним усклађеним протоколом или другим међународно признатим протоколом о међулабораторијским испитивањима који захтева укључивање валидних података из најмање осам различитих лабораторија. Једина разлика у односу на валидацију у једној лабораторији је та што 20 или више узорака по производу/нивоу може бити равномерно подељено међу лабораторијима које учествују, са најмање два узорка по лабораторији.
Г.2.А.2.3. Одређивање граничног нивоа и процента лажно сумњивих резултата слепих узорака
Као основа за израчунавање тражених параметара узимају се (релативни) одговори у случају негативних и позитивних контролних узорака.
Методе скрининга код којих је одговор пропорционалан концентрацији микотоксина
На методе скрининга код којих је одговор пропорционалан концентрацији микотоксина, примењује се следеће:
Гранична вредност = RSTC – t-вредност0,05 x SDSTC,
где је:
RSTC средњи одговор позитивних контролних узорака (при циљној концентрацији скринингa (STC));
t-вредност једносмерна t-вредност за проценат лажно негативних резултата од 5% (као што је наведено у Табели 37. овог прилога);
SDSTC стандардна девијација.
Методе скрининга код којих је одговор обрнуто пропорционалан концентрацији микотоксина
Слично томе, на методе скрининга код којих је одговор обрнуто пропорционалан концентрацији микотоксина гранична вредност се одређује као:
Гранична вредност = RSTC + t-вредност0,05 x SDSTC.
Користећи ову специфичну t-вредност за утврђивање граничне вредности, задата вредност процента лажно негативних резултата је подразумевано постављена на 5%.
Оцена погодности за сврху
Резултати добијени на основу негативних контролних узорака користе се за процену одговарајућег процента лажно сумњивих резултата, а t-вредност се израчунава у случају када је резултат негативног контролног узорка већи од граничне вредности, па је погрешно класификован као сумњив.
За методе скрининга код којих је одговор пропорционалан концентрацији микотоксина t-вредност је:

За методе скрининга код којих је одговор обрнуто пропорционалан концентрацији микотоксина t-вредност је:
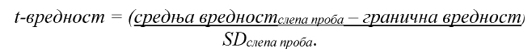
Из добијене t-вредности на основу степена слободе који су израчунати из бројних експеримената, може се израчунати вероватноћа појаве лажно сумњивих узорака за једнострану дистрибуцију (нпр. функција прошириве табеле „TDIST”) или узети из табеле за t-дистрибуцију (као што је наведено у Табели 37. овог прилога).
Одговарајућом вредношћу једностране t-дистрибуције одређује се проценат лажно сумњивих резултата.
Овај концепт је детаљно описан на примеру у Аналитичкој и биоаналитичкој хемији DOI 10.1007/s00216 -013-6922-1.
Г.2.А.2.4. Проширење области примене методе
Г.2.А.2.4.1. Проширење области примене на друге микотоксине
Када се области примене постојеће методе скрининга додају нови микотоксини, нужно је спровести потпуну валидацију ради доказивања погодности методе.
Г.2.А.2.4.2. Проширење на друге производе
Ако је познато или се очекује да ће метода скрининга бити применљива на друге производе, проверава се поузданост њене примене на те друге производе. Све док нови производ припада групи производа ,као што је наведено у Табели 36. овог прилога, за коју је већ спроведена почетна валидација, довољно је спровести додатну ограничену валидацију. Да би се то урадило, анализира се најмање 10 хомогених негативних и 10 хомогених позитивних контролних узорака (при циљној концентрацији скринингa – STC), уз услове средње прецизности. Позитивни су контролни узорци изнад граничне вредности. У случају да овај критеријум није испуњен, потребна је потпуна валидација.
Г.2.А.2.5. Провера метода које су већ валидиране међулабораторијским испитивањима
За методе скрининга које су већ успешно валидиране међулабораторијским испитивањима проверава се њихова изводљивост. Да би се то учинило, анализира се најмање шест негативних и шест позитивних контролних узорака (при циљној концентрацији скринингa – STC). Позитивни су контролни узорци изнад граничне вредности. У случају да овај критеријум није испуњен, лабораторија спроводи анализу основног узрока како би утврдила зашто не може да понови резултат добијен у међулабораторијском испитивању. Тек након предузимања потребних корективних мера, лабораторија интерно поновно проверава изводљивост методе. У случају да лабораторија није у могућности да верификује резултате међулабораторијског испитивања, она одређује сопствену граничну вредност спроводећи потпуну валидацију у једној лабораторији.
Г.2.А.2.6. Стална провера методе / непрекидна валидација методе
Након почетне валидације, додатни подаци за валидацију се добијају укључивањем најмање два позитивна контролна узорка у сваку групу прегледаних узорака. Један позитивни контролни узорак је познат узорак (нпр. један који је коришћен током почетне валидације), други је од различитог производа из исте групе производа (у случају кад се испитује само један производ, употребљава се други узорак тог производа). Укључивање негативног контролног узорка није обавезно. Резултати добијени за два позитивна контролна узорка додају се постојећем скупу за валидацију.
Најмање једном годишње поново се утврђује гранична вредност и поново оцењује поузданост методе (поновна процена доступних QА/QC података добијених у последњој години). Стална провера методе има неколико сврха, укључујући:
– контролу квалитета серије узорака која се проверава;
– пружање информација о робусности методе под условима у лабораторији која примењује методу;
– оправданост применљивости методе на различите производе;
– омогућавање прилагођавања граничних вредности у случају поступних одступања током времена.
Г.2.А.2.7. Извештај о валидацији
Извештај о валидацији садржи:
– изјаву о циљној концентрацији скрининга (STC);
– изјаву о добијеној граничној вредности (напомена: гранична вредност има једнак број значајних цифара као и STC. Нумеричке вредности које се користе за израчунавање граничне вредности имају најмање једну значајну цифру више од STC);
– изјаву о израчунатом проценту лажно сумњивих резултата;
– изјаву о начину добијања процента лажно сумњивих резултата који подлежу провери (напомена: изјава о израчунатом проценту лажно сумњивих резултата показује да ли је метода погодна за сврху, с обзиром на то да указује на број слепих узорака (или контаминацију ниског нивоа)).
Табела 36.
Групе производа за валидацију метода скрининга
|
Групе производа |
Категорије производа |
Типични репрезентативни производи обухваћени категоријом |
|
Високи садржај воде |
Воћни сокови |
Сок од јабуке, сок од грожђа |
|
Алкохолна пића |
Вино, пиво, сајдер |
|
|
Коренасто и кртоласто поврће |
Свежи ђумбир, биљни чејеви (течни) |
|
|
Пире на бази жита или воћа |
Пире за одојчад и малу децу |
|
|
Високи садржај масти |
Језграсто воћа и орашасти плодови |
Орах, лешник, кестен |
|
Семенке уљарица и њихови производи |
Уљана репица, сунцокрет, семе памука, соја, кикирики, сусам итд. |
|
|
Плодови уљарица и њихови производи |
Уља и пасте (нпр. маслац од кикирикија, тахини) |
|
|
Висок садржај скроба и/или протеина и низак садржај воде и масти |
Зрна житарица и њихови производи |
Пшеница, раж, јечам, кукуруз, пиринач, овас Интегрални хлеб, хлеб од белог брашна, крекери, жита за доручак, тестенина |
|
Дијететски производи |
Суви прашкови за припрему хране за одојчад и малу децу |
|
|
Висок садржај киселине и висок садржај воде(*) |
Производи од цитруса/ цитрусног воћа/агрума |
|
|
„Компликовани или јединствени производи”(**) |
Какао и његови производи, копра и њени производи, кафа, чај (сушени производ) Зачини, корен сладића/госпиног биља/слатки корен, биљни чејеви (сушени производ), дијететски производи, полен и производи од полена |
|
|
Висок садржај шећера, низак садржај воде |
Сушено воће |
Смокве, грожђице (од белог грожђа, од белог грожђа без семенки, од црног грожђа без семенки) |
|
Млеко и млечни производи |
Млеко |
Кравље, козије и бивоље млеко |
|
Сир |
Крављи и козији сир |
|
|
Млечни производи (нпр. млеко у праху) |
Јогурт, павлака |
|
|
Месо |
Јестиве изнутрице |
Бубрези, јетра |
|
Мишићно месо, производи од меса |
Шунка |
|
|
(*) Ако се у току екстракције за стабилизацију рН промена употребљава пуферски раствор, тада се та група производа може спојити у једну групу производа „Висок садржај воде”. (**) „Компликоване или јединствене производи” треба потпуно валидирати само ако се често испитују. Ако се испитују само повремено, валидација се може свести на проверу нивоа извештивања коришћењем обогаћених екстраката слепе пробе. |
||
Табела 37.
Једнострана t-вредност за лажно негативни проценат од 5%
|
Степен слободе |
Број понављања |
t-вредност (5%) |
|
10 |
11 |
1,812 |
|
11 |
12 |
1,796 |
|
12 |
13 |
1,782 |
|
13 |
14 |
1,771 |
|
14 |
15 |
1,761 |
|
15 |
16 |
1,753 |
|
16 |
17 |
1,746 |
|
17 |
18 |
1,74 |
|
18 |
19 |
1,734 |
|
19 |
20 |
1,729 |
|
20 |
21 |
1,725 |
|
21 |
22 |
1,721 |
|
22 |
23 |
1,717 |
|
23 |
24 |
1,714 |
|
24 |
25 |
1,711 |
|
25 |
26 |
1,708 |
|
26 |
27 |
1,706 |
|
27 |
28 |
1,703 |
|
28 |
29 |
1,701 |
|
29 |
30 |
1,699 |
|
30 |
31 |
1,697 |
|
40 |
41 |
1,684 |
|
60 |
61 |
1,671 |
|
120 |
121 |
1,658 |
|
∞ |
∞ |
1,645 |
Г.2.3. Захтеви за квалитативне методе скрининга (методе које не дају нумеричке вредности)
Развој смерница за валидацију метода бинарних тестова тренутно је у фокусу различитих тела за стандардизацију (нпр. AOAC, ISO). AOAC је недавно израдио смернице окоје се односе на ово питање. Овај документ се може посматрати као тренутно стање технике, односно најновији важећи документ у тој области. Према томе, методе које дају бинарне резултате (нпр. визуелни преглед биохемијске траке за тестирање) треба валидирати у складу са међународним смерницама AOAC за валидацију метода квалитативне бинарне хемије.34
Међутим, могу се користити и друге признате смернице за валидацију, као што је приступ предвиђен у SRPS CEN ISO/TS 23758:2021 IDF/RM 251 Смернице за валидацију квалитативних метода скрининга за детекцију остатака ветеринарских лекова у млеку и производима од млека.
Г.2.4. Квантитативно одређивање ергот склероције
Ергот склероцијe у житима се утврђују визуелном (макроскопском/микроскопском) идентификацијом ергот склероција и делова ергот склероција. Квантификација се спроводи вагањем количине идентификованих ергот склероција и делова ергот склероција величине > 0,5 mm.
Г.3. Процена мерне несигурности, израчунавање аналитичког приноса и извештавање о резултатима35
Г.3.1. Потврдне методе
Аналитички резултат се саопштава на следећи начин:
– са корекцијом за аналитички принос, при чему се наводи ниво аналитичког приноса. Корекција за аналитички принос није потребна у случају да је стопа аналитичког приноса између 90% и 110%;
––––––––
34 Доступно на: https://academic.oup.com/jaoac/article-pdf/97/5/1492/32425003/jaoac1492.pdf.
35 Више детаља о поступцима за процену мерне несигурности и о поступцима за оцену аналитичког приноса може се наћи у Извештају о односу између аналитичких резултата, мерне несигурности, фактора аналитичког приноса и одредби законодавства ЕУ о храни и храни за животиње, који је доступан на: https://food.ec.europa.eu/system/files/2016-10/cs_contaminants_sampling_analysis-report_2004_en.pdf.
– као x ± U, при чему је x аналитички резултат, а U проширена мерна несигурност, добијена коришћењем фактора покривености 2, који даје ниво поузданости од око 95%.
Као могућност може се пријавити подразумевана проширена мерна несигурност од 50%, под условом да лабораторија испуњава све захтеве за прецизност наведене у одељку Г.2.А. Појединачна лабораторија то може доказати испуњавањем критеријума за поновљивост (RSDr) и репродуктивност унутар лабораторије (RSDwR), уз успешно учешће у програмима тестирања оспособљености (осим ако није доступан одговарајући програм за тестирање оспособљености), јер средњи z-резултат при коме је |z| ≤ 2 показује да је испуњена захтевана репродуктивност (RSDR) (на основу циљне стандардне девијације од 25%).
У случају да је прописана максимална концентрација за збир токсина (нпр. афлатоксини, Т-2/НТ-2-токсин, фумонизини, ергот алкалоиди), биће приказани резултати анализе свих појединачних токсина. За ергот алкалоиде, такође је дозвољено извести збир сваког од шест парова епимера уместо 12 појединачних епимера.
Корекција аналитичког приноса, ако је применљива, ради се за сваки од појединачних токсина пре сумирања концентрација. За ергот алкалоиде, корекција се такође може урадити на основу аналитичког приноса добијеног за сваки од парова епимера.
За верификацију усклађености са сумом прописане максималне концентрације примениће се приступ доње границе што значи да ће резултати за појединачне токсине који су < LOQ бити замењени нулом за израчунавање суме.
Садашња правила тумачења резултата анализе у погледу прихватања или одбијања производне партије примењују се на аналитички резултат добијен на узорку за службену контролу.
Г.3.2. Методе скрининга
Резултат методе скрининга исказује се тако да је узорак усаглашен или да постоји сумња о његовој неусаглашености.
„Сумња о неусаглашености” значи да узорак премашује граничну вредност и може да садржи веће количине микотоксина од STC. У случају сумњивог резултата покреће се потврдно испитивање ради недвосмислене идентификације и квантификације микотоксина.
„Усаглашен” значи да је удео микотоксина у узорку мањи од STC са сигурношћу од 95%, тј. да постоји 5% могућности да су узорци нетачно приказани као негативни. Аналитички резултат приказује се као „< ниво STC ”, при чему је ниво STC наведен.
Г.4. Лабораторијски стандарди квалитета
Лабораторија треба да испуњава услове уређене прописом који се односи на безбедност хране.
ПРИЛОГ 3
МЕТОДЕ УЗОРКОВАЊА И ИСПИТИВАЊА УЗОРАКА ХРАНЕ ЗА СЛУЖБЕНУ КОНТРОЛУ НИВОА НИТРАТА36
A) ОПШТИ ЗАХТЕВИ
А.1. Сврха и циљ узорковања
Узорци намењени за службену контролу нивоа нитрата у храни која је наведена у посебном пропису којим се уређују максималне концентрације одређених контаминената у храни, узимају се у складу са методама прописаним у овом прилогу. Тако добијени збирни узорци, узети директно са поља или из производне партије, сматрају се репрезентативним за производне партије.
Усаглашеност са прописаним максималним концентрацијама, утврђује се на основу нивоа утврђених у лабораторијским узорцима.
––––––––
36 Прилог 3 овог правилника усклађен је са Уредбом Комисије (ЕЗ) број 1882/2006 од 19. децембра 2006. године о утврђивању метода узорковања и испитивања за службене контроле нивоа нитрата у одређеним прехрамбеним производима (Commission Regulation (EC) No 1882/2006 of 19 December 2006 Laying Down Methods of Sampling and Analysis for the Official Control of the Levels of Nitrates in Certain Foodstuff)
А.2. Дефиниције
Примењују се дефиниције из Прилога 1 Одељак А) овог правилника, као и следеће дефиниције:
1) поље јесте одређена површина земље са истим типом земљишта, начином узгојa и временом бербе, на коме се налази само једна сорта зелене салате или спанаћа у истој фази развоја и истом предвиђеном времену бербе; у опису методе узорковања, реч: „поље”, може се заменити речима: „производна партија”;
2) заштићен простор јесте одговарајућа површина земљишта под стаклеником или пластеником са пластичном или полиетиленском фолијом, или на други начин заштићен простор, са једном сортом зелене салате односно спанаћа у истој фази развоја и истом предвиђеном времену бербе; у опису методе узорковања, речи: „заштићени простор”, могу се заменити са речима: „производна партија”;
3) велика производна партија јесте површина земљишта већа од 3 ha или појединачно паковање веће од 30 t.
А.3. Општа правила
А.3.1. Лице које обавља узорковање
Узорковање обавља надлежни инспектор у складу са поделом надлежности уређеном прописом који се односи на безбедност хране.
А.3.2. Храна која се узоркује
Свака производна партија хране предвиђена за испитивање узоркује се посебно. Велике производне партије (нпр. веће од 30 t или вeће од 3 ha) деле се на потпартије које се узоркују посебно.
А.3.3. Мере предострожности
Током узорковања хране и припреме узорака предузимају се мере предострожности како би се избегле било какве промене које би могле:
– утицати на садржај нитрата;
– негативно утицати на аналитичко одређивање;
– утицати на збирне узорке и учинити их нерепрезентативним, (нпр. присутво земље у зеленој салати или спанаћу у току припреме узорка);
– утицати на безбедност хране или целовитост производних партија које се узоркују.
Такође, треба предузети све потребне мере за заштиту лица која узимају узорке.
А.3.4. Појединачни узорци
Када је могуће, појединачни узорци се узимају са различитих места у производној партији или потпартији.
Одступање од поступка узимања појединачних узорака наводи се у записнику о узорковању из тачке А.3.8. овог прилога.
А.3.5. Припрема збирног узорка
Збирни узорак се добија обједињавањем појединачних узорака.
А.3.6. Дупли узорци
Дупли узорци за сврхе службене контроле, додатна стручна мишљења (жалбе) и судске поступке узимају се из хомогенизованог збирног узорка.
А.3.7. Паковање и достављање узорака
Сваки узети узорак се ставља у чисту, инертну, непрозирну пластичну кесу која се чврсто затвара ради спречавања губитка влаге и заштите од оштећења и загађења.
Узорак се доставља лабораторији на испитивање у року од 24 часа од узимања узорка и у току транспорта треба да се држи на хладном. Ако то није могуће, узорак треба дубоко замрзнути у року од 24 часа од узимања узорка и чувати замрзнут (најдуже шест недеља од дана замрзавања).
Треба предузети све додатне мере предострожности да би се избегле све промене у саставу узорка до којих би могло доћи у току транспорта или складиштења.
А.3.8. Пломбирање и означавање узорака
Сваки узорак који се узима за службену контролу се пломбира и означава на месту узорковања.
О сваком узорковању сачињава се записник о узорковању који омогућава да свака производна партија или потпартија буде недвосмислено идентификована и у којем се наводи назив сорте, произвођача, датум и место узорковања, субјекат у пословању храном одговоран за пошиљку, заједно са додатним подацима који би могли бити од користи при лабораторијском испитивању.
А.4. Различите врсте производних партија
Храна се може стављати на тржиште у расутом стању (ринфуз) или у паковањима, укључујући вреће, врећице и гајбе, или у појединачним малопродајним паковањима. Метода узорковања може се применити на све различите облике у којима се роба ставља на тржиште.
Б) МЕТОДА УЗОРКОВАЊА
Када год је то могуће, појединачни узорци се узимају на различитим местима у производној партији или потпартији.
Б.1. Узорковање у пољу
Ако је потребно узорковати зелену салату или спанаћ у пољу, узорковање се спроводи на следећи начин:
– појединачни узорци се узимају са површина које су репрезентативни примерци поља или заштићеног простора;
– површине са различитим типовима земљишта, на којима се спроводе различити начини узгоја, или на којима се узгајају различите сорте зелене салате или спанаћа, или на којима се зелена салата или спанаћ беру у различито време, сматрају се одвојеним производним партијама или пољима; ако је поље веће од 3 hа, дели се на потпартије од 2 hа, с тим да се свака потпартија узоркује посебно;
– појединачни узорци се узимају ходајући преко поља у облику слова „W” или „X”, а ако се биљке гаје у уским лејама или заштићеном простору појединачни узорци се, према обрасцу у облику слова „W или „X”, узимају из неколико леја и сакупљају ради формирања збирног узорка;
– узорци се узимају сечењем биљака непосредно до земље;
– збирни узорак садржи најмање 10 биљака и има масу од најмање 1 kg;
– узоркују се само јединице (биљке) комерцијалне величине37;
– са сваке узорковане јединице (биљке) скида се земља, као и нејестиви спољашњи и оштећени листови.
Б.2. Узорковање на тржишту производних партија спанаћа, зелене салате, хране за бебе и прерађене хране на бази житарица за одојчад и малу децу
Ова метода узорковања се примењује на производне партије масе 25 t или мање.
У случају већих производна партија (> 30 t), производна партија се дели на потпартије од приближно 25 t, под условом да се могу физички раздвојити. Имајући у виду да маса производне партије није увек једнака збиру маса потпартија од 25 t, маса потпартије може прећи 25 t за највише 20%. То значи да маса потпартије може бити у распону од 15 до 30 t. У случају да се производна партија не може физички раздвојити на потпартије, узорак се узима из производне партије.
Маса збирног узорка је најмање 1 kg, осим када то није могуће, нпр. код узорковања једне главице или једног паковања.
Најмањи број појединачних узорака који се узима из производне партије дат је у Табели 1. овог прилога.
––––––––
37 Величина зелене салате, широколисне и ендивије коврџавих листова уређена је прописима о квалитету.
Табела 1.
Најмањи број појединачних узорака који се узимају из производне партије
|
Маса производне партије (у kg ) |
Најмањи број појединачних узорака |
Најмања маса збирног узорка (у kg ) |
|
˂ 50 |
3 |
1 |
|
50 до 500 |
5 |
1 |
|
˃ 500 |
10 |
1 |
Ако се производна партија састоји од појединачних паковања, број паковања који се узоркује ради формирања збирног узорка дат је у Табели 2. овог прилога.
Табела 2.
Број паковања (појединачних узорака) који се узимају за збирни узорак, ако се производна партија састоји од појединачних паковања
|
Број паковања или јединица у производној партији |
Број паковања или јединица које треба узорковати |
Најмања маса збирног узорка (у kg) |
|
1–25 |
1 паковање или јединица |
1 |
|
26–100 |
око 5 %, а најмање 2 паковања или јединице |
1 |
|
˃ 100 |
око 5 %, а највише 10 паковања или јединица |
1 |
Свака производна партија или потпартија, за коју се проверава усаглашеност, узоркује се посебно. Међутим, у случајевима када би такав начин узорковања довео до неприхватљивих комерцијалних последица услед оштећења производне партије (због облика паковања, транспортних средстава и сл.), може се применити алтернативна метода узорковања, под условом да обезбеђује да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована.
Место са кога је узет узорак у производној партији треба да се бира насумично, али, ако је то физички непрактично, место за узимање узорака треба одабрати насумично из приступачних делова производне партије.
Б.3. Узорковање у фази малопродаје
Узорковање хране у фази малопродаје спроводи се у складу сa методама прописаним у тачки Б.2. овог прилога. Ако то није могуће, може се применити алтернативна метода узорковања у фази малопродаје под условом да обезбеђује да збирни узорак буде довољно репрезентативан за узорковану производну партију и да је метода узорковања у потпуности описана и документована38.
Б.4. Прихватање производне партије или потпартије
Производна партија или потпартија се прихвата ако је аналитички резултат испитивања лабораторијског узорка у складу са прописаном максималном концентрацијом, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност.
Производна партија или потпартија се не прихвата ако аналитички резултат испитивања лабораторијског узорка ван сваке сумње прелази прописану максималну концентрацију, узимајући у обзир корекцију резултата за аналитички принос и мерну несигурност (тј. за процену усаглашености користи се аналитички резултат коригован за аналитички принос и умањен за проширену мерну несигурност).
В) ПРИПРЕМА УЗОРКА
У случају узорковања свежих производа, припрема узорка, ако је могуће, обавља се у року од 24 сата од узорковања. Ако то није могуће, узорак се чува замрзнут (највише до шест недеља).
––––––––
38 У случају да је део који треба узорковати тако мали да није могуће добити збирни узорак од 1 kg, маса збирног узорка може бити мања од 1 kg. Такође, ако се узоркује прерађена храна на бази житарица и храна за одојчад и малу децу, маса збирног узорка може бити 0,5 kg.
Са сваке узорковане појединачне јединице (биљке) уклања се земља, јако испрљани, нејестиви и оштећени спољашњи листови. Није дозвољено прање узорака, јер се прањем може смањити количина нитрата у узорцима.
Цео узорак се хомогенизује (додавање одређене количине воде није обавезно). У зависности од величине апарата за уситњавање (блендер/мацератор/сецкалица), може се хомогенизовати једна или више појединачних јединица. Замрзавање и уситњавање јединица пре хомогенизације може олакшати њихово мешање. Потребно је доказати да је коришћени поступак довео до потпуне хомогенизације узорка. Темељна хомогенизација је неопходна за максималну екстракцију и аналитички принос нитрата. Узорци се на овај начин третирају идентично, без обзира да ли су узорковани у пољу или у малопродаји.
За испитивање се узима један или више аналитичких узорака из хомогенизованог узорка.
Г) АНАЛИТИЧКА МЕТОДА, ИЗВЕШТАВАЊЕ О РЕЗУЛТАТИМА ИСПИТИВАЊА И ЗАХТЕВИ ЗА ЛАБОРАТОРИЈСКУ КОНТРОЛУ
Г.1. Дефиниције
Примењују се дефиниције од 1) до 6) из тачке В.3.1. Прилог 1 овог правилника.
Г.2. Општи захтеви
Потврдне методе испитивања које се користе у сврхе контроле хране треба да буду у складу са прописом којим се уређује службена контрола хране.
Г.3. Посебни захтеви
Г.3.1. Поступак екстракције
Посебну пажњу потребно је обратити на примену поступка екстракције. Доказано је да неколико поступака екстракције обезбеђује ефикасну екстракцију нитрата, као што је метода екстракције врућом водом или екстракција смешом метанола и воде (у односу 30:70). Екстракција хладном водом користи се само ако је узорак за испитивање пре екстракције био замрзнут.
Г.3.2 Критеријум изводљивости
Посебни критеријум за методе испитивања које се користе за праћење нивоа нитрата дати су у Табели 3. овог прилога.
Табела 3.
Критеријум изводљивости за нитрате
|
Критеријум |
Распон концентрације |
Препоручена вредност |
Максимално дозвољена вредност |
|
Аналитички принос |
< 500 mg/kg |
60–120% |
- |
|
≥ 500 mg/kg |
90–110% |
||
|
Прецизност RSDR |
Све |
Вредност добијена уз помоћ Horwitz-ове једначине |
2 × вредност добијена уз помоћ Horwitz-ове једначине |
|
Прецизност RSDr може се израчунати као 0,66 пута прецизност RSDR на нивоу концентрације концентрације која се разматра |
|||
Напомене уз критеријум изводљивости за нитрате:
– Опсези концентрација се не наводе, будући да се прецизност израчунава за релевантне концентрације.
– Прецизност се израчунава помоћу Horwitz-ове једначине, тј.:
RSDR = 2(1-0,5logC),
при чему је:
RSDR релативна стандардна девијација израчуната из резултата добијених под условима репродуктивности 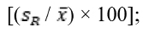
С однос концентрације (тј. 1 = 100 g/100g, 0,001 = 1 000 mg/kg).
Г.4. Извештавање о резултатима, процена мерне несигурности и израчунавање аналитичког приноса39
Аналитички резултат се изражава у истим јединицама и заокружује се на исти број децимала као и прописана максимална концентрација.
Аналитички резултат изражава се као кориговани или некориговани за аналитички принос. Обавезно се наводе начин извештавања и ниво аналитичког приноса. Резултат испитивања коригован за аналитички принос користи се за проверу усаглашености.
Аналитички резултат изражава се као x ± U, при чему је x аналитички резултат, а U проширена мерна несигурност, добијена коришћењем фактора покривености 2, који даје ниво поузданости од 95%.
Наведена правила тумачења аналитичког резултата у погледу прихватања или одбијања производне партије важе за аналитичке резултате добијене на узорку за службену контролу.
Г.5. Лабораторијски стандарди квалитета
Лабораторија треба да испуњава услове уређене прописом који се односи на безбедност хране.
ПРИЛОГ 4
МЕТОДЕ УЗОРКОВАЊА И ИСПИТИВАЊА УЗОРАКА ХРАНЕ ЗА СЛУЖБЕНУ КОНТРОЛУ НИВОА ДИОКСИНА, РСВ СЛИЧНИХ ДИОКСИНИМА И РСВ КОЈИ НИСУ СЛИЧНИ ДИОКСИНИМА40
1. МЕТОДЕ УЗОРКОВАЊА ЗА СЛУЖБЕНУ КОНТРОЛУ НИВОА ДИОКСИНА (PCDD/PCDF), РСВ СЛИЧНИХ ДИОКСИНИМА И РСВ КОЈИ НИСУ СЛИЧНИ ДИОКСИНИМА У ОДРЕЂЕНОЈ ХРАНИ
А) ДЕФИНИЦИЈЕ И СКРАЋЕНИЦЕ
Поједини изрази употребљени у овом прилогу имају следеће значење:
1) ниво/праг за деловање јесте количина одређене супстанце, због које се покрећу активности истраге / истраживања ради утврђивања извора те супстанце у случајевима када су откривене повећане количине те супстанце;
2) методе скрининга јесу методе која се користе за одабир оних узорака са концентрацијама PCDD/PCDF и диоксинима сличних РСВ које прелазе прописане максималне концентрације или нивое / прагове за деловање. Оне омогућавају економичну обраду великог броја узорака, чиме се повећава могућност откривања нових случајева када висока изложеност може довести до ризика за здравље потрошача. Методе скрининга се заснивају на биоаналитичким методама или методама гасне хроматографије/масене спектрометрије (GC-MS). Резултати узорака који премашују граничну вредност одређену за проверу усаглашености са максимално дозвољеном концентрацијом проверавају се спровођењем потпуног поновног испитивања оригиналног узорка коришћењем потврдне методе;
3) потврдне методе јесу методе које пружају потпуне или додатне информације које омогућавају недвосмислену идентификацију и квантификацију концентрација PCDD/PCDF и РСВ сличних
––––––––
39 Више детаља о поступцима за процену мерне несигурности и о поступцима за оцену аналитичког приноса може се наћи у Извештају о односу између аналитичких резултата, мерне несигурности, фактора аналитичког приноса и одредаба законодавства ЕУ о храни и храни за животиње (Report on the relationship between analytical results, measurement uncertainty, recovery factors and the provisions of EU food and feed legislation) – http://ec.europa.eu/food/food/chemicalsafety/contaminants/report– sampling_analysis _2004_en.pdf
40 Прилог 4 овог правилника усклађен је са Уредбом Комисије (ЕУ) број 2017/644 од 5. априла 2017. године о утврђивању метода за узорковање и испитивање за контролу нивоа диоксина, РСВ сличних диоксинима и РСВ који нису слични диоксинима у одређеним прехрамбеним производима и о стављању ван снаге Уредбе (ЕУ) број 589/2014 (Commission Regulation (EU) 2017/644 of 5 April 2017 laying down methods of sampling and analysis for the control of levels of dioxins, dioxin-like PCBs and non-dioxin-like PCBs in certain foodstuffs and repealing Regulation (EU) No 589/2014).
диоксинима на максималном нивоу или, у случају потребе, на нивоу/прагу за деловање. Ове методе користе гасну хроматографију / масену спектрометрију високе резолуције (GC-HRMS) или гасну хроматографију / тандемску масну спектрометрију (GC-MS/MS);
4) биоаналитичке методе јесу методе које се заснивају на биолошким начелима, као што су ћелијски тестови, рецепторски или имунолошки тестови. Ове методе не дају резултате на нивоу конгенера, већ само показују41 вредности токсичних еквивалената (ТЕQ) изражених у биоаналитичким еквивалентима (ВЕQ), с обзиром на то да сва једињења присутна у изолату узорка који произведу одговор при испитивању не испуњавају све захтеве начела ТЕQ;
5) аналитички принос добијен биоанализом јесте количина ВЕQ израчуната из калибрационе криве за 2,3,7,8-тетрахлордибензо-р-диоксин (ТСDD) или полихлоровани бифенил 126 (РСВ 126), коригована за вредност слепе пробе и затим подељенa са вредношћу ТЕQ одређеном потврдном методом. Ова метода има за циљ да коригује факторе као што су: губитак PCDD/PCDF и диоксинима сличних једињења током екстракције и пречишћавања, смањење или побољшање одговора коекстрахованих једињења (агонистички и антагонистички ефекти), квалитет уклапања криве или разлике између вредности ТЕF и релативне способности (RЕР). Аналитички принос добијен биоанализом израчунава се из одговарајућих референтних узорака који имају репрезентативну дистрибуцију конгенера око прописане максималне концентрације или нивоа / прага за деловање;
6) двоструко испитивање јесте засебно испитивање циљних аналита коришћењем другог аликвота истог хомогенизованог узорка;
7) прихватљива специфична граница42 квантификације појединачног конгенера у узорку јесте најмањи садржај аналита који се може измерити са прихватљивом статистичком сигурношћу, који испуњава критеријуме идентификације који су описани у међународно признатим стандардима као што је SRPS ЕN 16215:2020 (Храна за животиње – Методе узимања узорака – Одређивање диоксина и диоксинима сличних РСВ и индикаторских РСВ помоћу GC-HRMS) и/или у најновијим ревизијама метода ЕРА 1613 и 1668.
Граница квантификације појединачог конгенера може се дефинисати као:
– концентрација аналита у екстракту узорка која даје инструментални одговор при праћењу два различита јона, који треба пратити уз однос сигнала и шума (сигнал / шум) 3:1 за најмање интензиван сигнал сирових података, или ако из техничких разлога израчунавање односа сигнал/шум не даје поуздане резултате,
– тачка најниже концентрације на калибрационој криви која даје прихватљиво (≤ 30%) и константно одступање (мерено најмање на почетку и на крају низа (скупа) аналитичког узорка) од просечног релативног фактора одговора израчунатог за све тачке на калибрационој криви у свакој серији узорака43;
8) горња граница јесте концепт који захтева примену границе квантификације за израчунавање доприноса сваког појединачног конгенера који није квантификован;
9) доња граница јесте концепт који захтева коришћење нуле за израчунавање доприноса сваког појединачног конгенера који није квантификован;
10) средња граница јесте концепт који захтева примену половине границе квантификације за израчунавање доприноса сваког појединачног конгенера који није квантификован.
Поједине скраћенице које се користе у овом прилогу имају следеће значење:
BEQ јесу биоаналитички еквиваленти;
GC јесте гасна хроматографија;
HRMS јесте масена спектрометрија високе разолуције;
––––––––
41 Биоаналитичке методе нису специфичне за оне конгенере који су укључени у систем фактора еквивалентне токсичности (ТЕF). Друга структурно повезана једињења која се вежу на рецептор ароматичних угљоводоника (AhR) могу бити присутна у екстракту узорка који доприносе целокупном одговору, па према томе, биоаналитички резултати не могу бити процена, већ индикација нивоа ТЕQ у узорку.
42 Начела описана у Смерницама о процени границе детекције (LOD) и границе квантификације (LOQ) за мерења у области контаминената у храни и храни за животиње (Guidance Document on the Estimation of LOD and LOQ for Measurements in the Field of Contaminants in Feed and Food) поштују се ако је применљиво.
43 LOQ се израчунава из тачке најниже концентрације узимајући у обзир аналитички принос интерних стандарда и унос узорка.
LRMS јесте масена спектрометрија ниске резолуције;
МС/МС јесте тандем масена спектрометрија;
PCB јесте полихлоровани бифенил;
PCDD јесу 2, 3, 7, 8-супституисани полихлоровани дибензо-р-диоксини;
PCDF јесу полихлоровани дибензофурани;
QC јесте контрола квалитета;
REP јесте релативна способност;
ТЕF јесте фактор еквивалентне токсичности;
ТЕQ јесу токсични еквиваленти;
ТCDD јесте 2,3,7,8-тетрахлордибензо-р-диоксин;
U јесте проширена мерна несигурност.
Б) ПОЉЕ ПРИМЕНЕ
Узорци намењени за службену контролу нивоа диоксина (PCDD/PCDF), диоксинима сличних РСВ и диоксинима који нису слични РСВ у храни која је наведена у посебном пропису о максималним концентрацијама одређених контаминената у храни, узимају се у складу са методама прописаним у овом прилогу. Тако добијени збирни узорци сматрају се репрезентативним за производне партије или потпартије из којих су узети.
Усклађеност са прописаним максималним концентрацијама утврђује се на основу нивоа утврђених у лабораторијским узорцима.
Да би се осигурала усклађеност са одредбама посебног прописа о хигијени хране, субјекат у пословању храном, када се узимају узорци за контролу нивоа диоксина (PCDD/PCDF), РСВ сличних диоксинима и РСВ који нису слични диоксинима, узима узорке у складу са методама прописаним у одељку Г) део 1. овог прилога или применити еквивалентна методи узорковања за коју је доказано да има исти ниво репрезентативности као метода узорковања описана у одељку Г) део 1. овог прилога.
В) ОПШТИ ЗАХТЕВИ
В.1. Лице које обавља узорковање
Узорковање обавља надлежни инспектор у складу са поделом надлежности уређеном прописом који се односи на безбедност хране.
В.2. Храна која се узоркује
Свака производна партија или потпартија коју треба испитивати узоркује се посебно.
В.3. Мере предострожности
Током узорковања хране и припреме узорака предузимају се мере предострожности како би се избегле било какве промене које би могле утицати на садржај диоксина и РСВ, негативно утицати на аналитичко одређивање, као и на збирне узорке и учинити их нерепрезентативним.
В.4. Појединачни узорци
Појединачни узорци се узимају са различитих места у производној партији или потпартији. Одступање од поступка узимања појединачних узорака наводи се у записнику о узорковању из одељка В) пододељак В.8. овог прилога.
В.5. Припрема збирног узорка
Збирни узорак се добија обједињавањем појединачних узорака. Маса збирног узорка је најмање 1 kg, осим ако то није практично, нпр. ако се узоркује једно паковање или ако производ има врло високу комерцијалну вредност.
В.6. Поновљени узорци
Поновљени узорци за сврхе службене контроле, додатна стручна мишљења (жалбе) и судске поступке узимају се из хомогенизованог збирног узорка. Количина лабораторијског узорка за потребе спровођења контрола је таква да је довољна да омогући најмање двоструко испитивање.
В.7. Паковање и достављање узорака
Сваки узорак се ставља у чисту, инертну посуду која пружа одговарајућу заштиту од контаминације, губитка аналита адсорпцијом на унутрашњи зид посуде и оштећења у транспорту. Потребно је предузети све мере предострожности како би се избегла промена састава узорака до које би могло доћи током транспорта или складиштења.
В.8. Пломбирање и означавање узорака
Сваки узорак који се узима за службену контролу се пломбира и означава на месту узорковања.
О сваком узорковању сачињава се записник о узорковању који омогућава да свака производна партија буде недвосмислено идентификована и у којем се наводи датум и место узорковања, заједно са свим додатним подацима који би могли бити од користи при лабораторијском испитивању.
Г) ПЛАН УЗОРКОВАЊА
Метода узорковања која се користи треба да обезбеди репрезентативност збирног узорка производне партије, односно потпартије коју треба контролисати.
Г.1. Подела производне партије на потпартије
Велике производне партије деле се на потпартије под условом да се потпартија може и физички одвојити. За храну која се продаје у расутом стању (нпр. биљно уље) за поделу прозводне партије на потпартије примењује се Табела 1. овог прилога. За остале производе примењује се Табела 2. овог прилога. Узимајући у обзир да маса производне партије није увек тачан збир маса потпартија, маса потпартије може прећи доленаведену масу за највише 20%.
Табела 1.
Подела производних партија на потпартије за храну која се продаје у расутом стању
|
Маса производне партије (у t) |
Маса (у t) или број потпартија |
|
≥ 1500 |
500 |
|
> 300 и < 1.500 |
3 потпартије |
|
≥ 50 и ≤ 300 |
100 |
|
< 50 |
– |
Табела 2.
Подела производних партија на потпартије за осталу храну
|
Маса производне партије (у t) |
Маса (у t) или број потпартија |
|
≥ 15 |
15–30 |
|
< 15 |
– |
Г.2. Број појединачних узорака
Збирни узорак, који обједињује све појединачне узорке, је најмање 1 kg, како је наведено у одељку В) пододељак В.5. овог прилога.
Минималан број појединачних узорака који се узима из производне партије или потпартије наведен је у табелама 3. и 4. овог прилога.
У случају да се ради о течним производима у расутом стању, производне партије или потпартије треба темељно промешати непосредно пре узорковања, колико год је то могуће, ручно или помоћу механичких уређаја, у мери у којој то неће утицати на квалитет производа. У том случају се претпоставља да ће се испитивани контаминенти равномерно распоредити кроз целу производну партију или потпартију, односно да је наведени контаминент хомогено дистрибуиран у датој производној партији или потпартији. Стога је довољно узети три појединачна узорка из производне партије или потпартије да би се формирао збирни узорак.
Појединачни узорци су сличне масе. Маса појединачног узорка је најмање 100 g.
Свако одступање од ове методе уноси се у записник из одељка В) пододељак В.8. овог прилога.
У складу са одредбама прописа којим се уређује праћење одређених супстанци и њихових резидуа у одређеним производима животињског порекла, збирни узорак за кокошја јаја је најмање 12 јаја (за неупаковане производне партије, као и за производне партије које се састоје од појединачних паковања примењују се табеле 3. и 4. овог прилога).
Ако се производна партија или потпартија састоји од појединачних паковања или јединица, број паковања или јединица који се узима, да би се формирао збирни узорак, дат је у Табели 4. овог прилога.
Табела 3.
Минималан број појединачних узорака који се узима из производне партије или потпартије
|
Маса или запремина производне партије/потпартије (у kg или l) |
Минималан број појединачних узорака које треба узети |
|
< 50 |
3 |
|
≥ 50 и ≤ 500 |
5 |
|
> 500 |
10 |
Табела 4.
Број паковања или јединица (појединачних узорака) који се узимају за збирни узорак, када се производна партија или потпартија састоји од појединачних паковања или јединица
|
Број паковања или јединица у производној партији/потпартији |
Број паковања или јединица које треба узети |
|
≤ 25 |
најмање 1 паковање илијединица |
|
26 до 100 |
око 5%, а најмање 2 паковања или јединице |
|
> 100 |
око 5%, а највише 10 паковања или јединица |
Г.3. Посебне одредбе за узорковање производних партија које садрже целе рибе упоредиве величине и масе
Сматра се да су рибе упоредиве величине и масе када њихова међусобна разлика у величини и маси није већа од 50%.
Број појединачних узорака који се узимају из производне партије прописан је у Табели 3. овог прилога. Збирни узорак који обједињује све појединачне узорке је најмање 1 kg, како је наведено у одељку В) пододељак В.5. овог прилога.
Када производна партија која се узоркује садржи ситну рибу (појединачне рибе масе < 1 kg), за формирање збирног узорка се, као појединачни узорак, узима цела риба. Када је маса добијеног збирног узорка > 3 kg, појединачни узорци се састоје од средњих делова рибе, од којих је сваки најмање 100 g, а који чине збирни узорак. За хомогенизацију узорка користи се цео део на који се примењује максимално дозвољена концентрација.
Када производна партија која се узоркује садржи веће рибе (појединачне рибе масе ≥ 1 kg), појединачни узорак се састоји од средњег дела рибе. Сваки појединачни узорак је најмање 100 g.
За рибе средње величине (≥ 1 kg и < 6 kg), појединачни узорак се састоји од комада рибе узетог између кичме и трбуха у средњем делу рибе.
За веома велике рибе (≥ 6 kg), појединачни узорак се узима са десне стране (гледано спреда) из меса дорзо-латералног мишића у средњем делу рибе. Када узимање таквог комада средњег дела рибе може довести до значајне економске штете могу се, без обзира на величину производне партије, прихватити као довољни:
– три појединачна узорка од по најмање 350 g или
– три појединачна узорка од по најмање 350 g, сваки из једнаког дела (175 g) меса мишића узетог близу репа и меса мишића узетог близу главе сваке рибе.
Г.4. Узорковање производних партија риба које садрже целе рибе различите величине и/или масе
За припрему узорка примењују се правила из одељка Г) пододељак Г.3. овог прилога.
Када преовлађује риба одређене величине/категорије или масе (око 80% или више производне партије), узорак се узима од рибе преовлађујуће величине или масе. Сматра се да је узорак репрезентативан за целу производну партију.
Када одређена класа/категорија величине или масе не преовлађује, обезбеђује се да риба одабрана за узорак буде репрезентативна за производну партију. За такве случајеве, посебна упутства су дата у Смерницама за узорковање целе рибе различите величине и/или масе44.
Г.5. Узорковање у фази малопродаје
Узорковање хране у малопродаји спроводи се у складу са одељком Г) пододељак Г.2. овог прилога.
Ако узорковање није могуће, може се користити алтернативна метода узорковања у фази малопродаје, под условом да је та метода репрезентативна за узорковану производну партију или потпартију и да је у потпуности документована.
Д) УСAГЛАШЕНОСТ ПРОИЗВОДНЕ ПАРТИЈЕ СА СПЕЦИФИКАЦИЈОМ
Д.1. Усаглашеност производне партије у погледу PCB који нису слични диоксинима
Производна партија је усаглашена ако аналитички резултат за суму РСВ који нису слични диоксинима не прелази прописану максималну концентрацију, узимајући у обзир проширену мерну несигурност45.
Производна партија није усаглашена са прописаном макималном концентрацијом ако средња вредност два горенаведена аналитичка резултата добијена двоструким испитивањем46 без сумње прелази максималну концентрацију, узимајући у обзир проширену мерну несигурност.
Проширена мерна несигурност израчунава се коришћењем фактора покривености 2, што даје ниво поузданости од 95%. Производна партија није усаглашена ако је средња вредност измерених вредности, умањена за средњу вредност проширене мерне несигурности, изнад прописане максималне концентрације.
Претходно наведена правила примењују се на аналитичке резултате добијене на узорку за службену контролу, као и у случају испитивања за додатна стручна мишљења (жалбе) и судске поступке.
Д.2. Усаглашеност производне партије у погледу диоксина и PCB који су слични диоксинима
Производна партија је усаглашена ако резултат појединачног испитивања добијен:
методом скрининга, са уделом лажно усаглашених резултата мањим од 5%, упућује на то да ниво не прелази прописане максималне концентрације за PCDD/PCDF и суме PCDD/PCDF и РСВ сличних диоксинима;
потврдном методом не прелази прописане максималне концентрације за PCDD/PCDF и суме PCDD/PCDF и РСВ сличних диоксинима, узимајући у обзир проширену мерну несигурност47.
Ради одлуке о усаглашености са прописаним максималним концентрацијама за PCDD/PCDF и суме PCDD/PCDF и РСВ сличних диоксинима за методе скрининга утврђује се гранична вредност (cut-off вредност).
––––––––
44 Guidance document on sampling of whole fishes of different size and/or weight”, https://ec.europa. eu/ food/sites/food/files/safety/docs/cs_contaminants_catalogue_dioxins_guidance-sampling_ exemples-dec2006_en. pdf
45 Ако је применљиво, поштују се начела наведена у Смерницама за мерну несигурност за лабораторије које обављају испитивања PCDD/F и РСВ коришћењем методе масене спектрометрије са разблажењем изотопа (Guidance Document on Measurement Uncertainty for Laboratories performing PCDD/F and PCB Analysis using Isotope Dilution Mass Spectrometry).
46 Двоструко испитивање је потребно ако резултат првог одређивања није усаглашен. Двоструко испитивање је потребно да би се искључила могућност унутрашње унакрсне контаминације или случајне замене узорака. У случају да се испитивање изводи у току инцидента контаминације, потврђивање двоструким испитивањем може се изоставити у случају да су узорци који су одабрани за испитивање следивошћу повезани са инцидентом контаминације и откривени ниво значајно већи од максималног нивоа.
47 Смернице за мерну несигурност за лабораторије које обављају испитивања PCDD/F и РСВ коришћењем методе масене спектрометрије са разблажењем изотопа (Guidance Document on Measurement Uncertainty for Laboratories performing PCDD/F and PCB Analysis using Isotope Dilution Mass Spectrometry) и Смернице о процени LOD и LOQ за мерења у области контаминената у храни и храни за животиње (Guidance Document on the Estimation of LOD and LOQ for Measurements in the Field of Contaminants in Feed and Food).
Производна партија није усаглашена са прописаним максималним концентрацијама ако средња вредност два горња аналитичка резултата, (двоструко испитивање48) добијена коришћењем потврдне методе, без сумње прелази прописану максималну концентрацију, узимајући у обзир проширену мерну несигурност.
Проширена мерна несигурност израчунава се коришћењем фактора покривености 2, што даје ниво поузданости од 95%. Производна партија није усаглашена ако је средња вредност измерених вредности, умањена за средњу вредност проширене мерне несигурности, изнад прописане максималне концентрације.
Сума процењених проширених несигурности засебних аналитичких резултата PCDD/PCDF и РСВ сличних диоксинима користи се да би се добила сума PCDD/PCDF и РСВ сличних диоксинима.
Претходнонаведена правила примењују се на аналитичке резултате добијене на узорку за службену контролу, као и у случају испитивања за додатна стручна мишљења (жалбе) и судске поступке.
Ђ) ПРЕKOРАЧЕЊЕ НИВОА / ПРАГА ЗА ДЕЛОВАЊЕ
Нивои / прагови за деловање представљају алат за одабир узорака у оним случајевима у којима је потребно утврдити извор контаминације и предузети мере за његово смањење или уклањање. Методе скрининга утврђују одговарајуће граничне вредности за одабир тих узорака. Ако је откривање извора и смањење или уклањање контаминације тешко, потврда прекорачења нивоа/прага за деловање може бити двоструко испитивање, користећи потврдну методу и узимајући у обзир проширену мерну несигурност49.
2. ПРИПРЕМА УЗОРКА И ЗАХТЕВИ ЗА МЕТОДЕ ИСПИТИВАЊА КОЈЕ СЕ КОРИСТЕ ЗА СЛУЖБЕНУ КОНТРОЛУ НИВОА ДИОКСИНА (PCDD/PCDF) И РСВ СЛИЧНИХ ДИОКСИНИМА У ОДРЕЂЕНОЈ ХРАНИ
А) ПОЉЕ ПРИМЕНЕ
Захтеви из овог дела прилога примењују се кад се храна испитује за службену контролу нивоа 2, 3, 7, 8-супституисаних полихлорованих дибензо-р-диоксина и полихлорованих дибензофурана (PCDD/PCDF) и полихлорованих бифенила сличних диоксинима (РСВ сличних диоксинима), као и за припрему узорака и аналитичких захтева за друге регулаторне сврхе, укључујући контроле које спроводи субјекат у пословању храном да би осигурао усклађеност са одредбама закона којим је прописана безбедност хране, односно посебним прописом којим су прописани услови хигијене хране.
Присуство PCDD/PCDF и РСВ сличних диоксинима у храни може се пратити уз помоћу две различите врсте аналитичких метода: методе скрининга и потврдне методе.
А.1. Методе скрининга
Циљ метода скрининга је одабир узорака са концентрацијама PCDD/PCDF и РСВ сличних диоксинима који прелазе прописане максималне концентрације или нивое / прагове за деловање. Методе скрининга омогућавају економичну обраду великог броја узорака, чиме се повећава могућност откривања нових случајева када висока изложеност може довести до ризика за здравље потрошача. Циљ њихове примене је избегавање лажно усаглашених резултата. Оне могу укључивати биоаналитичке методе и методе гасне хроматографије / масене спектрометрије (GС/МС).
Методе скрининга се заснивају на поређењу аналитичког резултата са граничном вредношћу (cut-off вредност), омогућавајући одлуку о могућем прекорачењу прописане максималне
––––––––
48 Двоструко испитивање је потребно ако резултат првог одређивања, у коме се примењују потврдне методе коришћењем 13 C-обележеног интерног стандарда, није усаглашен. Двоструко испитивање је потребно да би се искључила могућност унутрашње унакрсне контаминације или случајне замене узорака. У случају да се испитивање изводи у току инцидента контаминације, потврђивање двоструким испитивањем може се изоставити у случају да су узорци који су одабрани за испитивање следивошћу повезани са инцидентом контаминације и откривени ниво значајно већи од максималног нивоа.
49 Идентично објашњење и захтеви за двоструко испитивање за контролу нивоа / прагова деловање као у фусноти (49) за максималне нивое.
концентрације или нивоа / прага за деловање. Концентрација PCDD/PCDF и суме PCDD/PCDF и РСВ сличних диоксинима у узорцима за које се сумња да су неусаглашени са прописаном максималном концентрацијом одређују се или потврђују методом потврде.
Осим тога, методе скрининга могу упутити на присуство концентрација PCDD/PCDF и РСВ сличних диоксинима у узорку. У случају примене биоаналитичких метода скрининга, резултати се изражавају као биоаналитички еквиваленти (ВЕQ), док се у случају примене физичко-хемијских GС-МС метода резултати изражавају као токсични еквиваленти (ТЕQ). Нумерички наведени резултати метода скрининга су погодни за доказивање усаглашености или сумње на неусаглшеност или прелажење нивоа / прага за деловање и показују распон концентрација у случају даљег праћења уз помоћ потврдних метода. Методе скрининга нису погодне за сврхе као што су оцена нивоа присуства, процена уноса, праћење тренда нивоа или поновна процена нивоа / прагова за деловање и прописаних максималних концентрација.
А.2. Потврдне методе
Потврдне методе омогућавају недвосмислено утврђивање и квантификацију PCDD/PCDF и РСВ сличних диоксинима у узорку и пружају потпуне информације на основу конгенера. Стога, те методе омогућавају контролу прописаних максималних концентрација и нивоа / прагова за деловање, укључујући потврду резултата добијених методама скрининга. Осим тога, резултати се могу користити и у друге сврхе, као што су одређивање ниских нивоа присуства код мониторинга хране, праћење трендова, процена изложености популације и стварање базе података због могуће поновне процене нивоа / прагова за деловање и максималних концентрација. Оне су важне и за одређивање профила конгенера у сврху утврђивања извора могуће контаминације. Такве методе користе гасну хроматографију-масену спектрометрију високе резолуције (GС-HRMS). За потврђивање усаглашености или неусаглашености са прописаном максималном концентрацијом може се користити и гасна хроматографија-тандем масена спектрометрија (GС-МС/МС).
Б) ОБЈАШЊЕЊЕ
За израчунавање концентрација токсичних еквивалената (ТЕQ), концентрације појединачних супстанци у датом узорку помноже се са њиховим одговарајућим фактором еквивалентне токсичности (ТЕF) које је утврдила Светска здравствена организација и који су наведени у додатку дела 2. овог прилога, а затим се они саберу да би се добила укупна концентрација једињења сличних диоксинима изражених као ТЕQ.
Методе скрининга и потврдне методе могу се користити само за контролу одређеног матрикса, ако су довољно осетљиве да поуздано детектују нивое који достижу ниво прописане максималне концентрације или ниво / праг за деловање.
В) ЗАХТЕВИ ЗА ОСИГУРАЊЕ КВАЛИТЕТА
У свакој фази узорковања и испитивања предузимају се мере за спречавање унакрсне контаминације.
Узорци се складиште и транспортују у посудама од стакла, алуминијума, полипропилена или полиетилена које су погодне за складиштење и не утичу на количине PCDD/PCDF и РСВ сличних диоксинима у узорцима. Из посуда за узорке треба уклонити трагове папирне прашине.
Складиштење и транспорт се спроводе тако да се очува целовитост узорка хране.
Уколико је то потребно, сваки лабораторијски узорак треба фино самлети и темељно промешати, користећи поступак за који је доказано да постиже потпуну хомогенизацију (нпр. просејавањем самлевеног узорка кроз сито отвора 1 mm). Ако је садржај влаге у узорку превисок, узорак се пре млевења суши.
Од опште је важности, контрола реагенаса, стакленог прибора и опреме због могућег утицаја на резултате изражене у ТЕQ или ВЕQ.
Испитивање слепе пробе врши се спровођењем читавог аналитичког поступка, изостављајући само узорак.
За биоаналитичке методе је од велике важности да се све стаклене посуде и растварачи који се користе у испитивању тестирају на садржај једињења која ометају детекцију циљних једињења у радном опсегу. Стаклени прибор се испира растварачима и/или загрева на температурама које су погодне за уклањање трагова PCDD/PCDF, једињења сличних диоксинима и ометајућих једињења са његове површине.
Количина узорка за екстракцију треба да буде довољна да се испуне захтеви у погледу довољно ниског радног опсега, укључујући концентрације на нивоу прописане максималне концентрације или нивоа/прагова за деловање.
Посебни поступци припреме узорка, који се користе за производе који се разматрају, треба да буду у складу са међународно прихваћеним смерницама.
У случају рибе, треба уклонити кожу, јер су максималне концентрације прописане за мишић без коже. Међутим, потребно је пажљиво и потпуно састругати целокупно мишићно и масно ткиво које се налази са унутрашње стране коже и додати у узорак који се испитује.
Г) ЗАХТЕВИ ЗА ЛАБОРАТОРИЈЕ
Количина узорка за екстракцију треба да буде довољна да се испуне захтеви у погледу довољно ниског радног опсега, укључујући концентрације на нивоу прописане максималне концентрације или нивоа/прага за деловање.
Посебни поступци припреме узорка, који се користе за производе који се разматрају, треба да буду у складу са међународно прихваћеним смерницама.
У случају рибе, треба уклонити кожу, јер су максималне концентрације прописане за мишић без коже. Међутим, потребно је пажљиво и потпуно састругати целокупно мишићно и масно ткиво које се налази са унутрашње стране коже и додати у узорак који се испитује.
Д) ОСНОВНИ ЗАХТЕВИ ЗА АНАЛИТИЧКЕ ПОСТУПКЕ ЗА ДИОКСИНЕ (PCDD/PCDF) И РСВ СЛИЧНЕ ДИОКСИНИМА
Д.1. Висока осетљивост и ниска граница квантификације
За PCDD/PCDF, због екстремне токсичности неких од ових једињења, количине које се могу детектовати треба да буду реда величине неколико фемтограма (10–15 g). За већину РСВ конгенера довољна је граница квантификације у нанограмском опсегу (10–9 g). Међутим, за мерење токсичнијих конгенера РСВ сличних диоксинима (а посебно не-орто-супституисаних конгенера) доња граница радног опсега треба да буде испод пикограма (10–12 g).
Д.2. Висока селективност (специфичност)
Неопходно је разликовати PCDD/PCDF и РСВ сличне диоксинима и мноштво других вероватно ометајућих једињења, која су истовремено екстрахована из узорка и присутна у концентрацијама које су неколико редова величине веће од концентрација предметних аналита. Код метода гасне хроматографије/масене спектрометрије (GС-МС), неопходно је правити разлику између различитих конгенера, као што су токсични конгенери (нпр. седамнаест 2,3,7,8-супституисаних PCDD/PCDF и дванаест РСВ сличних диоксинима) и други конгенери.
Потребно је да се са биоаналитичким методама открију циљна једињења, као што су суме PCDD/PCDF и/или РСВ слични диоксинима. Пречишћавање узорка има за циљ уклањање једињења која изазивају лажно неусаглашене резултате или једињења која могу смањити одговор и проузроковати лажно усаглашене резултате.
Д.3. Висока тачност (истинитост и прецизност, експериментално измерен аналитички принос у биотесту)
Код метода гасне хроматографије/масене спектрометрије (GС-МС), одређивање треба да обезбеди валидну процену праве концентрације у узорку. Висока тачност (тачност мерења: подударност између резултата мерења и стварне или приписане вредности количине која се мери) потребна је да би се избегло одбијање резултата испитивања узорка на основу слабе поузданости утврђеног нивоа токсичних еквивалената (ТЕQ). Тачност се изражава као истинитост (разлика између измерене средње вредности за аналит у сертификованом материјалу и његове сертификоване вредности, изражене као проценат ове вредности) и прецизност (RSDR релативна стандардна девијација израчунана из резултата добијених под условима поновљивости).
За биоаналитичке методе треба да се утврди експериментално измерени аналитички принос у биотесту.
Д.4. Валидација у распону прописане максималне концентрације и опште мере за контролу квалитета
У току поступка валидације и/или рутинске анализе, лабораторије треба да докажу изводљивост методе, у одређеном распону близу прописане максималне концентрације, нпр. 0,5 пута, једном и два пута већом концентрацијом од прописане максималне концентрације, са прихватљивим коефицијентом варијације за поновљено испитивање.
Као мере интерне контроле квалитета спроводе се редовне слепе пробе и експерименти са обогаћивањем или испитивање контролних узорака (пожељан је сертификовани референтни материјал, ако је доступан). Да би се обезбедило да се испитивање спроводи у складу са захтевима, израђују се и проверавају табеле контроле квалитета (QС) за слепе пробе, експерименте са обогаћивањем или испитивање контролних узорака.
Д.5. Граница квантификације
За метод биоаналитичког скрининга, одређивање границе квантификације (LОQ) није од суштинског значаја, али је потребно доказати да метода може да разликује слепу вредност од граничне вредности (cut-off вредност). При одређивању вредности биоаналитичких еквивалената (ВЕQ), одређује се ниво извештавања за обраду узорака који дају одговор испод тог нивоа. Потребно је доказати да се ниво очитавања најмање троструко разликује од нивоа при процедурама са слепим узорцима, са одговором испод радног опсега. Стога се овај ниво израчунава из узорака који садрже циљна једињења близу захтеваног минималног нивоа, а не из односа између сигнала и шума (S/N) или из слепе пробе.
Граница квантификације (LОQ) за потврдну методу треба да буде око једне петине прописане максималне концентрације.
Д.6. Аналитички критеријуми
За поуздане резултате потврдних метода или метода скрининга треба да буду испуњени критеријуми наведени у табели испод у распону прописане максималне концентрације за вредности токсичних еквивалената (ТЕQ), односно вредности биоаналитичких еквивалената (ВЕQ), које се одређују као укупна вредност ТЕQ или укупна вредност ВЕQ (као сума PCDD/PCDF и/или РСВ сличних диоксинима), или одвојено за PCDD/PCDF и/или РСВ сличне диоксинима.
|
Биоаналитичке |
Потврдне методе |
|
|
Учесталост лажно усаглашених резултата(*) |
< 5% |
|
|
Истинитост |
– 20% дo + 20% |
|
|
Поновљивост (RSDr) |
< 20% |
|
|
Унутарлабораторијска репродуктивност (средња прецизност) (RSDR) |
< 25% |
< 15% |
|
(*) У односу на прописане максималне концентрације. |
||
Д.7. Посебни захтеви за методе скрининга
Могу се користити GC-MS методе и биоаналитичке методе. За GC-MS методе примењују се захеви прописани у одељку Ђ) део 2. овог прилога. За ћелијске биоаналитичке методе примењују се посебни захтеви прописани у одељку Е) део 2. овог прилога.
Лабораторије које спроводе методе скринингa за рутинску контролу узорака треба да успоставе блиску сарадњу са лабораторијима које спроводе потврдну методу.
У току рутинског испитивања потребно је спровести проверу изводљивости методе скринингa, и то аналитичком контролом квалитета и валидацијом методе. Програм за контролу усаглашених резултата се спроводи континуирано.
Провера могућег смањења ћелијског одговора и цитотоксичност
20% екстраката узорака се мери у рутинском скрининг прегледу без додавања супстанце ТСDD и са додавањем ТСDD у концентрацији која одговара прописаној максималној концентрацији или нивоу / прагу за деловање, да би се проверило да ли је одговор можда смањен због ометајућих супстанци присутних у екстракту узорка. Измерена концентрација обогаћеног узорка упоређује се са сумом концентрације необогаћеног екстракта и концентрације обогаћеног екстракта. Ако је та измерена концентрација за више од 25 % нижа од израчунате (суме) концентрације, то указује на могуће смањење сигнала и тај узорак треба подвргнути потврдном испитивању. Резултати се прате коришћењем табела контроле квалитета.
Контрола квалитета усаглашених узорака
У зависности од матрикса узорка и лабораторијског искуства, треба да буде потврђено од 2% до 10% усаглашених узорака.
Одређивање учесталости лажно усаглашених резултата на основу података контроле квалитета
Одређује се учесталост лажно усаглашених резултата испитивања узорака испод и изнад прописане максималне концентрације или нивоa / прагa за деловање. Стварна учесталост лажно усаглашених резултата треба да буде испод 5%. Након што се добије најмање 20 потврђених резултата за сваку матрицу/групу матрица из контроле квалитета усклађених узорака, на основу ове базе података се доносе закључци о учесталости лажно усаглашених резултата. Резултати узорака са распоном концентрација од, на пример, до 2 пута веће од прописане максималне концентрације, анализирани у теренским студијама или у инцидентима контаминације, такође могу бити укључени у најмање 20 резултата да би се проценио удео лажних резултата усаглашености. Узорци треба да покрију најчешће узорке конгенера који представљају различите изворе.
Иако су методе скринингa усмерене првенствено на откривање узорака који прелазе ниво/праг за деловање, критеријум за одређивање лажно усаглашених резултата јесте прописана максимална концентрација, узимајући у обзир проширену мерну несигурност потврдне методе.
Могући неусаглашени резултати из скрининга се увек проверавају потпуним поновљеним испитивањем оригиналног узорка потврдном методом. Ти узорци се могу користити и за процену учесталости лажно неусаглашених резултата. Код метода скрининга учесталост лажно неусаглашених резултата је део резултата за које је потврђено да су усаглашени потврдним испитивањем, док је претходним скринингом за узорак изражена сумња да није усаглашен. Међутим, процена предности методе скрининга заснива се на поређењу броја лажно неусаглашених резултата са укупним бројем проверених узорака. Та учесталост треба да буде довољно ниска да би коришћење методе скрининга било корисно.
Биоаналитичке методе треба да, барем под условима валидације, обезбеде валидну индикацију нивоа ТЕQ, израчунату и изражену као ВЕQ.
Поред тога, за биоаналитичке методе спроведене у условима поновљивости, интралабораторијска поновљивост RSDr је уобичајено нижа од RSDR у условима поновљивости.
Ђ) ПОСЕБНИ ЗАХТЕВИ КОЈЕ ТРЕБА ДА ИСПУЊАВАЈУ GC-MS МЕТОДЕ ЗА СКРИНИНГ ИЛИ ПОТВРДНЕ МЕТОДЕ
Ђ.1. Прихватљиве разлике између горње и доње границе нивоа WНО-ТЕQ
Разлика између горње и доње границе не може бити већа од 20% да би се потврдило прекорачење прописане максималне концентрације или у случају потребе прекорачења нивоа/прага за деловање.
Ђ.2. Контрола аналитичког приноса
Додавање 13С-означених 2,3,7,8-хлор-супституисаних унутраш-њих стандарда за PCDD/PCDF и 13С-означених унутрашњих стандарда за РСВ сличне диоксинима потребно је спровести на самом почетку аналитичке методе, на пример пре екстракције, како би се вредновао аналитички поступак. Додаје се најмање по један конгенер за све тетра до окта-хлороване хомологне групе за PCDD/PCDF и најмање по један конгенер за сваку хомологну групу за РСВ сличне диоксинима (односно најмање по један конгенер за сваки изабрани јон у спектрометрији маса која се користи за праћење PCDD/PCDF односно РСВ сличних диоксинима). У случају потврдних метода користи се свих седамнаест 13С-означених 2,3,7,8-супституисаних унутрашњих стандарда за PCDD/PCDF-ове и свих дванаест 13С-означених унутрашњих стандарда за РСВ сличне диоксинима.
Релативне факторе одговора треба утврдити и за оне конгенере за које се не додаје ни један 13С-означен аналог, тако што ће се користити одговарајући калибрациони раствори.
За храну биљног и животињског порекла која садржи мање од 10% масти, пре екстракције обавезно се додају интерни стандарди. За храну животињског порекла у којој је удео масти већи од 10%, интерни стандарди се могу додати пре или после екстракције масти. Треба да се спроведе одговарајуће вредновање ефективности екстракције, што зависи од фазе када се додају интерни стандарди и да ли се резултати исказују на основу производа или масти.
Пре GC-MS испитивања треба додати један или два (сурогат) стандарда ради провере аналитичког приноса.
Потребно је контролисати аналитички принос. За потврдне методе, аналитички принос појединачних интерних стандарда треба да буде у распону између 60% и 120%. Мањи или већи аналитички принос за појединачне конгенере, а посебно за неке хепта– и окта-хлороване дибензо-р-диоксине и дибензофуране, прихватљив је под условом да је њихов допринос ТЕQ вредности мањи од 10% укупне ТЕQ вредности (добијене на основу суме PCDD/PCDF и РСВ сличних диоксинима). За GC-MS методе скрининга аналитички принос треба да буде у распону између 30% и 140%.
Ђ.3. Уклањање ометајућих супстанци
Одвајање PCDD/PCDF од ометајућих хлорованих једињења, као што су РСВ који нису слични диоксинима и хлоровани дифенил етри, спроводи се помоћу одговарајућих хроматографских техника (најбоље уз помоћ колоне са флорисилом, алуминијум оксидом и/или активним угљем).
Раздвајање изомера гасном хроматографијом треба да буде задовољавајуће (< 25% између два пика 1,2,3,4,7,8-HxCDF и 1,2,3,6,7,8-HxCDF).
Ђ.4. Калибрација са стандардном кривом
Распон калибрационе криве треба да обухвати релевантни распон прописаних максималних концентрација или нивоа/прагова за деловање.
Ђ.5. Посебни захтеви за потврдне методе
За GC-HRMS:
У HRMS-у резолуција је типично ≥ 10.000 за цео масени распон при 10% најмањег размака између два пика једнаког интензитета.
Испуњавање даљих критеријума за идентификацију и потврђивање како су наведени у међународно признатим стандардима, на пример у стандарду SRPS ЕN 16215:2020 (Храна за животиње – Методе узимања узорака – Одређивање диоксина и диоксинима сличних РСВ и индикаторских РСВ помоћу GC-HRMS) и/или у методама ЕРА 1613 и 1668, како су ревидиране.
За GC-MS/MS:
Праћење барем два специфична прекурсор јона, сваког са једним посебним одговарајућим прелазним јоном производа за све означене и неозначене аналите у оквиру испитивања.
Максимална дозвољена толеранција релативних интензитета јона од ± 15% за одабране транзиционе јоне производа у поређењу са израчунатим или измереним вредностима (просек стандарда калибрације), применом идентичних услова MS/MS, посебно енергије судара и притиска колизионог гаса за сваки прелаз датог аналита.
Разлагање за сваки квадропол треба поставити једнако или боље од јединичног масеног разлагања (јединично масено разлагање: разлагање које је довољно да раздвоји два пика за једну масену јединицу) како би се смањила могућа међуделовања (интерференције) предметних аналита.
Испуњавање даљих захтева како су наведени у међународно признатим стандардима, на пример у стандарду SRPS ЕN 16215:2020 (Храна за животиње – Методе узимања узорака – Одређивање диоксина и диоксинима сличних РСВ и индикаторских РСВ помоћу GC-HRMS) и/или у методама ЕРА 1613 и 1668, како су ревидиране, осим обавезе да се користи GC/HRMS.
Е) ПОСЕБНИ ЗАХТЕВИ ЗА БИОАНАЛИТИЧКЕ МЕТОДЕ
Биоаналитичке методе су методе које се заснивају на коришћењу биолошких начела као што су тестови на ћелијској основи, тестови на основу рецептора или имунолошки тестови. У овом одељку прописују се општи захтеви за биоаналитичке методе.
Методом скрининга се у начелу узорак класификује као усаглашен или као лажно неусаглашен узорак. У ту сврху, израчуната вредност ВЕQ упоређује се са граничном вредношћу из одељка Е) пододељак Е.3. део 2. овог прилога. Узорци испод граничне вредности сматрају се усаглашеним. За узорке који су једнаки граничним вредностима или изнад њих сумња се да нису усаглашени, што захтева испитивање потврдном методом. У пракси, ВЕQ вредност која одговара двема трећинама прописане максималне концентрације, може се користити као најпримеренија гранична вредност, под условом да се обезбеди учесталост лажно усаглашених резултата < 5% и прихватљива учесталост лажно неусаглашених резултата. Са различитим прописаним максималним концентрацијама за PCDD/PCDF и за суму PCDD/PCDF и РСВ сличних диоксинима, провера усаглашености узорака без фракционисања захтева да биолошки тест има одговарајуће граничне вредности за PCDD/PCDF За проверу узорака који прелазе нивое/прагове за деловање, одговарајући проценат датог нивоа/прага за деловање може се користити као гранична вредност.
Ако је оквирна вредност изражена у ВЕQ, резултати из узорка наводе се у радном распону и прекорачују границу извештавања, како је наведено у тач. Е.1.1. и Е.1.6. пододељак Е.1. одељак Е) део 2. овог прилога.
Е.1. Процена одговора на испитивање
Е.1.1. Општи захтеви
Када се концентрације израчунавају из калибрационе криве за ТСDD, вредности на горњем крају криве показују велике варијације (висок коефицијент варијације (СV)). Радни опсег је опсег у коме је СV мањи од 15%. Доња граница радног опсега (праг извештавања) поставља се знатно изнад нивоа поступка слепе пробе (најмање три пута више). Горња граница радног опсега обично представља вредност ЕС70 (70% највеће ефективне концентрације), али је нижи ако је СV у том опсегу већи од 15%. Радни опсег се одређује у току валидације. Граничне вредности како су прописане у одељку Е) пододељак Е.3. део 2. овог прилога треба да буду унутар радног опсега.
Стандардни раствори и екстракти узорака испитују се троструком или барем двоструком анализом. Када се употребљавају двоструке анализе, стандардни раствори или екстракти контролних узорака испитани у четири до шест јама распоређених по плочици показују одговор или концентрацију (могуће само у радном опсегу) на основу СV < 15%.
Е.1.2. Калибрација
Е.1.2.1. Калибрација са стандардном кривом
Нивои у узорцима се могу проценити поређењем одговора на испитивање са калибрационом кривом ТСDD (или РСВ 126 или стандардна мешавина PCDD/PCDF/РСВ сличних диоксинима) за израчунавање ВЕQ вредности у екстракту и касније у узорку.
Калибрациона крива садржи осам до 12 концентрација (барем у дупликату) са довољно концентрација у доњем делу криве (радни распон). Посебну пажњу треба обратити на квалитет подударности криве у радном распону. У процени степена усаглашености у нелинеарној регресији, вредност R2 као таква има мало или никакво значење. Боља подударност постиже се смањивањем разлике између израчунатих и посматраних нивоа у радном распону криве (нпр. смањивањем суме квадрата резидуа).
Процењена вредност у eкстракту узорка се затим коригује за вредност ВЕQ, израчунату за слепи узорак матрице или растварача (како би се узеле у обзир нечистоће из употребљених растварача и хемикалија) и за експериментално мерен аналитички принос (израчуната из ВЕQ вредности одговарајућих референтних узорака са репрезентативним профилима конгенера близу прописане максималне концентрације или нивоа/прага за деловање). Да би се извршила корекција аналитичког приноса, експериментално измерени аналитички принос треба увек да буде у траженом распону, како је прописано у делу 2. одељак Е) пододељак Е.1. тачка Е.1.4. овог прилога. Референтни узорци коришћени за корекцију аналитичког приноса треба да испуњавају захтеве из дела 2. одељак Е) пододељак Е.2. овог прилога.
Е.1.2.2. Калибрација са референтним узорцима
Друга могућност је да се употреби калибрациона крива припремљена из барем четири референтна узорка, како је наведено у делу 2. одељак Е пододељак Е.2. овог прилога: једна слепа проба и три референтна узорка са 0,5 пута, 1 пут и 2 пута већом вредношћу од прописане максималне концентрације или нивоа/прага за деловање, због чега корекција вредности слепих проба и аналитичког приноса више није потребна ако својства матрице референтних узорака одговарају непознатим узорцима. У овом случају, одговор теста који одговара двема трећинама прописане максималне концентрације, како је наведено у делу 2. одељак Е) пододељак Е.3. овог прилога, може се израчунати непосредно из тих узорака и користити као гранична вредност. За проверу узорака који прелазе нивое/прагове за деловање, гранична вредност може бити одговарајући проценат ових нивоа/прагова за деловање.
Е.1.3. Одвојено одређивање PCDD/PCDF и РСВ сличних диоксинима
Изолати се могу поделити у фракције које садрже PCDD/PCDF и РСВ сличне диоксинима, које омогућавају одвојено исказивање вредности ТЕQ за PCDD/PCDF и РСВ сличне диоксинима (у ВЕQ). По могућности, користи се стандардна калибрациона крива РСВ 126 за процену резултата за фракцију која садржи РСВ сличне диоксинима.
Е.1.4. Eкспериментално мерен аналитички принос при биолошким тестовима
Eкспериментално мерен аналитички принос израчунава се из одговарајућих референтних узорака са репрезентативним узорцима конгенера око прописане максималне концентрације или нивоа/прагова за деловање и изражава се као проценат вредности ВЕQ у поређењу са вредношћу ТЕQ. У зависности од врсте испитивања и коришћених ТЕF50, разлике између фактора ТЕF и RЕР за РСВ сличне диоксинима могу проузроковати мањи експериментално мерен аналитички принос за РСВ сличне диоксинима у поређењу са PCDD/PCDF. Због тога, ако се спроводи одвојено одређивање PCDD/PCDF и РСВ сличних диоксинима, експериментално мерен аналитички принос при биолошким тестовима износи: за РСВ сличне диоксинима од 20% до 60%, а за PCDD/PCDF од 50% до 130% (распони важе за ТCDD калибрациону криву). Будући да допринос РСВ сличних диоксинима суми PCDD/PCDF и РСВ сличних диоксинима може варирати код различитих матрица и узорака, експериментално мерен аналитички принос при биолошким тестовима за параметар суме одражава те распоне и биће између 30% и 130%.
Е.1.5. Контрола аналитичког приноса при пречишћавању
Губитак једињења у току пречишћавања проверава се током валидације. Слепа проба са додатком мешавине различитих конгенера подвргава се пречишћавању (најмање n = 3), а принос и варијабилност се проверавају потврдном методом. Принос треба
––––––––
50 Тренутни захтеви заснивају се на ТЕF објављенима у: M. Van den Berg et al, Toxicol Sci 93 (2), 223.–241. (2006.).
да износи од 60% до 120%, нарочито за конгенере који доприносе више од 10% вредности ТЕQ у различитим мешавинама.
Е.1.6. Граница за извештавање
За извештавање о вредностима ВЕQ, граница за извештавање одређује се на основу одговарајућих узорака матрица који укључују типичне узорке конгенера, али не на основу калибрациионе криве стандарда због ниске прецизности у доњем распону криве. У обзир треба да се узму ефекти екстракције и пречишћавања. Граница за извештавање треба да се одреди значајно изнад поступка са слепим узорцима (најмање три пута више).
Е.2. Коришћење референтних узорака
Референтни узорци представљају узорке матрица, узорке конгенера и распоне концентрација за PCDD/PCDF и РСВ сличне диоксинима око прописане максималне концентрације или нивоа/прага за деловање.
Уз сваку серију узорака која се испитује треба да се укључи једна слепа проба или по могућности слепа матрица и један референтни узорак са прописаном максималном концентрацијом или на нивоу/прагу за деловање. Ови узорци се екстрахују и испитују истовремено у истим условима. Референтни узорак треба да покаже много јаснији одговор од слепог узорка, чиме се осигурава примереност теста. Ти узорци се могу користити за корекцију слепе пробе и аналитичког приноса.
Референтни узорци одабрани за корекцију аналитичког приноса треба да буду репрезентативни за испитиване узорке, што значи да модели конгенера не смеју да доведу до потцењивања нивоа.
Приликом провере прописане максималне концентрације или нивоа/прага за деловање могу се укључити додатни референтни узорци са вредностима које су, на пример, 0,5 и 2 пута веће од прописане максималне концентрације или нивоа/прага за деловање, како би се утврдила ефикасност испитивања у значајном распону. У комбинацији, ови узорци се могу користити за израчунавање нивоа ВЕQ у тестним узорцима, како је наведено у подтачки Е.1.2.2. овог прилога.
E.3. Одређивање граничних вредности
Треба успоставити корелацију између биоаналитичких резултата изражених у ВЕQ и резултата метода потврђивања изражених у ТЕQ (нпр. експериментима калибрације подударних матрица у којима се узима у обзир утицај матрице на калибрационе линије и који укључују референтне узорке обогаћене да достигну 0, 0,5, 1 и 2 пута прописану максималну концентрацију са шест понављања на сваком нивоу (n = 24). Корекциони фактори (за слепу пробу и аналитички принос) могу се проценити из овог односа, али треба да се провере за сваку серију испитивања, укључивањем поступака са слепим пробама или слепе пробе матрица, као и узорака за аналитички принос у складу са пододељком Е.2. одељак Е) овог прилога.
Граничне вредности одређују се за доношење одлуке о усаглашености узорка са прописаним максималним концентрацијама или за контролу нивоа/прага за деловање, ако је релевантно, с обзиром на дату прописану максималну концентрацију или ниво/праг за деловање одређене посебно за PCDD/PCDF и РСВ сличне диоксинима или за суму PCDD/PCDF и РСВ сличних диоксинима. Приказује их доња крајња тачка дистрибуције биоаналитичких резултата (кориговано за вредност слепе пробе и за аналитички принос), што одговара одлучујућој (критичној) граници потврдне методе на основу нивоа поузданости од 95%, што подразумева да је удео лажно усаглашених резултата < 5%, и на основу RSDR < 25%. Одлучујућа (критична) граница потврдне методе је прописана максимална концентрација, узимајући у обзир проширену мерну несигурност.
У пракси, гранична вредност (у ВЕQ) се може израчунати на следећи начин (видети слику 1):
Е.3.1. Коришћење доње границе 95%-тног интервала поузданости на одлучујућој (критичној) граници потврдне методе
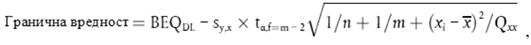
где је:
BEQDL = ВЕQ који одговара одлучујућој (критичној) граници потврдне методе, која је једнака прописаној максималној концентрацији, узимајући у обзир проширену мерну несигурност;
sy,x = стандардна девијација резидуа;
tα,f = m – 2 = студент фактор (α = 5%, f = степени слободе, једнострани);
m =– укупан број калибрацијских тачки (индекс ј);
n = број понављања на сваком нивоу;
xi = концентрација узорка (у TEQ) калибрационе тачке i одређене потврдном методом;
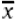 = средња вредност концентрација (у TEQ) свих калибрисаних узорака;
= средња вредност концентрација (у TEQ) свих калибрисаних узорака;
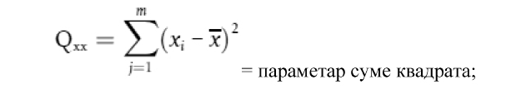
i = индекс за калибрациону тачку i.
Е.3.2. Израчунавање засновано на биоаналитичким резултатима
Израчунавање засновано на биоаналитичким резултатима (кориговано за вредност слепе пробе и за aналитички принос) из више анализа узорака (n ≥ 6) контаминираних на одлучујућој (критичној) граници потврдне методе, као доња крајња тачка дистрибуције података при одговарајућој средњој ВЕQ вредности:
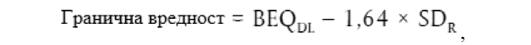
где је: SDR = стандардна девијација резултата биоаналитичких тестова при BEQDL, измерено у условима унутарлабораторијске поновљивости.
E.3.3. Израчунавање као средња вредност биоаналитичких резултата
Израчунавање као средња вредност биоаналитичких резултата (изражено у ВЕQ, кориговано за вредност слепе пробе и за aналитички принос) више анализа узорака (n ≥ 6) контаминираних на две трећине прописане максималне концентрације или нивоа/прага за деловање. Ово је на основу запажања да ће вредност бити око граничних вредности прописаних у одељку Е) пододељак Е.3 тач. Е.3.1. или Е.3.2. овог прилога.
Израчунавање граничне вредности на основу нивоа поузданости од 95%, што значи да је удео лажно усаглашених резултата < 5% и на основу RSDR < 25%:
из доње границе 95 %-тног интервала поузданости на одлучујућој (критичној) граници потврдне методе;
из вишеструких анализа узорака (n ≥ 6) контаминираних на одлучујућој (критичној) граници потврдне методе као доња крајња тачка дистрибуције података (на слици 1. представљена звонастом кривом) при одговарајућој средњој ВЕQ вредности.
Е.3.4. Ограничавање граничних вредности
Граничне вредности засноване на ВЕQ, које су израчунате из RSDR постигнуте током валидације коришћењем ограниченог број узорака из различитих матрица/профила конгенера, могу бити веће од прописане максималне концентрације или нивоа/прагова за деловање, на основу вредности ТЕQ због веће поузданости него што се може постићи у рутинским анализама када се мора пратити непознати спектар могућих профила конгенера. У таквим случајевима, граничне вредности се израчунавају из RSDR = 25%, или, пожељно, две трећине прописане максималне концентрације или нивоа/прага за деловање.
Е.4. Карактеристике изводљивости
С обзиром на то да се у биоаналитичким методама не могу користити интерни стандарди, спроводе се испитивања поновљивости како би се добили подаци о стандардној девијацији унутар и између серија испитивања. Поновљивост је < 20%, а интерна лабораторијска поновљивост мања од 25%. То се заснива и на нивоима израчунатим у ВЕQ након корекције за вредност слепе пробе и за aналитички принос.
Слика 1.
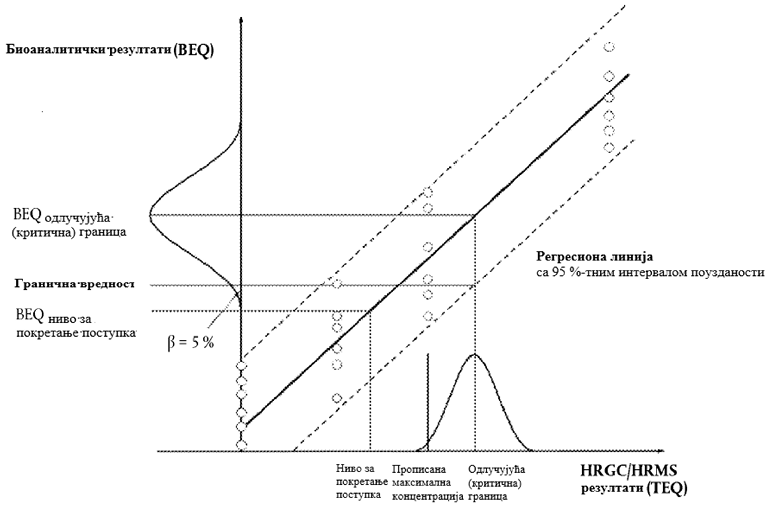
У поступку валидације доказује се да тест прави разлику између слепе пробе и нивоа граничне вредности омогућавајући идентификацију узорака изнад одговарајуће граничне вредности како је наведена у у тачки Е.1.2. пододељак Е.1. одељак Е) овог прилога.
Утврђују се циљна једињења, могуће интерференције и максимални нивои за слепе пробе.
Процентуална стандардна девијација у одговору или у концентрацији израчуната из одговора (могуће само у радном опсегу) при троструком одређивању естракта узорка не треба да буде изнад 15 %.
Некориговани резултати референтног/референтних узорака изражени у ВЕQ (вредност слепе пробе и при прописаној максималној концентрацији или нивоу/прагу за деловање) користе се за оцену изводљивости биоаналитичке методе у току континуираног временског периода.
Дијаграми контроле квалитете (QС) за поступке са слепим пробама и свака врста референтног узорка се евидентирају и проверавају како би се осигурало да је изводљивост анализа у складу са захтевима, посебно за поступак са слипим узорцима у погледу захтеване најмање разлике до доњег дела радног опсега и за референтне узорке у погледу унутарлабораторијске обновљивости. Поступке са слепим пробама потребно је добро контролисати како би се избегли лажно усаглашени резултати у одбитку.
Резултати анализа потврдним методама сумњивих узорака и од 2% до 10% усаглашених узорака (најмање 20 узорака по матрици) прикупљају се и користе за процену изводљивости методе скрининга и односа између ВЕQ и ТЕQ. Ова база података може се користити за поновљену евалуацију грничних вредности које се примењују на рутинске узорке за валидиране матрице.
Успешна изводљивост методе може се доказати и прстенастим тестовима. Резултати узорака анализираних у прстенастим тестовима који покривају распон концентрација до 2 пута већу од прописане максималне концентрације, такође могу бити део процене учесталости лажно усаглашних резултата, ако лабораторија може да докаже успешну изводљивост. Узорци покривају најчешће профиле конгенера, који представљају различите изворе.
У току инцидената граничне вредности се могу поново проценити, узимајући у обзир посебне узорке матрица и конгенера који се појављују у том инциденту.
Ж) ИЗВЕШТАВАЊЕ О РЕЗУЛТАТИМА
Ж.1. Потврдне методе
Аналитички резултати треба да садрже количине појединачних PCDD/PCDF и конгенера РСВ сличних диоксинима, а о вредностима се извештава као о доњим, горњим или средњим, како би се у извештај укључило што више података о резултатима и на тај начин омогућило тумачење резултата према посебним захтевима.
У извештај је потребно укључити и методу која се користи за екстракцију PCDD/PCDF, РСВ сличних диоксинима и масти. Удео масти у узорку одређује се и исказује за матрице хране са прописаним максималним концентрацијама израженим на основу масти и са очекиваном концентрацијом масти у распону од 0% до 2% (у складу са постојећим законодавством). За друге узорке одређивање удела масти није обавезно.
Аналитички приноси појединих интерних стандарда се наводе у случају да су изван распона наведеног у одељку Ђ) пододељак Ђ.2. овог прилога, у случају да је добијени резултат већи од прописане максималне концентрације ( у овом случају аналитички принос за једну или две поновљене анализе), а у другим случајевима на захтев.
С обзиром на то да проширену мерну несигурност треба узети у обзир при одлуци о усаглашености узорка, потребно је навести и тај параметар. Стога се аналитички резултати приказују као x +/– U, при чему је x аналитички резултат, а U је проширена мерна несигурност, добијена коришћењем фактора покривености 2, чиме се добија ниво поузданости од приближно 95%. У случају када се PCDD/PCDF и РСВ слични диоксинима одређују одвојено, тада се сума процењене проширене несигурности за појединачне аналитичке резултате PCDD/PCDF и РСВ сличних диоксинима користи за суму PCDD/PCDF и РСВ сличних диоксинима.
Резултати се изражавају у истим јединицама и заокружују се на исти број битних децималних места као и прописане максималне концентрације.
Ж.2. Биоаналитичке методе скрининга
Резултат методе скрининга изражава се као усаглашен или се за њега сумња да је неусаглашен („сумњив”).
Осим тога, оквирни резултат за PCDD/PCDF и/или РСВ сличне диоксинима може се изразити у ВЕQ (не ТЕQ), како је наведено у делу 2. одељак А) овог прилога. За узорке сa одговором испод границе извештавања наводи се да су испод границе извештавања. За узорке са одговором изнад радног опсега наводи се да прелазе радни опсег и ниво који одговара горњем делу радног опсега наводи се у ВЕQ.
У извештају се, за сваку врсту узорка матрице, наводи прописана максимална концентрација или ниво/праг за деловање на којима се процена заснива.
У извештају се наводи врста испитивања која се користи, основно начело испитивања и врста калибрације.
У извештај је потребно укључити и методу која се користи за екстракцију PCDD/PCDF, РСВ сличних диоксинима и масти. Удео масти у узорку утврђује се и исказује за матрице хране са прописаним максималним концентрацијама израженим на основу масти и са очекиваном концентрацијом масти у распону од 0% до 2% (у складу са постојећим законодавством). За друге узорке одређивање удела масти није обавезно.
У случају узорака за које се сумња да нису усаглашени, извештај укључује напомену о поступку који треба предузети. Концентрација PCDD/PCDF и сума PCDD/PCDF и РСВ сличних диоксинима у тим узорцима са повећаним нивоима утврђује се потврдном методом.
Неусаглашни резултати се наводе само из потврдне анализе.
Ж.3. Физичко-хемијске методе скрининга
Резултат методе скрининга изражава се као усаглашен или се за њега сумња да је неусаглашен („сумњив”).
У извештају се, за сваку врсту узорка матрице, наводи прописана максимална концентрација или ниво/праг за деловање на којима се процена заснива.
Осим тога, могу се навести нивои за поједине PCDD/PCDF и/или конгенере РСВ сличних диоксинима као и вредности ТЕQ изражене као доње, горње и средње. Резултати се изражавају у истим јединицама и заокружују се (барем) на исти број битних децималних места као и прописане максималне концентрације.
Аналитички приноси појединих интерних стандарда се наводе у случају да су изван распона наведеног у одељку Ђ) пододељак Ђ.2. овог прилога, а у другим случајевима на захтев.
У извештају се наводи примењена GC-MS метода.
У извештај треба укључити и методу која се користи за екстракцију PCDD/PCDF, РСВ сличних диоксинима и масти. Удео масти у узорку утврђује се и исказује за матрице хране са прописаним максималним концентрацијама израженим на основу масти и са очекиваном концентрацијом масти у распону од 0 до 2% (у складу са постојећим законодавством). За друге узорке одређивање удела масти није обавезно.
У случају узорака за које се сумња да нису усаглашени, извештај укључује напомену о поступку који треба спровести. Концентрација PCDD/PCDF и сума PCDD/PCDF и РСВ сличних диоксинима у тим узорцима са повећаним нивоима утврђује се потврдном методом.
О неусаглашности се може одлучити само након потврдне анализе.
Додатак
WHО-ТЕF за процену ризика за здравље људи заснована је на закључцима заседања Међународноg програмa о безбедности хемикалија (International Programme on Chemical Safety) Светскe здравственe организацијe, одржаног у Женеви јуна 2005. године51.
––––––––
51 Тренутни захтеви заснивају се на ТЕF објављенима у: M. Van den Berg et al, Toxicol Sci 93 (2), 223–241. (2006.).
|
Конгенер |
TEF вредност |
Конгенер |
TEF вредност |
|
Dibenzo-p-dioksini (PCDD): 2,3,7,8-TCDD 1,2,3,7,8-PeCDD 1,2,3,4,7,8-HxCDD 1,2,3,6,7,8-HxCDD 1,2,3,7,8,9-HxCDD 1,2,3,4,6,7,8-HpCDD OCDD |
1 1 0,1 0,1 0,1 0,01 0,0003 |
PCB слични диоксинима: Не orto PCB + mono-orto PCB: Не orto PCB: PCB 77 PCB 81 PCB126 PCB 169 |
0,0001 0,0003 0,1 0,03 |
|
Dibenzofurani (PCDF): 2,3,7,8-TCDF 1,2,3,7,8-PeCDF 2,3,4,7,8-PeCDF 1,2,3,4,7,8-HxCDF 1,2,3,6,7,8-HxCDF 1,2,3,7,8,9-HxCDF 2,3,4,6,7,8-HxCDF 1,2,3,4,6,7,8-HpCDF 1,2,3,4,7,8,9-HpCDF OCDF |
0,1 0,03 0,3 0,1 0,1 0,1 0,1 0,01 0,01 0,0003 |
Mono-orto PCB: PCB 105 PCB 114 PCB 118 PCB 123 PCB 156 PCB 157 PCB 167 PCB 189 |
0,0003 0,0003 0,0003 0,0003 0,0003 0,0003 0,0003 0,0003 |
|
Коришћене скраћенице: „Т” = тетра; „Pе” = пента; „Hh” = хекса; „Hp” = хепта; „О” = окта; „CDD” = хлордибензодиоксин, „CDF” = хлордибензофуран, „CB” = хлоробифенил. |
|||
3. ПРИПРЕМА УЗОРКА И ЗАХТЕВИ ЗА МЕТОДЕ ИСПИТИВАЊА КОЈЕ СЕ КОРИСТЕ ЗА СЛУЖБЕНУ КОНТРОЛУ НИВОА РСВ КОЈИ НИСУ СЛИЧНИ ДИОКСИНИМА У ОДРЕЂЕНОЈ ХРАНИ
Захтеви из овог дела примењују се кад се испитује храна за службену контролу количина РСВ који нису слични диоксинима и у погледу приреме узорака и аналитичких захтева за друге регулаторне сврхе, укључујући контроле које спроводи субјект у пословању храном ради обезбеђења усклађености са одредбама посебног прописа о хигијени хране.
Одредбе о припреми узорка из дела 2. одељак В) овог прилога применљиве су и на контролу количина РСВ који нису слични диоксинима у храни.
А) МЕТОДЕ ДЕТЕКЦИЈЕ КОЈЕ СЕ КОРИСТЕ
Користи се гасна хроматографија са различитим детекторима (GC-ECD), GC-LRMS, GC-MS/MS, GC-HRMS или еквивалентне методе.
Б) ИДЕНТИФИКАЦИЈА И ПОТВРДА РЕЛЕВАНТНИХ АНАЛИТА
Релативно ретенционо време у односу на интерне стандарде или референтне стандарде (прихваћена девијација од +/– 0,25%).
Раздвајање РСВ који нису слични диоксинима гасном хроматографијом (раздвајање од ометајућих супстанци, нарочито ко-елуираних РСВ, а посебно ако су концентрације у узорцима у распону законски дозвољених граница и неусаглашеност се мора потврдити52).
За технике GC-MS: Праћење најмање следећег броја молекуларних јона или карактеристичних јона из молекуларног кластера:
– два специфична јона за HRMS;
– три специфична јона за LRMS;
– два специфична јонска прекурсора, сваки са посебним јоном прелазног производа за MS-MS.
Највећа дозвољена одступања за однос заступљености одабраних масених фрагмената: Релативна девијација односа заступљености
––––––––
52 Конгенери за које је често установљено да ко-елуирају су нпр. PCB 28/31, PCB 52/69 и PCB 138/163/164. За GC/MS такође треба узети у обзир могуће сметње узроковане фрагментима конгенера са већим садржајем хлора.
одабраних масених фрагмената у односу на теоретску заступљеност или калибрациони стандард за циљни јон (праћени јон са највећом заступљеношћу) и потврдни јон/потврдне јоне: ± 15%.
За технике GC-ECD: Потврда резултата који прелазе прописане максималне концентрације са две GC колоне са стационарним фазама различитог поларитета.
В) ДОКАЗИВАЊЕ ЕФИКАСНОСТИ МЕТОДЕ
Валидација у распону прописанe максималнe концентрацијe (0,5 до 2 пута више од прописанe максималнe концентрацијe) сa прихватљивим коефицијентом варијације за поновљене анализе, како је наведено у захтевима за средњу прецизност у одељку Ж) део 3. овог прилога.
Г) ГРАНИЦА КВАНТИФИКАЦИЈЕ
Сума LOQ53 РСВ који нису слични диоксинима не треба да буде већа од једне трећине прописанe максималнe концентрацијe54.
Д) КОНТРОЛА КВАЛИТЕТA
Редовне слепе пробе, анализе узорака са додатком референтног материјала, анализе узорака за контролу квалитета, учешће у међулабораторијским студијама са релевантним матрицама узорака.
Ђ) КОНТРОЛА АНАЛИТИЧКОГ ПРИНОСА
Коришћење примерених интерних стандарда са физичко-хемијским својствима који одговарају предметним аналитима.
Додавање интерних стандарда:
– додавање производима (пре екстракције и поступка пречишћавања);
– могуће је додавање екстрахованој масти (пре поступка пречишћавања), ако се прописанe максималнe концентрацијe утврђују на основу масти.
Захтеви за методе у којима се користи свих шест изотопски обележених конгенера РСВ који нису слични диоксинима:
– корекција резултата за аналитички принос интерних стандарда;
– опште прихватљив аналитички принос изотопски обележених интерних стандарда је између 60% и 120%;
– нижи или виши аналитички приноси су прихватљиви за појединачне конгенере у којима је удео суме РСВ који нису слични диоксинима мањи од 10%.
Захтеви за методе у којима се не користи свих шест изотопски обележених интерних стандарда или се користе други интерни стандарди:
– контрола аналитичког приноса интерног/интерних стандарда за сваки узорак;
– прихватљиви аналитички приноси интерног/интерних стандарда између 60% и 120%;
– корекција резултата за аналитичке приносе интерних стандарда.
Аналитички приноси неозначених конгенера проверавају се анализом узорака са додатком референтног материјала или контролних узорака са концентрацијама у распону прописанe максималнe концентрацијe. Прихватљиви аналитички приноси за те конгенере су између 60% и 120%.
Е) ЗАХТЕВИ ЗА ЛАБОРАТОРИЈЕ
Лабораторије се акредититују у складу са стандардом SRPS ISO/IEC 17025 – Општи захтеви за компетентност лабораторија за испитивање и лабораторија за еталонирање. Поред тога, тамо где је применљиво, прате се начела описана у техничким смерницама за процену мерне несигурности и граница квантификације за потребе РСВ анализe55.
––––––––
53 Тамо где је то применљиво, треба поштовати принципе наведене у Смерницама за процену LOD и LOQ за мерења у области контаминената у храни и храни за животиње (Guidance Document on the Estimation of LOD and LOQ for Measurements in the Field of Contaminants in Feed and Food)
54 Изразито се препоручује да удео нивоа реагенса у слепој проби буде што нижи у односу на ниво контаминента у узорку. Лабораторија је одговорна за контролу варијација нивоа вредности слепих проба, нарочито ако су те вредности одузете.
55 Guidance Document on Measurement Uncertainty for Laboratories performing PCDD/F and PCB Analysis using Isotope Dilution Mass Spectrometry, Guidance Document on the Estimation of LOD and LOQ for Measurements in the Field of Contaminants in Feed and Food
Ж) КАРАКТЕРИСТИКЕ ЗА ЕФЕКТИВНОСТ
Критеријуми за суму РСВ који нису слични диоксинима при прописаној максималној концентрацији
|
Разређивање изотопа – масена спектрометрија(*) |
Остале технике |
|
|
Истинитост |
– 20 дo + 20 % |
– 30 дo + 30 % |
|
Репродуктивност (Средња прецизност) (RSDR) |
≤ 15 % |
≤ 20 % |
|
Разлика између израчунавања горње и доње границе |
≤ 20 % |
≤ 20 % |
|
(*) Коришћење свих шест 13С-означених аналога према захтевима интерних стандарда. |
||
З) ИЗВЕШТАВАЊЕ О РЕЗУЛТАТИМА
Аналитички резултати садрже нивое појединачних конгенера РСВ који нису слични диоксинима и суму РСВ који нису слични диоксинима и наводе се као доња, горња или средња граница, како би се у извештај укључило што више информација о резултатима и на тај начин омогућило тумачење резултата у складу са посебним захтевима.
У извештај је потребно укључити и методу која се користи за екстракцију РСВ и масти. Удео масти у узорку утврђује се и исказује за узорке хране са прописаним максималним концентрацијама израженим на основу масти и са очекиваном концентрацијом масти у распону од 0% до 2% (у складу са постојећим законодавством). За друге узорке одређивање удела масти није обавезно.
Аналитички приноси појединих интерних стандарда се наводе у случају да су изван распона наведеног у одељку Д) део 2. овог прилога, када је премашена прописана максимална концентрација, а у другим случајевима на захтев.
С обзиром да проширену мерну несигурност треба узети у обзир при одлуци о усаглашености узорка, потребно је навести и тај параметар. Стога се аналитички резултати приказују као x +/– U, при чему је x аналитички резултат, а U је проширена мерна несигурност, добијена коришћењем фактора покривености 2, чиме се добија ниво поузданости од приближно 95%.
Резултати се изражавају у истим јединицама и заокружују се на исти број битних децималних места као и прописане максималне концентрације.
ПРИЛОГ 5
МЕТОДЕ УЗОРКОВАЊА И ИСПИТИВАЊА УЗОРАКА ХРАНЕ ЗА СЛУЖБЕНУ КОНТРОЛУ НИВОА ЕРУКА КИСЕЛИНЕ56
А) ДЕФИНИЦИЈЕ
Примењују се дефиниције из Прилога 1. одељак А) овог правилника.
Б) МЕТОДЕ УЗОРКОВАЊА
Б.1. Општa правила
Б.1.1. Лице које обавља узорковање
Узорковање обавља надлежни инспектор, у складу са поделом надлежности уређеном прописом који се односи на безбедност хране.
Б.1.2. Храна која се узоркује
Свака производна партија или потпартија хране предвиђена за испитивање узоркује се посебно.
––––––––
56 Прилог 5 овог правилника усклађен је са Уредбом Комисије (ЕУ) број 2015/705 од 30. априла 2015. године о утврђивању метода узорковања и критеријума изводљивости за методе испитивања за службену контролу нивоа ерука киселине у прехрамбеним производима и о стављању ван снаге Директиве Комисије 80/891/ЕЕЗ (Commission Regulation (EU) 2015/705 of 30 April 2015 laying down methods of sampling and performance criteria for the methods of analysis for the official control of the levels of erucic acid in foodstuffs and repealing Commission Directive 80/891/EEC)
Б.1.3. Мере предострожности
Током узорковања хране предузимају се мере предострожности како би се избегле било какве промене које би могле утицати на нивое ерука киселине у храни, негативно утицати на лабораторијско испитивање или би због тих промена збирни узорци постали нерепрезентативни.
Б.1.4. Појединачни узорци
Када год је то могуће, појединачни узорци се узимају са различитих места у серији или подсерији.
Одступање од поступка узимања појединачних узорака наводи се у записнику о узорковању из одељка Б) пододељак Б.1 тачка Б.1.8. овог прилога.
Б.1.5. Припрема збирног узорка
Збирни узорак се добија обједињавањем појединачних узорака.
Б.1.6. Контролни узорци и узорци за суперанализу
Контролни узорци и узорци за суперанализу узимају се из хомогенизованог збирног узорка.
Б.1.7. Паковање и достављање узорака
Сваки узорак ставља се у чисту, инертну посуду, кесу или контејнер који пружа одговарајућу заштиту од контаминације, губитка аналита адсорпцијом на унутрашњим зидовима посуде/кесе/контејнера и оштећења приликом преноса и/или транспорта. Потребно је предузети све мере предострожности како би се избегла промена састава узорака до које би могло доћи током транспорта или складиштења.
Б.1.8. Пломбирање и означавање узорака
Сваки узорак који се узима за службену контролу се пломбира и означава на месту узорковања.
О сваком узорковању сачињава се записник о узорковању који омогућава да свака производна партија или потпартија буде недвосмислено идентификована и у којем се наводи број производне партије/потпартије, датум и место узорковања, заједно са додатним подацима који би могли бити од користи при лабораторијском испитивању.
Б.2. Планови узорковања
Б.2.1. Подела производне партије на потпартије
Велике производне партије деле се на потпартије под условом да се потпартија може и физички одвојити. За храну која се продаје у расутом стању за поделу прозводне партије на потпартије примењује се Табела 1. овог прилога. За остале производе примењује се Табела 2. овог прилога. Узимајући у обзир да маса производне партије није увек тачан збир маса потпартија, маса потпартије може прећи доленаведену масу за највише 20%.
Табела 1.
Подела производних партија на потпартије за храну која се продаје у расутом стању
|
Маса производне партије (у t) |
Маса (у t) или број потпартија |
|
≥ 1500 |
500 t |
|
> 300 и < 1500 |
3 потпартије |
|
≥ 100 и ≤ 300 |
100 t |
|
< 100 |
– |
Табела 2.
Подела производних партија на потпартије за осталу храну
|
Маса производне партије (у t) |
Маса (у t) или број потпартија |
|
≥ 15 |
15–30 t |
|
< 15 |
– |
Б.2.2. Број, маса и запремина појединачних узорака
Збирни узорак је најмање 1 kg или 1 l, осим ако то није могуће, нпр. ако се узорак састоји од једног паковања или јединице.
Минималан број појединачних узорака који се узима из производне партије или потпартије наведен је у Табели 3. овог прилога.
Табела 3.
Минималан број појединачних узорака који се узима из производне партије или потпартије
|
Маса или запремина производне партије/потпартије (у kg или l) |
Минималан број појединачних узорака које треба узети |
|
< 50 |
3 |
|
≥ 50 и ≤ 500 |
5 |
|
> 500 |
10 |
У случају да се ради о течним производима у великим паковањима, производне партије или потпартије треба темељно промешати непосредно пре узорковања, колико год је то могуће, ручно или помоћу механичких уређаја, у мери у којој то неће утицати на квалитет производа. У том случају се претпоставља да ће се контаминенти равномерно распоредити кроз целу производну партију или потпартију. Стога, да би се формирао збирни узорак, из производне партије или потпартије треба узети три појединачна узорка.
Појединачни узорци су сличне масе/запремине. Маса/запремина појединачних узорака је најмање 100 g или 100 ml, а збирни узорак је најмање 1 kg или 1 l. Одступање од ове методе наводи се у записнику о узорковању из одељка Б) пододељак Б.1 тачка Б.1.8. овог прилога.
Ако се прозводна партија или потпартија састоји од појединачних паковања или јединица, број паковања или јединица (појединачни узорци) које се узимају за збирни узорак треба да буде у складу са Табелом 4. овог прилога.
Табела 4.
Број паковања или јединица (појединачних узорака) који се узоркују за збирни узорак, кад се производна партија или потпартија састоји од појединачних паковања или јединица
|
Број паковања или јединица у производној партији/потпартији |
Број паковања или јединица које треба узети |
|
≤ 25 |
најмање 1 паковање или јединица |
|
26 до 100 |
око 5%, а најмање 2 паковања или јединице |
|
> 100 |
око 5%, а највише 10 паковања или јединица |
Ако узорковање није могуће због неприхватљивих комерцијалних последица (на пример због облика паковања, оштећења у производној партији и сл.) или када није могуће применити горенаведену методу узорковања, узорковање се може спровести алтернативном методом, под условом да је та метода репрезентативна за узорковану производну партију или потпартију и да је у потпуности документована. То се уноси у записник из одељка Б) пододељак Б.1 тачка Б.1.8. овог прилога.
Б.3. Узорковање у фази малопродаје
Узорковање хране у малопродаји спроводи се у складу са одељком Б) пододељак Б.2 тачка Б.2.2. овог прилога.
Ако узорковање није могуће због неприхватљивих комерцијалних последица (на пример због облика паковања, оштећења у производној партији и сл.) или када није могуће применити горенаведену методу узорковања, узорковање се може спровести алтернативном методом, под условом да је та метода репрезентативна за узорковану производну партију или потпартију и да је у потпуности документована. То се уноси у записник из одељка Б) пододељак Б.1. тачка Б.1.8. овог прилога.
В) ПРИПРЕМА И ИСПИТИВАЊЕ УЗОРАКА
В.1. Лабораторијски стандарди квалитета
Лабораторије које спроводе испитивања хране на присуство конатаминената за службену контролу треба да учествују у одговарајућим лабораторијским проверама квалитета рада у складу са Међународним усклађеним протоколом за проверу квалитета рада (хемијских) аналитичких лабораторија57 развијеним у складу са IUPAC/ISO/АОАC.
Лабораторије требa да имају успостављен интерни систем за контролу квалитета. Примери за то су Смернице IUPAC/ISO/АОАC за интерну контролу квалитета у аналитичким хемијским лабораторијима58.
Тачност испитивања оцењује се коришћењем у испитивању одговарајућих сертификованих референтних материјала, када год је то могуће.
В.2. Припрема узорка
В.2.1. Мере предострожности и општа правила
Основни захтев је да се припреми репрезентативан и хомоген лабораторијски узорак, без секундарне контаминације.
Сав узорковани материјал који је достављен у лабораторију користи се за припрему лабораторијског узорка.
Усклађеност са прописаним максималним концентрацијама утврђује се на основу концентрације утврђене у лабораторијским узорцима.
В.2.2. Обрада узорка који је примљен у лабораторији
Када је то неопходно, цео збирни узорак фино се самеље и детаљно измеша, користећи поступак којим се доказано постиже потпуна хомогенизација.
В.3. Критеријуми изводљивости за методе испитивања
В.3.1. Дефиниције
Поједини изрази употребљени у овом прилогу имају следеће значење:
1) r јесте поновљивост, односно вредност испод које се може, са одређеном вероватноћом (обично 95%), очекивати да ће износити апсолутна разлика између вредности резултата појединачних испитивања спроведених у условима поновљивости (нпр. исти узорак, исти испитивач, исти инструмент, иста лабораторија и кратак временски размак спровођења), па је због тога r = 2,8 x sr;
2) sr јесте стандардна девијација израчуната из резултата добијених под условима поновљивости;
3) RSDr јесте релативна стандардна девијација израчуната из резултата добијених под условима поновљивости
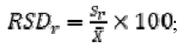
4) R јесте репродуктивност, односно вредност испод које се може, са одређеном вероватноћом (обично 95%), очекивати да ће износити апсолутна разлика између вредности резултата појединачних тестова спроведених у условима репродуктивности (нпр. на идентичном материјалу који су испитивачи добили користећи стандардизовану методу за ипитивање у различитим лабораторијима) R = 2,8 x sr;
5) SR јесте стандардна девијација израчуната из резултата добијених под условима репродуктивности;
6) RSDR јесте релативна стандардна девијација израчуната из резултата добијених под условима репродуктивности
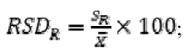
7) LOD јесте граница детекције, односно најмањи измерени садржај из кога се, са оправданом статистичком вероватноћом, може утврдити присуство аналита. Нумерички, граница детекције једнака је трострукој стандардној девијацији средње вредности слепих проба (n > 20);
––––––––
57 Међународни усклађени протокол за проверу квалитета рада (хемијских) аналитичких лабораторија (The international harmonized protocol for the proficiency testing of analytical chemistry laboratories), аутори М. Thompson, S.L.R. Ellison и R. Wood, Pure. Appl. Chem., 2006, 70, 145-196.
58 Приредили М. Thompson и R. Wood, Pure. Appl. Chem., 1995, 67, 649-666.
8) LOQ јесте граница квантификације, односно најмања количина аналита који се може одредити уз одређену статистичку вероватноћу. Ако су и тачност и прецизност константне у концентрацијском распону око границе детекције, тада је граница квантификације нумерички једнака шестострукој или десетострукој стандардној девијацији средње вредности слепих проба (n > 20);
9) u јесте комбинована стандардна мерна несигурност добијена коришћењем појединачних стандардних мерних несигурности које су у вези са улазним количинама у мерном моделу59;
10) U јесте проширена мерна несигурност, добијена коришћењем фактора покривености 2, који даје ниво поузданости од око 95%;
11) Uf јесте највећа стандардна мерна несигурност.
В.3.2. Општи захтеви
Методе испитивања које се користе за потребе службене контроле хране треба да буду у складу са прописом којим се уређује безбедност хране.
В.3.3. Посебни захтеви
В.3.3.1. Критеријуми изводљивости
Када нису прописане посебне методе за одређивање контаминената у храни, лабораторије могу да изаберу било коју валидирану методу испитивања за одређени контаминент, под условом да изабрана метода испуњава посебне критеријуме изводљивости наведене у Табели 5. овог прилога.
Препоручује се примена потпуно валидираних метода (тј. метода које су валидиране међулабораторијским испитивањем дате матрице) према потреби и доступности. Могу се употребљавати и друге одговарајуће валидиране методе (нпр. методе валидиране у лабораторију за дату матрицу) под условом да испуњавају критеријуме изводљивости из Табеле 5. овог прилога.
Детаљни подаци наведени су у Напоменама за критеријуме изводљивости, како је наведено у овој тачки.
Ако је могуће, валидација укључује сертификовани референтни материјал.
Табела 5.
Критеријуми изводљивости за методе испитивања ерука киселине
|
Параметар |
Критеријум |
|
Применљивост |
Храна наведена у посебном пропису о максималним концентрацијама одређених контаминената у храни |
|
Специфичност |
Без спектралних интерференција или утицаја матрикса |
|
Поновљивост (RSDr) |
0,66 х RSDr како је добијена из Horwitz-ове једначине (модификоване) |
|
Репродуктивност (RSDR) |
2 х добијена из Horwitz-ове једначине (модификоване) |
|
Аналитички принос |
95–105% |
|
Граница детекције (LOD) |
≤ 1 g/kg |
|
Граница квантификације (LOQ) |
≤ 5 g/kg |
Напомене за критеријуме изводљивости:
Horwitz-ова једначина60 (за концентрације 1,2 × 10-7 ≤ С ≤ 0,138) и модификована Horwitz-ова једначина61 (за концентрације С < 1,2 × 10-7) су генерализоване једначине за прецизност, независне од аналита и матрикса и зависе искључиво од концентрације за све рутинске методе испитивања.
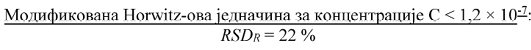
где је:
RSDR релативна стандардна девијација израчуната из резултата добијених у условима репродуктивности
––––––––
59 Међународни речник метрологије – Основни и општи појмови и придружени термини (VIM), JCGM 200: 2008 (International vocabulary of metrology – Basic and general concepts and associated terms (VIM), JCGM 200:2008).
60 W. Horwitz, L.R. Kamps, K.W. Boyer, J.Assoc.Off.Analy.Chem,1980, 63, 1344.
61 Thompson, Analyst, 2000, стр. 125 и 385–386.
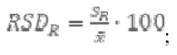
С однос концентрације (тј. 1 = 100 g/100g, 0,001 = 1.000 mg/kg). Модификована Horwitz-ова једначина примењује се за концентрације C < 1,2 × 10-7.
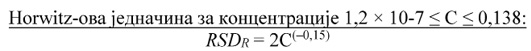
где је:
RSDR релативна стандардна девијација израчуната из резултата добијених у условима репродуктивности
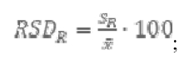
С однос концентрације (тј. 1 = 100 g/100g, 0,001 = 1.000 mg/kg). Horwitz-ова једначина примењује се за концентрације 1,2 × 10-7 ≤ C ≤ 0,138.
В.3.3.2. Приступ „примереност за примену”
За интерно валидoване методе може се користити приступ „примереност за примену”62, као алтернатива за процену њихове примерености за службену контролу. Методе које су примерене за службену контролу треба да дају резултате са комбинованом стандардном мерном несигурношћу (u), којa је мања од највеће стандардне мерне несигурности израчунате уз помоћ следеће формуле:
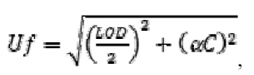
где је:
Uf највећа стандардна мерна несигурност (μg/kg);
граница детекције (LOD) граница детекције методе (μg/kg) која испуњава критеријуме изводљивости из подтачке В.3.3.1. овог прилога за концентрацију која се разматра;
C концентрација која се разматра (μg/kg);
α нумерички фактор који се користи у зависности од вредности C, а вредности које се користе дате су у Табели 6. овог прилога.
Табела 6.
Нумеричке вредности које се користе за константу α, у зависности од концентрације која се разматра
|
C (μg/kg) |
Α |
|
≤ 50 |
0,2 |
|
51 до 500 |
0,18 |
|
501 до 1.000 |
0,15 |
|
1.001 до 10.000 |
0,12 |
|
> 10.000 |
0,1 |
Г) ИЗВЕШТАВАЊЕ И ТУМАЧЕЊЕ РЕЗУЛТАТА
Г.1. Извештавање
Г.1.1. Изражавање резултата
Резултати се изражавају у истим јединицама и заокружују се на исти број децимала као и максималне концентрације уређене посебним прописом који се односи на максималне концентрације одређених контаминената у храни.
Г.1.2. Израчунавање аналитичког приноса
Ако је у аналитичкој методи коришћен поступак екстракције, аналитички резултат се коригује за аналитички принос. У том случају, у извештају се наводи ниво аналитичког приноса.
––––––––
62 M. Thompson and R. Wood, Accred. Qual. Assur, 2006, стр. 10. и 471–478.
Ако се у аналитичкој методи не примењује екстракција, резултат се не коригује за аналитички принос ако је правилним коришћењем одговарајућег сертификованог референтног материјала доказано да је добијена сертификована концентрација унутар граница мерне несигурности (тј. велика тачност мерења). У случају да је резултат изражен без корекције за аналитички принос, то треба и да се наведе у извештају.
Г.1.3. Мерна несигурност
Резултат испитивања изражава се као x +/– U, где је x аналитички резултат, а U је проширена мерна несигурност, добијена коришћењем фактора покривености 2, који даје ниво поузданости од 95% (U = 2u).
Аналитичар узима у обзир и Извештај о односу између аналитичких резултата, мерне несигурности, фактора аналитичког приноса и одредаба законодавства ЕУ о храни и храни за животиње63.
Г.2. Тумачење резултата
Г.2.1. Прихватање производне партије/потпартије
Производна партија или потпартија се прихвата ако аналитички резултат за лабораторијски узорак не прелази прописану максималну концентрацију, узимајући у обзир проширену мерну несигурност и корекцију резултата за аналитички принос, ако је у коришћеној аналитичкој методи примењен поступак екстракције.
Г.2.2. Одбијање производне партије/потпартије
Производна партија или потпартија се одбија ако аналитички резултат за лабораторијски узорак прелази прописану максималну концентрацију, узимајући у обзир проширену мерну несигурност и корекцију резултата за аналитички принос, ако је у коришћеној аналитичкој методи примењен поступак екстракције.
ПРИЛОГ 6
МЕТОДЕ УЗОРКОВАЊА И ИСПИТИВАЊА УЗОРАКА ХРАНЕ ЗА СЛУЖБЕНУ КОНТРОЛУ НИВОА ПЕРФЛУОРАЛКИЛ СУПСТАНЦИ64
Примењују се дефиниције из Прилога 1. одељак А) овог правилника, као и следеће дефиниције:
1) упоредива величина или маса јесте разлика у величини или маси која није већа од 50%;
2) прецизност јесте степен подударности између резултата независних испитивања добијених под прописаним условима. Прецизност се изражава као стандардно одступање или коефицијент варијације резултата испитивања;
3) граница квантификације (LOQ) јесте најмања количина аналита који се може одредити са оправданом статистичком вероватноћом, тј. најнижа концентрација или масени удео аналита који је потврђен са прихватљивом тачношћу применом потпуне аналитичке методе и идентификационих критеријума;
4) комбинована стандардна мерна несигурност (u) јесте параметар који није негативан, а који је повезан са резултатом мерења и означава дисперзију вредности које би се оправдано могле приписати мереној величини на основу коришћених података. Комбинована стандардна мерна несигурност се добија коришћењем појединачних стандардних мерних несигурности које су у вези са улазним количинама у мерном моделу;
––––––––
63 Извештај о односу између аналитичких резултата, мерне несигурности, фактора аналитичког приноса и одредaбa законодавства ЕУ о храни и храни за животиње (Report on the relationship between analytical results, measurement uncertainty, recovery factors and the provisions of EU food and feed legislation) http://ec.europa.eu/food/food/chemicalsafety/ contaminants/report-sampling_analysis_ 2004_en.pdf.
64 Прилог 6 овог правилника усклађен је са Спроведбеном уредбом Комисије (ЕУ) број 2022/1428 од 24. августа 2022. године о утврђивању метода узорковања и испитивања за службену контролу перфлуоралкил супстанци у одређеним прехрамбеним производима (Commission Implementing Regulation (EU) 2022/1428 of 24 August 2022 Laying Down Methods of Sampling and Analysis for the Control of Perfluoroalkyl Substances in Certain Foodstuffs)
5) проширена мерна несигурност (U) јесте вредност добијена коришћењем фактора покривености 2, који даје ниво поузданости од око 95%;
6) истинитост јесте степен подударности између средње вредности добијене из великог низа резултата испитивања и прихваћене референтне вредности. Та се вредност може проценити редовном анализом сертификованих референтних материјала, тестова обогаћивања или учешћем у међулабораторијским испитивањима и изражава се као очигледно одступање.
А) МЕТОДЕ УЗОРКОВАЊА
А.1. Општa правила
А.1.1. Храна која се узоркује
Свака производна партија или потпартија хране предвиђена за испитивање узоркује се посебно.
А.1.2. Појединачни узорци
Када год је то могуће, појединачни узорци се узимају са различитих места у серији или подсерији.
Одступање од поступка узимања појединачних узорака наводи се у записнику о узорковању из одељка А) пододељак А.1. тачка А.1.6. овог прилога.
А.1.3. Припрема збирног узорка
Збирни узорак се добија обједињавањем појединачних узорака. Има најмање 1 kg или 1 l, осим ако то није практично, нпр. ако се узоркује једно паковање или ако производ има врло високу комерцијалну вредност.
А.1.4. Поновљени узорци
Поновљени узорци за сврхе службене контроле, додатна стручна мишљења (жалбе) и судске поступке узимају се из хомогенизованог збирног узорка.
А.1.5. Мере предострожности
Током узорковања хране предузимају се мере предострожности како би се избегле било какве промене које би могле утицати на садржај перфлуоралкилних супстанци у храни, негативно утицати на лабораторијско испитивање или би због тих промена збирни узорци постали нерепрезентативни.
Лице одговорно за узорковање предузима следеће мере предострожности:
– не носи одећу или рукавице које садрже флуорполимерне облоге или које су третиране перфлуоралкилним супстанцама како би се побољшала водоотпорност и отпорност на мрље (прљање);
– на дан узорковања не употребљава хидратизирајућа средства, козметичке производе, креме за руке, производе за заштиту од сунца и сродне производе који садрже перфлуоралкилне супстанце.
Материјали који се употребљавају у току узорковања, складиштења узорка и транспорта узорка не смеју да садрже перфлуороалкилне супстанце. Узорак не сме доћи у контакт са материјалима као што су плоче за резање, посуде за узорке и облоге чепова посуда за узорке који су израђени од политетрафлуоретилена (PTFE или тефлон), поливинилиден флуорида (PVDF) или других флуорполимера. Треба избегавати контакт са другим материјалима који садрже перфлуоралкилне супстанце.
A.1.6. Пломбирање и означавање узорака
Сваки узорак који се узима за службену контролу се пломбира и означава на месту узорковања.
О сваком узорковању сачињава се записник о узорковању који омогућава да свака производна партија или потпартија буде недвосмислено идентификована и у којем се наводи број производне партије/потпартије, датум и место узорковања, заједно са додатним подацима који би могли бити од користи при лабораторијском испитивању и тумачењу резултата.
А.1.7. Паковање и достављање узорака
Сваки узорак ставља се у чисту, инертну посуду, кесу или контејнер, направљене од полипропилена, полиетилена или другог материјала без полифлуоралкил супстанци (PFAS), која пружају одговарајућу заштиту од контаминације, губитка аналита адсорпцијом на унутрашњим зидовима посуде/кесе/контејнера и оштећења приликом преноса и/или транспорта. Употреба стаклених посуда/контејнера није дозвољена. Потребно је предузети све мере предострожности како би се избегла промена састава узорака до које би могло доћи током транспорта или складиштења.
А.2. Планови узорковања
А.2.1. Подела производне партије на потпартије
Велике производне партије деле се на потпартије под условом да се потпартија може и физички одвојити. За храну која се продаје у расутом стању (нпр. биљна уља), за поделу прозводне партије на потпартије примењује се Табела 1. овог прилога. За остале производе примењује се Табела 2. овог прилога. Узимајући у обзир да маса производне партије није увек тачан збир маса потпартија, маса потпартије може прећи доленаведену масу за највише 20%.
Табела 1.
Подела производних партија на потпартије за храну која се продаје у расутом стању
|
Маса производне партије (у t) |
Маса (у t) или број потпартија |
|
≥ 1500 |
500 t |
|
> 300 и < 1500 |
3 потпартије |
|
≥ 100 и ≤ 300 |
100 t |
|
<100 |
– |
Табела 2.
Подела производних партија на потпартије за осталу храну
|
Маса производне партије (у t) |
Маса (у t) или број потпартија |
|
≥ 15 |
15–30 t |
|
< 15 |
– |
А.2.2. Број појединачних узорака
Минималан број појединачних узорака који се узима из производне партије или потпартије наведен је у табелама 3. и 4. овог прилога.
У случају да се ради о течним производима у расутом стању (великим паковањима), производне партије или потпартије треба темељно промешати непосредно пре узорковања, колико год је то могуће, ручно или помоћу механичких уређаја, у мери у којој то неће утицати на квалитет производа. У том случају се претпоставља да ће се контаминенти равномерно распоредити кроз целу производну партију или потпартију. Стога, да би се формирао збирни узорак, из производне партије или потпартије треба узети три појединачна узорка.
Ако се прозводна партија или потпартија састоји од појединачних паковања или јединица, број паковања или јединица (појединачни узорци) које се узимају за збирни узорак треба да буде у складу са Табелом 4. овог прилога.
Појединачни узорци су сличне масе/запремине. Маса/запремина појединачних узорака је најмање 100 g или 100 ml, тако да је збирни узорак најмање 1 kg или 1 l. Када то није могуће, примењује се одељак А) пододељак А.2 тачка А.2.6. овог прилога.
Табела 3.
Минималан број појединачних узорака који се узима из производне партије или потпартије
|
Маса или запремина производне партије/потпартије (у kg или l) |
Минималан број појединачних узорака које треба узети |
|
< 50 |
3 |
|
≥ 50 и ≤ 500 |
5 |
|
> 500 |
10 |
Табела 4.
Број паковања или јединица (појединачних узорака) који се узоркују за збирни узорак, кад се производна партија или потпартија састоји од појединачних паковања или јединица
|
Број паковања или јединица у производној партији/потпартији |
Број паковања или јединица које треба узети |
|
≤ 25 |
најмање 1 паковање или јединица |
|
26 до 100 |
око 5%, а најмање 2 паковања или јединице |
|
> 100 |
око 5%, а највише 10 паковања или јединица |
А.2.3. Посебне одредбе за узорковање производних партија које садрже целе рибе упоредиве величине или масе
Број појединачних узорака који се узимају из производне партије наведен је у Табели 3. овог прилога. Збирни узорак који обједињује све појединачне узорке је најмање 1 kg, како је прописано у одељку А) пододељак А.1. тачка А.1.3. овог прилога.
Када производна партија која се узоркује садржи ситну рибу (појединачне рибе масе < 1 kg), да би се формирао збирни узорак, за формирање збирног узорка се као појединачни узорак узима цела риба. Када је маса добијеног збирног узорка већа од 3 kg, појединачни узорци се могу састојати од средњих делова рибе, од којих је сваки најмање 100 g, а који чине збирни узорак. За хомогенизацију узорка користи се цео део на који се примењује максимално дозвољена концентрација.
Средњи део рибе је тамо где је центар гравитације. У већини случајева налази се на леђној пераји (у случају да риба има леђно пераје) или на пола пута између шкржног отвора и ануса.
Када производна партија која се узоркује садржи веће рибе (појединачне рибе масе ≥ 1 kg), појединачни узорак се састоји од средњег дела рибе. Маса сваког појединачног узорка је најмање 100 g. За рибе средње величине (≥ 1 kg и < 6 kg), појединачни узорак се састоји од комада рибе узетог између кичме и трбуха у средњем делу рибе.
За веома велике рибе (≥ 6 kg), појединачни узорак се узима из меса дорзо-латералног мишића који се налази на десној страни (гледано са предње стране) у средњем делу рибе. Када узимање таквог комада средњег дела рибе може довести до значајне економске штете могу се, без обзира на величину производне партије, прихватити као довољна:
три појединачна узорка који су најмање 350 g или
три појединачна узорка од најмање 350 g, сваки из једнаког дела (175 g) меса мишића узетог близу репа и меса мишића узетог близу главе сваке рибе.
А.2.4. Посебне одредбе за узорковање производних партија које садрже целе рибе различите величине и/или масе
За припрему узорка примењују се правила из одељка А) пододељак А.2. тачка А.2.3. овог прилога.
Када преовлађује риба одређене величине/категорије или масе (око 80% или више производне партије), узорак се узима од рибе преовлађујуће величине или масе. Сматра се да је узорак репрезентативан за целу производну партију.
Када одређена класа/категорија величине или масе не преовлађује, обезбеђује се да риба одабрана за узорак буде репрезентативна за производну партију. За такве случајеве, посебна упутства су дата у Смерницама за узорковање целе рибе различите величине и/или масе65.
А.2.5. Посебне одредбе за узорковање копнених животиња
За месо и изнутрице свиња, говеда, оваца, коза и копитара узима се узорак од 1 kg од најмање једне животиње. Ако није могуће узети узорак од 1 kg од најмање једне животиње, узимају се једнаке количине узорка од више животиња да би се добила количина узорка од 1 kg.
За месо живине, да би се добио збирни узорак од 1 kg, узоркују се једнаке количине од најмање три животиње. За изнутрице живине, да би се добио збирни узорак од 300 g, узоркују се једнаке количине од најмање три животиње.
––––––––
65 https://ec.europa.eu/food/system/files/2022-05/cs_contaminants_sampling_guid-samp-fishes.pdf
За месо и изнутрице дивљачи из узгоја и дивљих копнених животиња узима се узорак од 300 g од најмање једне животиње. Ако није могуће узети узорак од 300 g од најмање једне животиње, узимају се једнаке количине узорка од више животиња да би се добила количина узорка од 300 g.
А.2.6. Алтернативне методе узорковања
Ако узорковање није могуће због неприхватљивих комерцијалних последица (на пример због облика паковања, оштећења у производној партији и сл.) или када није могуће применити горенаведену методу узорковања, узорковање се може спровести алтернативном методом под условом да је та метода репрезентативна за узорковану производну партију или потпартију и да је у потпуности документована. То се уноси у записник из одељка А) пододељак А.1 тачка А.1.6. овог прилога.
А.2.7. Узорковање у фази малопродаје
Узорковање хране у фази малопродаје спроводи се, ако је могуће, у складу сa одредбама из овог одељка. Ако то није могуће, може се применити алтернативна метода узорковања у фази малопродаје, под условом да је довољно репрезентативна за узорковану производну партију или потпартију.
Б) ПРИПРЕМА УЗОРКА И ИСПИТИВАЊЕ
Б.1. Лабораторијски стандарди квалитета
Поштују се принципи наведени у Смерницама референтних лабораторија ЕУ у погледу аналитичких параметара за одређивање перфлуоралкил и полифлуоралкил супстанци у храни и храни за животиње66.
Б.2. Припрема узорка
Б.2.1. Општи захтеви
Основни захтев је да се добије репрезентативан и хомоген лабораторијски узорак без секундарне контаминације.
Комплетан збирни узорак, који је лабораторија примила, фино се самеље, када је то примењиво, и темљно се промеша применом поступка за који је доказано да се њиме постиже потпуна хомогенизација.
За производе који нису риба, сав узорковани материјал који је лабораторија примила, на који се примењује максимална концентрација, употребљава се за припрему лабораторијског узорка.
За рибу, сав узорковани материјал који је лабораторија примила и на који се примењује максимална концентрација, хомогенизује се. Репрезентативни део или количина хомогенизованог збирног узорка користи се за припрему лабораторијског узорка.
Усаглашеност са прописаним максималним концентрацијама утврђује се на основу нивоа утврђених у лабораторијским узорцима.
Б.2.2. Посебни поступци припреме узорака и мере предострожности
У току припреме узорака, аналитичар треба да обезбеди да се узорци не контаминирају, пратећи мере предострожности прописане у одељку А) пододељак А.1. тачка А.1.5. овог прилога. Штавише, кад год је то могуће, уређаји и опрема који долазе у контакт са узорком не треба да садрже перфлуоралкилне супстанце и замењују се нпр. деловима од нерђајућег челика, полиетилена високе густоће (HDPE) или полипропилена. Они се чисте водом, растварачима или детергентима који не садрже перфлуоралкилне супстанце.
Реагенси и друга опрема која се користи за испитивање и узорковање треба да се контролише да би се избегло могуће уношење или губитак перфлуоралкилних супстанци.
Слепа проба реагенса се изводи тако што се цео аналитички поступак спроводи на исти начин као и узорак за испитивање. При припреми слепих проба реагенса, уместо матрице може се употребити вода. Количине у слепим пробама реагенса прате се у свакој серији узорака.
––––––––
66 https://ec.europa.eu/food/system/files/2022-05/cs_contaminants_sampling_guid-doc-analyt-para_0.pdf
Б.3. Методе испитивања: посебни захтеви у погледу изводљивости
Лабораторије могу одабрати било коју валидирану методу испитивања за одговарајућу матрицу, под условом да одабрана метода испуњава посебне критеријуме изводљивости из Табеле 5. овог прилога.
Примењују се потпуно валидиране методе (тј. методе потврђене међулабораторијским испитивањем одговарајуће матрице) или, ако то није могуће, друге валидиране методе (нпр. интерно валидиране методе за одговарајућу матрицу), под условом да испуњавају критеријуме изводљивости из Табеле 5. овог прилога.
Ако је могуће, валидација интерно валидираних метода укључује употребу сертификованог референтног материјала и/или суделовање у међулабораторијским студијама.
Табела 5.
|
Параметар |
Критеријум |
|
Применљивост |
Храна наведена у посебном пропису којим којим се уређују максималне концентрације одређених контаминената у храни |
|
Селективност |
Аналитичким методама доказује се способност поузданог и доследног одвајања предметних аналита од других истовремено екстрахованих и потенцијално интерферирајућих једињења која могу бити присутна. |
|
Интра-лабораторијска поновљивост (средња прецизност) (RSDR) |
≤ 20% |
|
Истинитост |
oд – 20% дo + 20% |
|
Граница квантификације (LOQ) |
Граница квантификације за PFOS, PFOA, PFNA и PFHxS je ≤ максималним прописаним концентрацијама (нивоима) за одговарајућу појединачну перфлуоралкил супстанцу (PFAS). Усклађеност са овим захтевом подразумева да се граница квантификације не ради за концентрацију суме PFOS, PFOA, PFNA и PFHxS, која се израчунава сабирањем само концентрација PFOS, PFOA, PFNA и PFHxS које су одређене на одговарајућој граници или изнад ње. |
PFAS = Перфлуоралкил супстанце
PFOS = Перфлуороктан сулфонат или перфлуороктан сулфонска киселина
PFOA = Перфлуороктанска киселина
PFNA = Перфлуорнонанска киселина
PFHxS = Перфлуорхексансулфонска киселина
В) ИЗВЕШТАВАЊЕ И ТУМАЧЕЊЕ РЕЗУЛТАТА
В.1. Извештавање
В.1.1. Изражавање резултата
Резултати се исказују као анјони и изражавају се у истим јединицама и заокружују на исти број битних децималних места као прописане максималне концентрације. За израчунавање суме PFOS, PFOA, PFNA и PFHxS узимају се у обзир само концентрације на граници квантификације или изнад те границе.
В.1.2. Мерна несигурност
Аналитички резултат изражава се као „x ± У”, при чему је „x” аналитички резултат, а „У” је проширена мерна несигурност, добијена коришћењем фактора покривености 2, који даје ниво поузданости од 95% (У = 2у).
За извештавање о параметрима суме и могуће поређење са законским границама, за ове параметре суме урадиће се такође и процена проширене мерне несигурности. За перфлуоралкилне супстанце то је случај за суму PFOS, PFOA, PFNA и PFHxS и за укупне PFOS, ако се израчунава као сума линеарних и разгранатих PFOS.
У тим случајевима се комбинована стандардна мерна несигурност „у” параметра суме израчунава као квадратни корен суме квадрата појединачних комбинованих несигурности.
Аналитичар узима у обзир и Извештај о односу између аналитичких резултата, мерне несигурности, фактора аналитичког приноса и одредаба законодавства ЕУ о храни и храни за животиње67.
––––––––
67 https://ec.europa.eu/food/system/files/2016-10/cs_contaminants_sampling_analysis-report_2004_en.pdf
В.2. Тумачење резултата
В.2.1. Прихватање производне партије или потпартије
Производна партија или потпартија се прихватају ако аналитички резултат лабораторијског узорка не премашује одговарајућу максималну концентрацију уређену у посебном пропису који се односи на максималне концентрације одређених контаминената у храни, узимајући у обзир проширену мерну несигурност.
В.2.2. Одбијање производне партије или потпартије
Производна партија или потпартија се одбијају ако аналитички резултат лабораторијског узорка премашује одговарајућу максималну концентрацију уређену у посебном пропису који се односи на максималне концентрације одређених контаминената у храни, узимајући у обзир проширену мерну несигурност.
В.2.3. Применљивост
Oвa правила за тумачење резултата примењују се на аналитички резултат добијен на узорку узетом за сврхе службене контроле.